四川2018年高二化学上半年期中考试免费试卷完整版
| 1. 选择题 | 详细信息 |
|
化学与生产、生活密切相关,下列应用和判断不正确的是 A. 化石燃料终将枯竭,解决能源危机的办法是加大化石燃料的开采、储存 B. 节日燃放的焰火与原子核外电子的跃迁有关 C. 生活中常用的肥皂和洗涤剂既含有亲水基团,也含有疏水基团 D. 夏天当厕所里比较刺鼻时,用大量水冲洗可避免其气味,利用了气体的相似相溶原理。 |
|
| 2. 选择题 | 详细信息 |
|
下列溶液中不存在配离子的是 A. CuSO4水溶液 B. 银氨溶液 C. 硫氰化铁溶液 D. I2的CCl4溶液 |
|
| 3. 选择题 | 详细信息 |
|
在以离子键为主的化学键中常含有共价键的成分,两种元素电负性差异越小,其共价键成分越大。下列各对原子形成的化学键中共价键成分最多的是 A. K与F B. Na与F C. Al与Cl D. Mg与Cl |
|
| 4. 选择题 | 详细信息 |
|
下列原子外围电子层的电子排布图正确的是( ) A. O C. Si |
|
| 5. 选择题 | 详细信息 |
|
下列各微粒的电子式书写正确的是 A.甲基  C. NH4H 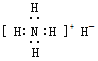 D.硫化氢 D.硫化氢 |
|
| 6. 选择题 | 详细信息 |
|
下列说法不正确的是 A. 风能、太阳能等属于一次能源 B. X C. 化学反应的焓变ΔH越大,表示放热越多 D. 稀溶液中,酸碱中和反应生成1 mol H2O时放热不一定为57.3 kJ |
|
| 7. 选择题 | 详细信息 |
|
某微粒的核外电子排布式为1s22s22p6,下列说法不正确的是 A. 可以确定该微粒为Ne B. 对应元素可能位于元素周期表中第13列 C. 它的单质可能是强还原剂 D. 对应元素可能是电负性最大的元素 |
|
| 8. 选择题 | 详细信息 |
|
已知钛有48Ti、49Ti、50Ti等同位素,下列关于金属钛的叙述中不正确的是 A. 上述钛原子中,中子数不可能为22 B. 钛元素在周期表中处于第四周期ⅡB族 C. 钛原子的外围电子层排布为3d24s2 D. 钛元素位于元素周期表的d区,是过渡元素 |
|
| 9. 选择题 | 详细信息 |
|
用VSEPR模型预测下列分子或离子的立体结构,其中正确的是 ( ) A. H2O与BeCl2为角形(V形) B. CS2与SO2为直线形 C. SO3与CO |
|
| 10. 选择题 | 详细信息 |
|
“类推”是一种重要的学习方法,但有时会产生错误结论,下列类推结论中正确的是 A.碱金属氟化物的晶格能顺序是LiF>NaF>KF>RbF>CsF;则钠的卤化物的晶格能顺序是NaF>NaCl>NaBr>NaI B.ⅣA族元素氢化物沸点顺序是GeH4>SiH4>CH4;则ⅤA族元素氢化物沸点顺序是AsH3>PH3>NH3 C.晶体中有阴离子,必有阳离子;则晶体中有阳离子,必有阴离子 D.若盐酸的浓度是醋酸浓度的2倍;则盐酸中H+浓度也是醋酸中H+浓度的2倍 |
|
| 11. 选择题 | 详细信息 |
某反应过程能量变化如图所示,下列说法正确的是 ( )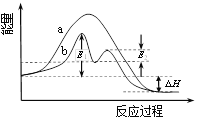 A. 反应过程a有催化剂参与 B. 该反应为吸热反应,热效应等于∆H C. 改变催化剂,可改变该反应的活化能 D. 有催化剂的条件下,反应的活化能等于E1+E2 |
|
| 12. 选择题 | 详细信息 |
|
已知,在25℃、101 kPa时:① C(s)+O2(g)==CO2(g) ΔH=-393.5 kJ/mol ② 2C(s)+O2(g)==2CO(g) ΔH=-221.0 kJ/mol ③ 2H2(g)+O2(g)==2H2O(g) ΔH=-483.6 kJ/mol 下列判断不正确的是 A.6g碳完全燃烧时放出热量196.8 kJ B.CO的燃烧热ΔH=-283.0 kJ/mol C.H2的燃烧热ΔH=-241.8 kJ/mol D.制备水煤气的反应热ΔH=+131.3 kJ/mol |
|
| 13. 选择题 | 详细信息 |
|
关于晶体下列各种说法错误的是 A. 分子晶体中分子间的作用力相对于化学键较弱,故熔、沸点较低 B. 金刚石和晶体硅是结构相似的原子晶体,但金刚石的熔点比晶体硅高 C. 固体NaCl和MgO都是型离子晶体,但NaCl的晶格能小于MgO D. 固体石墨能导电,属于金属晶体 |
|
| 14. 选择题 | 详细信息 |
|
在中和反应反应热的测定实验中,下列实验误差分析结论不正确的是 A. 若将NaOH溶液分多次倒入盐酸中,测得温度计的最高读数偏小 B. 若将环形玻璃搅拌棒换成铜棒,测得温度计的最高读数偏小 C. 若将稀盐酸换成浓硫酸,测得的反应热ΔH偏大 D. 若大小烧杯的烧杯口未对齐,测得的反应热ΔH偏大 |
|
| 15. 选择题 | 详细信息 |
设NA为阿伏加德罗常数的值,下列叙述错误的是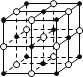 A. 含16 g氧原子的二氧化硅晶体中含有的σ键数目为2NA B. 58.5 g NaCl晶体中含有0.25NA个右图所示的结构单元 C. 常温常压下,5 g D2O含有的质子数、电子数、中子数均为2.5NA D. 2 mol SO2和1 mol O2在一定条件下反应所得混合气体分子数小于2NA |
|
| 16. 选择题 | 详细信息 |
|
下列说法错误的是 A.在熔化状态下能导电的化合物一定是离子晶体 B.分子晶体的状态变化只需克服分子间作用力 C.金属键的本质是金属离子与自由电子间的相互作用 D.原子晶体中只存在非极性共价键 |
|
| 17. 选择题 | 详细信息 |
|
已知:H2(g)+1/2O2(g)===H2O(g) ΔH1=-241.8 kJ·mol-1,C(s)+1/2O2(g)===CO(g) ΔH2=-110.5 kJ·mol-1。由此可知焦炭与水蒸气反应的热化学方程式为:C(s)+H2O(g)===CO(g)+H2(g) ΔH3,则ΔH3为( ) A. +131.3 kJ·mol-1 B. -131.3 kJ·mol-1 C. +352.3 kJ·mol-1 D. -352.3 kJ·mol-1 |
|
| 18. 填空题 | 详细信息 |
|
A、B、D、E、G、M六种元素位于元素周期表前四周期,原子序数依次增大。其中,元素A的一种核素无中子,B的单质既有分子晶体又有原子晶体,化合物DE2为红棕色气体,G是前四周期中电负性最小的元素,M的原子核外电子数比G多10。 请回答下列问题: (1)基态G原子的核外电子排布式是___________,M在元素周期表中的位置是_______,元素B、D、E的第一电离能由大到小的顺序为______________________(用元素符号表示)。 (2)元素A和E组成的阳离子空间构型为__________________________;化合物ABD的结构式为____________,其中B原子的杂化方式为____。 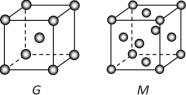 (3)G、M的晶体晶胞结构如图所示,这两种晶胞中原子的配位数之比为___________。若晶体M密度为8.9 g·cm-3,则M的晶胞边长是____________________cm(不必计算出结果)。 |
|
| 19. 综合题 | 详细信息 |
(1)碳的一种单质的结构如图(a)所示。该单质的晶体类型为___________,碳原子的杂化轨道类型为_________。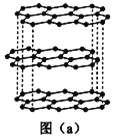 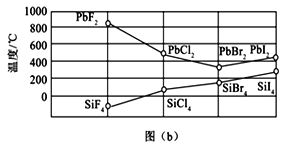  (2)SiCl4分子的中心原子的价层电子对数为__________,分子的立体构型为_______。 (3)四卤化硅SiX4的沸点和二卤化铅PbX2的熔点如图(b)所示。 SiX4的沸点依F、Cl、Br、I次序升高的原因是:______________________________________。 (4)碳的另一种单质C60可以与钾形成低温超导化合物,晶体结构如图(c)所示。K位于立方体的棱上和立方体的内部,此化合物的化学式为_______________;其晶胞参数为1.4 nm,晶体密度为___________________________________g·cm-3(列式并计算保留1位小数)。 |
|
| 20. 综合题 | 详细信息 |
|
M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y的负一价离子的最外层电子数与次外层的相同。回答下列问题: (1)单质M的晶体中原子间通过______________________作用形成面心立方密堆积,其中M原子的配位数____________。 (2)元素Y的含氧酸中,酸性最强的是________________(写化学式),该酸根离子的立体构型为______________________。 (3)M与Y形成的一种化合物的立方晶胞如图所示。 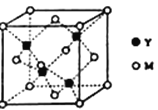 ①该化合物的化学式为______________________,已知晶胞参数a=0.542 nm,此晶体的密度为__________________________g·cm–3。(只写出计算式,阿伏加德罗常数为NA) ②该化合物难溶于水但易溶于氨水,其原因是:_____________________________________。 |
|
| 21. 填空题 | 详细信息 | ||||||||||
|
PCl3和Cl2在一定条件下反应生成PCl5。 (1)有88 g CO2与足量H2恰好完全反应,生成气态水和甲醇,可放出1.2014×105 J的热量,试写出该反应的热化学方程式_______________________________________。 (2)25 ℃、101 kPa下,CH4的燃烧热为a kJ/mol,9 g液态水变为水蒸气吸热b kJ,则CH4燃烧生成二氧化碳和水蒸气热化学方程式为________________________________。 (3)硅与氯两元素的单质反应生成1mol硅的最高价化合物,恢复至室温,放热687kJ,已知该化合物的熔、沸点分别为-69℃和58℃,写出该反应的热化学方程式:________________________________________________。 (4)CO2与CH4经催化重整制得合成气:CH4(g)+ CO2(g)
|
|||||||||||
最近更新