湖南省长沙市长郡中学2020-2021年高二上半年入学考试化学题带参考答案
| 1. 选择题 | 详细信息 |
|
在配制一定物质的量浓度的溶液的实验中,不会选用的仪器是( ) A.  B. B. C. C. D. D. |
|
| 2. 选择题 | 详细信息 |
|
下列气体中,既可用浓硫酸干燥,又可用生石灰干燥的是( ) A.Cl2 B.NH3 C.SO2 D.CH4 |
|
| 3. 选择题 | 详细信息 |
|
在抗击“新冠肺炎”疫情中,广泛使用化学药剂对公共场所进行消毒。下列物质不能作为此消毒液的是( ) A.“84”消毒液 B.NaHCO3溶液 C.KMnO4溶液 D.75%的医用酒精 |
|
| 4. 选择题 | 详细信息 |
|
BaSO4在医疗上称作钡餐。下列关于 A.中子数是56 B.核外电子数是81 C.质量数是137 D.第六周期IA族元素 |
|
| 5. 选择题 | 详细信息 |
|
在溶液中加入适量Na2O2后仍能大量共存的是( ) A.NH B.Na+、Mg2+、C1-、C1O- C.Cu2+、Na+、NO D.K+、A1O |
|
| 6. 选择题 | 详细信息 |
|
反应2Al+WO3=W+Al2O3可用于制备金属钨(W)。下列关于该反应的说法正确的是( ) A.WO3是还原剂 B.Al失去电子 C.Al被还原 D.WO3发生氧化反应 |
|
| 7. 选择题 | 详细信息 |
|
下列关于苯的叙述正确的是( ) A.分子中含有碳碳双键,属于不饱和烃 B.分离苯与蒸馏水应采用蒸馏的方法 C.苯的化学性质很稳定,但能跟溴水发生取代反应 D.不能使酸性高锰酸钾溶液褪色 |
|
| 8. 选择题 | 详细信息 |
|
有关煤、石油和天然气的综合利用,下列说法正确的是( ) A.水煤气的主要成分是CH4 B.煤的气化和液化、石油的分馏都是物理变化 C.裂解的目的是提高汽油的产量 D.直馏汽油和裂化汽油可用KMnO4溶液鉴别 |
|
| 9. 选择题 | 详细信息 |
|
下列物质不能发生水解的是( ) A.葡萄糖 B.蔗糖 C.油脂 D.淀粉 |
|
| 10. 选择题 | 详细信息 |
某反应由两步反应A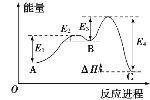 A.两步反应均为吸热反应 B.三种化合物中C最稳定 C.A与C的能量差为E4 D.A |
|
| 11. 选择题 | 详细信息 |
|
为除去食盐中少量的SO A.加过量BaCl2溶液,过滤 B.加过量BaCl2溶液,过滤,然后加过量的盐酸 C.加过量BaCl2溶液,再加过量Na2CO3溶液,过滤后加过量的盐酸,蒸发 D.加过量BaCl2溶液,过滤,再加入过量Na2CO3溶液,然后加过量的盐酸 |
|
| 12. 选择题 | 详细信息 |
|
化学与环境密切相关,下列有关说法正确的是 A.CO2属于大气主要污染物 B.大气中CO2含量的增加会导致温室效应 C.CO2或NO2都会导致酸雨的形成 D.酸雨是pH小于7的雨水 |
|
| 13. 选择题 | 详细信息 | ||||||||
一定温度下,在2L恒容密闭容器中发生反应:H2(g)+I2(g)
|
|||||||||
| 14. 选择题 | 详细信息 |
化学能与电能等能相互转化,根据如图所示装置,下列说法正确的是( )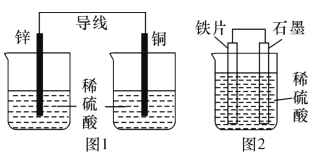 A.图1、图2都能将化学能转化为电能 B.图1中锌、铜都溶解 C.图2中铁失去电子,石墨得到电子 D.图2中铁作负极,电极反应为Fe-2e-=Fe2+ |
|
| 15. 选择题 | 详细信息 |
|
NA表示阿伏加德罗常数的值。在标准状况下,下列说法正确的是( ) A.22.4L乙烯的分子中含有共价键为5NA B.11.2LHC1和11.2LNH3混合,所含分子数为NA C.11.2LNO和11.2LO2混合气体充入密闭容器,所含分子数小于NA D.0.1mo1/LBaC12溶液中含有Ba2+数为0.1NA |
|
| 16. 选择题 | 详细信息 |
|
某溶液中可能含有K+、NH ①在一份溶液中加入足量NaOH,加热,可收集到标准状态下的气体1.12L; ②在另一份溶液中加入足量Ba(NO3)2溶液,有白色沉淀产生,过滤得到沉淀2.33g; ③在②的滤液中加入足量AgNO3溶液,又有4.7g沉淀产生。 有关该溶液中离子种类(不考虑H+和OH-)的判断正确的是( ) A.原溶液中至少有2种阳离子 B.能确定的只有溶液中NH C.原溶液中最多有4种阴离子 D.原溶液中可能同时存在K+和NO |
|
| 17. 选择题 | 详细信息 |
向盛有紫色石蕊溶液的试管中持续通入氯气,溶液颜色呈如下变化: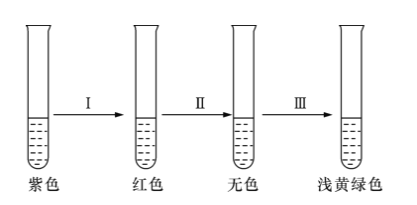 关于I、II、III步溶液中导致变色的微粒的对应判断,正确的是( ) A.H+、HClO、Cl2 B.H+、ClO-、Cl- C.H+、Cl-、ClO- D.HClO、H+、Cl2 |
|
| 18. 选择题 | 详细信息 | ||||||||||||||||||||
下列实验现象所对应的化学方程式或离子方程式正确的是( )
|
|||||||||||||||||||||
| 19. 选择题 | 详细信息 |
|
“清肺排毒汤”来源于中医经典方剂组合,可用于治疗新型冠状病毒感染。其中有一味中药成分麻黄碱的结构简式及提取部分流程如图所示,下列说法正确的是( ) 麻黄碱结构简式: 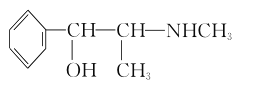 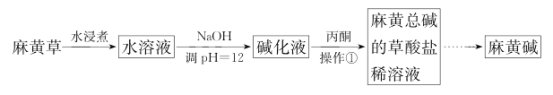 A.麻黄碱难溶于水 B.操作①是使麻黄碱溶于丙酮,属于过滤操作 C.麻黄碱分子中所有碳原子位于同一平面上 D.麻黄碱分子式是C10H15ON |
|
| 20. 选择题 | 详细信息 |
|
四种主族元素的离子aXm+、bYn+、cZn-和dRm-(a、b、c、d为元素的原子序数),它们具有相同的电子层结构,若m>n,则下列叙述的判断正确的是( ) A.a-b=n-m B.元素的原子序数a>b>c>d C.最高价氧化物对应水化物的碱性X>Y D.离子半径r(Rm-)>r(Zn-)>r(Yn+)>r(Xm+) |
|
| 21. | 详细信息 |
|
A、B、C、D是四种原子序数依次增大的短周期元素,A最外层电子数是其内层电子数的2倍,B的单质在空气中含量最多,C是短周期中金属性最强的元素,D最外层电子数与其电子层数相等。请回答下列问题: (1)A、C两种元素的名称分别是:A___,C___; (2)D位于周期中第___周期___族。 (3)A的最高价氧化物的电子式是___; (4)B的最简单氢化物的化学式是___,其化学键类型为___; (5)D的最高价氧化物与C的最高价氧化物对应的水化物在溶液中反应的离子方程式为___。 |
|
| 22. | 详细信息 |
碘是人体必需的元素之一,海洋植物如海带、海藻中含有丰富的以碘离子形式存在的碘元素。在实验室中,从海藻里提取碘的流程如图: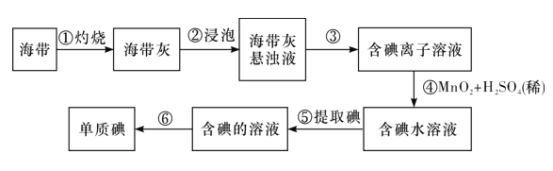 (1)实验操作步骤⑥的名称为___; (2)写出步骤④对应反应的离子方程式:___; (3)检验碘水中是否含有碘的方法是加入淀粉溶液,看溶液是否变___色; (4)提取碘的过程中,步骤⑤可供选择的试剂是___(填标号) A.酒精 B.醋酸 C.烧碱 D.苯 选择该种试剂的理由是___。 |
|
| 23. | 详细信息 |
消毒剂过氧乙酸具有很强的氧化性和腐蚀性。以乙烯为原料经过一系列反应可生产过氧乙酸,其合成路线如图: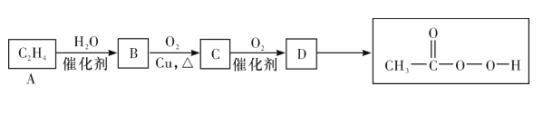 请回答下列问题: (1)A→B的反应类型是___,C的官能团名称是___; (2)D的结构简式为___; (3)浓过氧乙酸溶液中加入少许紫色石蕊试液,溶液最终为___。 (4)过氧乙酸与乳酸(  ),是否为同系物?___(填“是”或“否”) ),是否为同系物?___(填“是”或“否”)(5)写出B→C反应的化学方程式:___。 |
|
| 24. | 详细信息 |
以高硫铝土矿(主要成分为A12O3、Fe2O3、SiO2,少量FeS2和金属硫酸盐)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如图: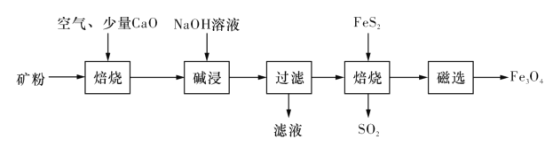 请回答下列问题: (1)矿粉焙烧时加少量CaO,主要目的是将SiO2转化为___(填化学式)。 (2)过滤后的固体焙烧时产生的SO2气体可以用___(填标号)吸收; A.浓硫酸 B.NaOH溶液 C.水 (3)可以将少量Fe3O4产品溶于稀硫酸中,再滴入酸性高锰酸钾溶液,若溶液褪色,能否证明产品中含有FeO?___ (填“能”或“否”); (4)过滤后的滤液中的铝元素主要以___(填化学式)离子存在,可以往滤液中通入过量二氧化碳,经过滤、灼烧生产氧化铝。请写出往滤液中通入过量二氧化碳的化学方程式___。 |
|
| 25. 实验题 | 详细信息 |
从有机反应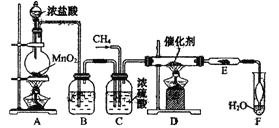 (1)写出实验室制Cl2的离子方程式________________________。 (2)装置B中盛放的溶液是____________;作用是___________________。 (3)装置C有三种功能:①_________;②__________;③观察气泡的产生情况,便于控制两种气体的配比。 (4)玻璃管E中放在石棉碎块上的碘化钾的作用是:_______________。导管末端“肚形”装置的作用是____________________________。 (5)从F中分离出盐酸的最佳方法是____________。该套实验装置还存在的缺陷是_______。 |
|
| 26. 计算题 | 详细信息 |
硫酸铜晶体受热脱水是分步进行的。现取1.60gCuSO4·5H2O样品,在隔绝空气条件下受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示。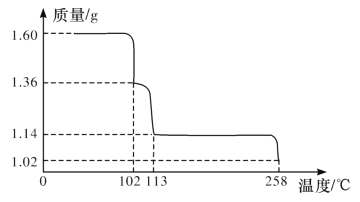 请回答下列问题: (1)试确定200℃时:①固体物质的化学式___; ②写出推断计算过程:___。 (2)取270℃所得样品,于570℃灼烧得到的主要产物是黑色粉未和一种氧化性气体,该反应的化学方程式为___。把该黑色粉未溶解于稀硫酸中,经浓缩、冷却,有晶体析出,该晶体的化学式为___,其存在的最高温度是___; (3)上述氧化性气体与水反应生成一种化合物,该化合物的浓溶液与Cu在加热时发生反应的化学方程式为___。 |
|
最近更新



