云南高一化学期中考试(2019年上册)免费试卷
| 1. 选择题 | 详细信息 |
|
下列有关实验操作正确的是( ) A.点燃酒精灯  B.称量10.05g固体 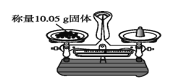 C.检查容量瓶是否漏水 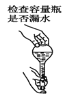 D.量取9.5mL液体 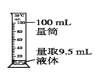 |
|
| 2. 选择题 | 详细信息 |
|
下列物质中,既属于电解质又能导电的是( ) A.二氧化硫 B.NaOH溶液 C.石墨 D.熔融的KNO3 |
|
| 3. 选择题 | 详细信息 |
|
下列反应不属于氧化还原反应的是 ( ) A.3Fe + 4H2O(g) B.3NO2 +H2O = 2HNO3+ NO C.Ca(OH)2+SO2 = CaSO3 + H2 O D.Cu+2H2SO4 (浓) |
|
| 4. 选择题 | 详细信息 |
|
胶体区别于其他分散系的本质特征是( ) A.分散质粒子能作不停的、无规则的运动 B.光线透过时能观察到光亮的通路 C.静置后既不分层,也无沉淀产生 D.分散质粒子直径在10-9~10-7 m之间 |
|
| 5. 选择题 | 详细信息 |
|
用NA表示阿伏加德罗常数的值,下列说法中正确的是( ) A.标准状况下,22.4 L三氧化硫中含有的分子数为NA B.0.5 mol·L-1的Na2SO4溶液中,含有Na+的个数为NA C.标准状况下,22.4L二氧化硫与22.4L氧气所含的原子总数均为2NA D.32 g 氧气所含的氧原子数目为2NA |
|
| 6. 选择题 | 详细信息 |
|
分类法在化学学科的发展中起到了非常重要的作用,下列分类标准合理的是( ) A. 根据是否含氧元素,将物质分为氧化剂和还原剂 B. 根据反应中是否有电子转移,将化学反应分为氧化还原反应和非氧化还原反应 C. 根据水溶液是否能够导电,将物质分为电解质和非电解质 D. 根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体 |
|
| 7. 选择题 | 详细信息 |
|
下列反应中,水作为还原剂的是( ) A.2F2 + 2H2O = 4HF + O2 B.Na2O + H2O = NaOH C.Br2 + H2O |
|
| 8. 选择题 | 详细信息 |
|
在物质分类中,前者包括后者的是 A.氧化物、化合物 B.化合物、电解质 C.溶液、胶体 D.溶液、分散系 |
|
| 9. 选择题 | 详细信息 |
|
配制一定物质的量浓度的NaOH溶液时,使所配制的溶液浓度偏小的操作是 ①将NaOH固体放在纸上称量,再转移到烧杯中溶解 ②烧杯中NaOH溶液移入容量瓶后没有洗涤烧杯 ③实验用的容量瓶洗净后未干燥,里面有少量水 ④定容时俯视容量瓶液面 A.①② B.③④ C.①③ D.②④ |
|
| 10. 选择题 | 详细信息 |
|
在同温同压下,某气体与氮气质量相同,体积比为2:3,则该气体的相对分子量为( ) A.42 B.56 C.21 D.72 |
|
| 11. 选择题 | 详细信息 |
|
在无色强酸性溶液中,下列各组离子能够大量共存的是 ( ) A. Cl -、Na+、NO3-、Ca2+ B. NH4+、HCO3-、Cl-、K+ C. K+、Ba2+、Cl-、SO42- D. Cu2+、NH4+、I-、Cl- |
|
| 12. 选择题 | 详细信息 |
|
下列电离方程式书写正确的是 A. NaOH=Na++O2-+H+ B. FeCl3=Fe3++Cl3- C. Ca(NO3)2=Ca2++2(NO3)2- D. H2SO4=2H++SO42- |
|
| 13. 选择题 | 详细信息 |
|
下列反应中画线物质是还原剂的是( ) A. Zn+H2SO4=ZnSO4+H2↑ B. Cl2+2NaBr=2NaCl+Br2 C. C+CO2 |
|
| 14. 选择题 | 详细信息 |
下列能达到实验目的的是( )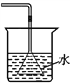  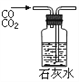 A. 吸收HCl防倒吸 B. 制取少量蒸馏水 C. 转移溶液 D. 除去杂质气体CO2 |
|
| 15. 选择题 | 详细信息 |
|
下列变化过程中,需要加入还原剂才能实现的是( ) A.MnO2→MnO4- B.AlO2-→Al(OH)3 C.AsO33-→AsO43- D.MnO2→MnCl2 |
|
| 16. 选择题 | 详细信息 |
|
某盐的混合物中含有0.2 mol/L Na+、0.4 mol/L Mg2+、0.4 mol/L Clˉ,则SO42ˉ为 A. 0.1 mol/L B. 0.2 mol/L C. 0.3 mol/L D. 0.4 mol/L |
|
| 17. 选择题 | 详细信息 |
|
下列反应的化学方程式不能用离子方程式Ba2++ SO42- =BaSO4↓来表示的是( ) A. Ba(NO3)2+Na2SO4 B. BaCO3+H2SO4 C. H2SO4+BaCl2 D. Ba(NO3)2+H2SO4 |
|
| 18. 选择题 | 详细信息 |
|
下列氧化还原反应中,电子转移的方向和数目均正确的是 A.  B. B.  C.  D. D.  |
|
| 19. 选择题 | 详细信息 |
|
用0.1 mol/L的Na2SO3溶液30 mL,恰好将2×10-3 mol XO4-还原,则元素X在还原产物中的化合价是( ) A.+4 B.+3 C.+2 D.+1 |
|
| 20. 选择题 | 详细信息 |
|
下列离子方程式书写正确的是( ) A.碳酸钙中加入盐酸:CO32-+2H+=H2O+CO2↑ B.铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ C.碳酸钠溶液中加入氢氧化铜:Cu2++CO32-=CuCO3↓ D.澄清石灰水中通入少量二氧化碳:Ca2++2OH-+CO2=CaCO3↓+H2O |
|
| 21. 选择题 | 详细信息 |
|
下列对于某些离子的检验及结论一定正确的是( ) A. 加入稀盐酸产生无色气体,原物质一定有CO32- B. 加入氯化钡溶液有白色沉淀产生,一定有SO42- C. 加入硝酸银溶液产生白色沉淀,则原溶液一定有Cl- D. 加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,不一定有Ba2+ |
|
| 22. 选择题 | 详细信息 |
|
下列事实与胶体性质无关的是( ) A.纳米科技的发展有赖于胶体化学原理与方法 B.硝酸银溶液中滴入氯化钠溶液出现沉淀 C.用一束平行光线照射豆浆时,可看到光亮的通路 D.长江入海口处形成沙洲 |
|
| 23. 选择题 | 详细信息 |
|
工业上冶炼锡的第一步反应原理为2SnO2 + 3C A. 反应中SnO2被还原 B. a的值为3 C. 反应后有两种氧化产物 D. 每生成1 mol CO2转移电子8 mol |
|
| 24. 选择题 | 详细信息 |
|
已知I-、Fe2+、SO2、Cl-和H2O2均有还原性,它们在酸性溶液中还原性的强弱顺序为 Cl-<Fe2+<H2O2<I-<SO2,则下列反应中不能发生的是 A. 2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ B. I2+SO2+2H2O=H2SO4+2HI C. H2O2+H2SO4=SO2↑+O2↑+2H2O D. 2Fe3++2I-=2Fe2++I2 |
|
| 25. 填空题 | 详细信息 |
|
请完成下列填空: (1)当SO2和SO3中分子个数比为1:1 时,原子总数之比为____,质量之比为____。 (2)将5mol/L的Mg(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO3-的物质的量浓度是______。 (3)中和含0.2molHCl的稀盐酸,需NaOH的物质的量为_______;如改用KOH,则所需KOH的质量为________。 |
|
| 26. 填空题 | 详细信息 |
|
3H2O2 + 2H2CrO4 =2 Cr(OH)3 + 3O2 ↑+ 2H2O (1)其中Cr被___________,H2O2作____________剂。 (2)_____________是氧化产物,_______________发生还原反应。 (3)反应转移了0.3mol电子,则产生的气体在标准状态下体积约为__________。 (4)用单线桥标明电子转移的方向和数目。_______ |
|
| 27. 推断题 | 详细信息 |
|
有一包白色粉末,其中可能含有Ba(NO3)2、MgCl2、K2CO3、NaOH,现做以下实验: ①取一定量粉末加入水中,振荡,有白色沉淀生成; ②向①的沉淀物中加入足量稀硝酸,白色沉淀完全消失,没有气泡产生; ③向①的上层清液中滴入稀硫酸,有白色沉淀产生。 根据上述实验事实,回答下列问题: (1)原白色粉末中一定含有的物质是________,一定不含有的物质是________。(写化学式) (2)写出各步变化的离子方程式 ①_______________________________________________________; ②_______________________________________________________; ③_______________________________________________________。 |
|
| 28. 实验题 | 详细信息 |
|
某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质。 (1)若将饱和FeCl3溶液分别滴入下列物质中,能形成胶体的是____。 A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液 (2)现有甲、乙、丙三名同学进行Fe(OH)3胶体的制备实验: ①甲同学的操作是:取一小烧杯,加入25 mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2 mL FeCl3饱和溶液,继续煮沸至混合液呈红褐色,停止加热。请评价该操作是否正确____。 ②乙同学直接加热饱和FeCl3溶液,请评价是否正确____。 ③丙同学向沸水中滴加饱和FeCl3溶液,为了使反应进行充分,煮沸10分钟,请评价是否正确__。 (3)写出制备Fe(OH)3胶体的化学方程式:_____。证明有Fe(OH)3胶体生成的实验操作是________。利用的胶体性质是___。 (4)Fe(OH)3胶体稳定存在的主要原因是___。 A.胶粒直径小于1 nm B.胶粒带正电荷 C.胶粒作布朗运动 D.胶粒能透过滤纸 |
|
| 29. 计算题 | 详细信息 |
|
某市售盐酸试剂瓶标签上的部分信息如下: 盐酸 分子式:HCl 相对分子质量:36.5 密度约1.18g•mL-1 HCl的质量分数:36.5% (1)该盐酸的物质的量浓度为_________ mol·L-1。 (2)取该盐酸50 mL加水稀释到500 mL,则稀释后溶液中c(HCl)=_____mol·L-1。 (3)取稀释后的适量盐酸与足量的锌粒作用,生成0.25 mol氢气,在标准状况下气体的体积____ L。 |
|
最近更新



