景谷一中2019年高二下册化学月考测验无纸试卷
| 1. 选择题 | 详细信息 |
|
下列关于能层与能级的说法中正确的是( ) A. 同一原子中,符号相同的能级,其上电子能量不一定相同 B. 任一能层的能级总是从s能级开始,而且能级数不一定等于该能层序数 C. 同是s能级,在不同的能层中所能容纳的最多电子数是不相同的 D. 多电子原子中,每个能层上电子的能量一定不同 |
|
| 2. 选择题 | 详细信息 |
|
生活中的下列现象与原子核外电子发生跃迁有关的是 A. 钢铁长期使用后生锈 B. 节日里燃放的焰火 C. 金属导线可以导电 D. 卫生丸久置后消失 |
|
| 3. 选择题 | 详细信息 |
|
下列表示钠原子的符号和图示中能反映能级差别和电子自旋状态的是( ) A. B. C. 1s22s22p63s1 D.  |
|
| 4. 选择题 | 详细信息 |
|
下列说法正确的是( ) A. 第三能层有s、p共两个能级 B. 3d能级最多容纳5个电子 C. 第三能层最多容纳8个电子 D. 无论哪一能层的s能级最多容纳的电子数均为2个 |
|
| 5. 选择题 | 详细信息 |
|
下列原子中未成对电子数最多的是( ) A. C B. N C. O D. Cl |
|
| 6. 选择题 | 详细信息 |
如图是元素周期表中短周期元素的一部分,其中电负性最小的元素是( ) 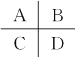 A. A B. B C. C D. D |
|
| 7. 选择题 | 详细信息 |
|
在下列所示的微粒中,氧化性最强的是 A.1s22s22p2 B.1s22s22p5 C.1s22s22p63s1 D.1s22s22p6 |
|
| 8. 选择题 | 详细信息 |
|
下列有关σ键和π键的说法正确的是( ) A. 单键既有σ键也有π键 B. 所有的π键都容易打开 C. σ键可沿键轴自由旋转而不影响键的强度 D. π键比σ键重叠程度大,形成的共价键强 |
|
| 9. 选择题 | 详细信息 |
|
4p轨道填充一半的元素,其原子序数是( ) A. 15 B. 33 C. 35 D. 51 |
|
| 10. 选择题 | 详细信息 |
|
基态硅原子的最外能层的各能级中,电子排布的方式正确的是( ) A. C. |
|
| 11. 选择题 | 详细信息 |
|
下列原子或离子原子核外电子排布不属于基态排布的是 A. Na: 1s22s22p53s2 B. S2-: 1s22s22p63s23p6 C. N: 1s22s22p3 D. Si: 1s22s22p63s23p2 |
|
| 12. 选择题 | 详细信息 |
|
下列微粒半径大小比较错误的是( )。 A. K>Na>Li B. Na+>Mg2+>Al3+ C. Mg2+>Na+>F- D. Cl->F->F |
|
| 13. 选择题 | 详细信息 |
|
下列说法错误的是 A. ns电子的能量不一定高于(n-1)p电子的能量 B. 6C的电子排布式1s22s22px2违反了洪特规则 C. 电子排布式(21Sc)1s22s22p63s23p63d3违反了能量最低原理 D. 电子排布式(22Ti)1s22s22p63s23p10违反了泡利原理 |
|
| 14. 选择题 | 详细信息 |
|
下列有关化学键类型的判断正确的是( ) A. 全部由非金属元素组成的化合物中肯定不存在离子键 B. 所有物质中都存在化学键 C. 已知乙炔的结构式为H—C≡C—H,则1个乙炔分子中存在2个σ键(C—H)和3个π键(C≡C) D. 乙烷分子中只存在σ键,即C—H键和C—C键都为σ键,不存在π键 |
|
| 15. 选择题 | 详细信息 | ||||||||||||
下表列出了某短周期元素R的各级电离能数据(用I1、I2……表示,单位为kJ·mol-1)。关于元素R的判断中一定正确的是( )
|
|||||||||||||
| 16. 选择题 | 详细信息 |
|
硒是人体必需的微量元素,它能有效提高人体免疫机能,抑制癌症和心脑血管等疾病的发病率。下列有关说法正确的是( ) A. 硒元素位于元素周期表中第15列 B. 硒元素原子的价电子排布式为4s24p4 C. 硒的氧化物只有一种 D. 基态原子核外电子排布中共有7个能级 |
|
| 17. 选择题 | 详细信息 |
|
现有四种元素的基态原子的电子排布式如下: ① 1s22s22p63s23p4 ②1s22s22p63s23p3 ③1s22s22p3 ④1s22s22p5 则下列有关比较中正确的是( ) A. 第一电离能:④>③>②>① B. 原子半径:④>③>②>① C. 电负性:④>③>②>① D. 最高正化合价:④>③=②>① |
|
| 18. 选择题 | 详细信息 |
|
若某元素原子处于能量最低状态时,价电子排布式为3d14s2,则下列说法正确的是( ) A. 该元素原子处于能量最低状态时,原子中共有3个未成对电子 B. 该元素原子最外层有3个电子 C. 该元素原子的M层共有8个电子 D. 该元素原子核外共有4个电子层 |
|
| 19. 选择题 | 详细信息 |
|
下列说法正确的是( ) A. 原子核外电子排布式为1s2的原子与核外电子排布式为1s22s2的原子化学性质相似 B. Fe3+的最外层电子排布式为3s23p63d5 C. 基态铜原子的最外层的电子排布图: D. 基态碳原子的最外层电子排布图: |
|
| 20. 选择题 | 详细信息 |
|
下列有关说法正确的是 A. C、N、O三种元素第一电离能从大到小的顺序是O>N>C B. 根据同周期元素的第一电离能变化趋势,推出Al的第一电离能比Mg大 C. 根据主族元素最高正化合价与族序数关系,推出卤族元素最高正价都是+7 D. Ni原子的核外电子排布式为1s22s22p63s23p63d84s2 |
|
| 21. 选择题 | 详细信息 |
|
某元素位于第三周期第ⅥA族。下列叙述不正确的是 A. 该元素是非金属元素 B. 该元素原子的核电荷数为16 C. 该元素原子核外有3个电子层 D. 该元素原子容易失去最外层电子 |
|
| 22. 选择题 | 详细信息 |
|
下列各组化合物中,化学健的类型完全相同的是 ①CaCl2 和Na2S ②Na2O 和Na2O2 ③CO2 和CS2 ④HCl 和NaOH A. ①② B. ②③ C. ①③ D. ②④ |
|
| 23. 填空题 | 详细信息 |
|
比较下列多电子原子的原子轨道的能量高低. (1)2s ________3s (2)2s ________3d (3)3d ________4s (4)4f ________6f (5)3px ________3pz (填“>”或“<”或“=”)。 |
|
| 24. 推断题 | 详细信息 | ||||||||||
J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如下表。J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素。
|
|||||||||||
| 25. 推断题 | 详细信息 |
|
有三种物质AC2(气体)、B2C2、AD4,元素A的最高正价和负价绝对值相等;元素B的单质能在C的气态单质中剧烈燃烧,火焰呈黄色,并生成淡黄色固体B2C2;元素D的负一价阴离子电子层结构与氩原子相同,则: (1)AC2、AD4的化学式分别为______、______。 (2)AD4分子其中含有的σ键类型为_______(填“s-s σ键”“s-p σ键”或“p-p σ键”)。 (3)D的负一价阴离子的电子排布式为_________,B2C2的电子式为__________,属___________(填“离子化合物”或“共价化合物”)。 (4)写出一种与AC互为等电子体的分子______________ |
|
| 26. 填空题 | 详细信息 |
|
根据元素周期表中完整周期元素的性质,完成下列空格。 (1)在第三周期中,第一电离能最小的元素符号是________,其原子的结构示意图为__________,第一电离能最大的元素符号是________,其价电子排布式为___________________________。 (2)在元素周期表中,电负性最大的元素名称是________,其价电子排布图为______________ (3)第四周期元素中未成对电子数最多的元素符号是________,其原子的简化电子排布式为__________,有_____个未成对电子,有_____个能级,能量最高的能级符号为_______。 (4)某元素的基态原子价电子排布式为3d104s1 ,该元素符号是_________,原子中所有电子占有________个轨道,核外共有________个不同运动状态的电子。 |
|
最近更新



