2016-2017年高一下半期化学开学考试(山东省济南市历城区第二中学)
| 1. | 详细信息 |
|
下列关于实验操作的叙述中正确的是( ) A.从试剂瓶中取出任何药品,若有剩余一定不能再放回原试剂瓶中 B.可燃性气体点燃之前必须验纯 C.用胶头滴管向试管中滴加液体,一定要将滴管伸入试管内 D.用温度计搅拌溶液一定要慢慢搅拌 |
|
| 2. | 详细信息 |
下列实验装置、选用的试剂或实验操作中,都正确的是( ) A.实验室用装置A制取氨气 B.用B装置吸收氨气,并防止倒吸 C.用C装置稀释浓硫酸 D.用D装置除去CO2中的HCl |
|
| 3. | 详细信息 |
|
下列括号中的分离方法运用得当的是( ) A.植物油和水(蒸馏) B.水溶液中的食盐和碘(分液) C.CaCO3和CaCl2(溶解、过滤、蒸发) D.自来水中的杂质(萃取) |
|
| 4. | 详细信息 |
|
将CO2通入下列物质的溶液中不与其反应的是( ) ①Na2CO3②Ca(ClO)2③CaCO3④CaCl2 . A.①③④ B.①和③ C.只有② D.只有④ |
|
| 5. | 详细信息 |
|
下列有关氮气的说法正确的是( ) A.氮气是由氮原子构成的双原子分子,所以化学性质不活泼 B.1 mol N2可与3 mol H2完全反应生成2 mol NH3 C.电闪雷鸣的雨天,雨水中会含有一定量的硝酸,其中发生的反应之一是N2+2O2 = 2NO2 D.NO、NO2在一定条件下可相互转化,且二者都是引起光化学烟雾的大气污染物 |
|
| 6. | 详细信息 |
|
下列离子方程式与所述事实相符且正确的是( ) A.实验室用MnO2和浓盐酸制取Cl2:MnO2+4HCl(浓) B.Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O C.向NaHSO4溶液中滴加Ba(OH)2溶液至呈中性:2H++SO42?+Ba2++2OH?=2H2O+BaSO4↓ D.向次氯酸钠溶液中通入SO2:2ClO?+SO2+H2O=SO32-+2HClO |
|
| 7. | 详细信息 |
|
同温同压下,在3支相同体积的试管中分别充有等体积混合的两种气体,它们是:①NO和NO2 , ②NO2和O2 , ③NH3和N2。现将3支试管均倒置于水槽中,充分反应后,试管中剩余气体的体积分别为V1、V2、V3 , 则下列关系正确的是( ) A.V1>V2>V3 B.V1>V3>V2 C.V2>V3>V1 D.V3>V1>V2 |
|
| 8. | 详细信息 |
|
Cu粉放入稀H2SO4中,加热后无现象,当加入一种盐后,Cu粉质量减少,而溶液变蓝,同时有气体生成,此盐是( ) A.氯化物 B.硫酸盐 C.硝酸盐 D.碳酸盐 |
|
| 9. | 详细信息 |
|
在某100 mL的混合液中,硝酸和硫酸的物质的量浓度分别是0.4 mol?L-1、0.1 mol?L-1,向该混合液中加入1.92 g铜粉,加热,待充分反应后,所得溶液中铜离子物质的量浓度( mol?L-1)是( ) A.0.15 B.0.225 C.0.35 D.0.45 |
|
| 10. | 详细信息 |
|
下列试剂的保存不用棕色瓶的是( ) A.浓硝酸 B.硝酸银 C.氯水 D.浓硫酸 |
|
| 11. | 详细信息 |
|
下列溶液中能大量共存的离子组是( ) A.H+、Fe2+、Cl-、NO3- B.NH4+、SO42-、Na+、OH- C.Cu2+、Fe3+、NO3-、Cl- D.H+、Na+、HCO3-、SO42- |
|
| 12. | 详细信息 |
|
氯气是一种重要的工业原料。工业上利用反应3Cl2+2NH3=N2+6HCl检查氯气管道是否漏气。下列说法错误的是( ) A.若管道漏气遇氨就会产生白烟 B.该反应利用了Cl2的强氧化性 C.该反应属于复分解反应 D.生成1 mol N2有6 mol电子转移 |
|
| 13. | 详细信息 |
|
下列有关厨房铝制品的使用中,你认为合理的是( ) A.盛放食醋 B.用碱液洗涤 C.烧制开水 D.用金属丝擦洗表面污垢 |
|
| 14. | 详细信息 |
|
在溶液中加入足量Na2O2后仍能大量共存的离子组是( ) A.K+、AlO2-、Cl-、SO42- B.H+、Ba2+、Cl-、NO- C.Ca2+、Fe2+、NO3?、HCO3- D.Na+、Cl-、CO32-、SO32- |
|
| 15. | 详细信息 |
|
下列溶液能既能用玻璃瓶盛放,又能用玻璃塞的是( ) A.HNO3溶液 B.HF溶液 C.Na2SiO3溶液 D.NaOH溶液 |
|
| 16. | 详细信息 |
|
将足量CO2气体通入硅酸钠溶液中,然后加热蒸干,再在高温下充分反应,最后所得的固体物质是( ) A.Na2SiO3 B.Na2CO3、Na2SiO3 C.Na2CO3、SiO2 D.SiO2 |
|
| 17. | 详细信息 |
|
将3.9 g镁铝合金投入到 500 mL 2 mol/L的盐酸中,金属完全溶解,再加入4mol/L的NaOH溶液,若要生成的沉淀最多,加入的这种NaOH溶液的体积为( ) A.125mL B.200mL C.250mL D.560mL |
|
| 18. | 详细信息 |
现有Al、Cl2、Al2O3、HCl(aq)、Al(OH)3、NaOH(aq)六种物质,它们之间有如图所示转化关系,图中每条线两端的物质之间都可以发生反应,下列推断不合理的是( ) A.N一定是HCl(aq) B.X可能为Al或Cl2 C.Y一定为NaOH(aq) D.Q、Z中的一种必定为Al2O3 |
|
| 19. | 详细信息 |
某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-、CO32-等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化的图像如图所示。下列说法正确的是( )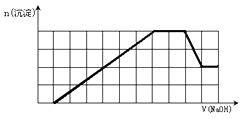 A.原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+ B.原溶液中一定含有SO42-和Na+ C.原溶液中含有的Fe3+和Al3+的物质的量之比为1:1 D.反应最后形成的溶液中含有的溶质为Na2SO4 |
|
| 20. | 详细信息 |
|
在含1 mol KAl(SO4)2的溶液中逐滴加入2 mol Ba(OH)2溶液,下列有关说法中正确的是( ) A.先生成沉淀,后沉淀全部溶解 B.当溶液中Ba2+全部沉淀出来时,沉淀的总物质的量最大 C.最后得到的沉淀是BaSO4 D.最后的沉淀为2 mol BaSO4、1 mol Al(OH)3 |
|
| 21. | 详细信息 |
|
在Al2(SO4)3、K2SO4和明矾的混合液中,如果SO42-的物质的量浓度为0.2 mol?L-1 , 当加入等体积的0.2 mol?L-1的KOH溶液时,生成的沉淀恰好溶解,则原混合物中K+的物质的量浓度是( ) A.0.2 mol?L-1 B.0.25 mol?L-1 C.0.225mol?L-1 D.0.45 mol?L-1 |
|
| 22. | 详细信息 |
|
为了检验某FeCl2溶液是否变质,可向溶液中加入( ) A.NaOH B.铁片 C.KSCN溶液 D.石蕊溶液 |
|
| 23. | 详细信息 |
|
把铁片放入下列溶液中,铁片溶解,溶液质量增加,但没有气体放出的是( ) A.稀硫酸 B.CuSO4溶液 C.Fe2(SO4)3溶液 D.AgNO3溶液 |
|
| 24. | 详细信息 |
|
下列不能由单质直接化合而成的物质是 ( ) A.FeCl2 B.CuCl2 C.AlCl3 D.NaCl |
|
| 25. | 详细信息 |
|
下列离子方程式正确的是 ( ) A.二氧化硅与强碱溶液反应: SiO2+2OH- = SiO32-+ H2O B.将氯气通入NaOH溶液中:Cl2 + OH-= Cl-+ HClO C.金属钠与水反应:Na+2H2O=Na+ + 2OH-+ H2↑ D.少量的金属锌加入到FeCl3溶液中: 2Fe3++3Zn = 2Fe+3Zn2+ |
|
| 26. | 详细信息 |
|
根据下列反应判断氧化剂的氧化性由强到弱的顺序正确的是 ( ) ① Cl2+2KI=I2+2KCl ② 2FeCl3+2HI=I2+2FeCl2+2HCl ③ 2FeCl2+Cl2=2FeCl3 ④ I2+SO2+2H2O=2HI+H2SO4 A.Cl2>I2>Fe3+>SO2 B.Cl2>Fe3+>I2>SO2 C.Fe3+>Cl2>I2>SO2 D.Cl2>Fe3+>SO2>I2 |
|
| 27. | 详细信息 |
|
往盛氯水的试管里滴入少量紫色石蕊试液,观察到的现象是 ( ) A.紫色石蕊试液显蓝色 B.紫色石蕊试液显红色 C.紫色石蕊试液的颜色消失 D.紫色石蕊试液先显红色,后红色消失 |
|
| 28. | 详细信息 |
|
为了防止FeSO4被氧化而变质,实验室在配制FeSO4溶液时,常在溶液中加入少量的( ) A.铜粉 B.铁粉 C.锌粉 D.Fe2(SO4) |
|
| 29. | 详细信息 |
|
对于溶液中某些离子的检验及结论一定正确的是( ) A.加入稀盐酸产生无色气体,将气体通入澄清石灰水,溶液变浑浊,一定有CO32- B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- C.加入足量稀盐酸,再加入氯化钡溶液后有白色沉淀产生,一定有SO42- D.加入碳酸钠溶液产生白色沉淀,再加盐酸沉淀消失,一定有Ba2+ |
|
| 30. | 详细信息 |
|
已知5KCl+KClO3+3H2SO4=3Cl2↑+3K2SO4+3H2O,下列说法不正确的是( ) A.KClO3是氧化剂 B.被氧化与被还原的氯元素的质量比为5:1 C.H2SO4既不是氧化剂又不是还原剂 D.1mol KClO3参加反应时有10mol电子转移 |
|
最近更新



