2017-2018年高二上册期中考试化学在线测验(河北省衡水市安平中学)
| 1. | 详细信息 |
|
下列物质中,属于强电解质的是 A. |
|
| 2. | 详细信息 |
|
下列电离方程式书写正确的是 A. CH3COOH B. NaHSO4 C. H2CO3 D. NaHCO3 |
|
| 3. | 详细信息 |
|
常温下,下列离子能使纯水中的H+离子数目增加的是 A. S2- B. CO32- C. NH4+ D. Br- |
|
| 4. | 详细信息 |
|
下列水解化学方程式或水解离子方程式正确的是: ( ) A. CH3COO? + H2O C. CH3COOH + NaOH |
|
| 5. | 详细信息 |
|
用铂电极电解下列溶液时,阴极和阳极上的主要产物分别为H2和O2的是 ( ) A. 稀HCl溶液 B. 稀Na2SO4溶液 C. CuCl2溶液 D. AgNO3溶液 |
|
| 6. | 详细信息 |
|
将氨水缓缓地滴入盐酸中至中性,下列有关的说法:①盐酸过量 ②氨水过量 ③恰好完全反应 ④c(NH4+)=c(Cl-) ⑤c(NH4+)<c(Cl-)正确的是( ) A. ①⑤ B. ③④ C. ②⑤ D. ②④ |
|
| 7. | 详细信息 |
|
随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程,其首要原因是 A. 利用电池外壳的金属材料 B. 防止电池中汞、镉和铅等重金属离子对土壤和水源的污染 C. 不使电池中渗泄的电解液腐蚀其他物品 D. 回收其中石墨电极 |
|
| 8. | 详细信息 |
|
相同温度下等物质的量浓度的下列溶液中,pH值最小的是 A. |
|
| 9. | 详细信息 |
|
使10 mL浓度为1 mol/L的盐酸与过量的锌粉反应,若加入适量的下列溶液,能减慢反应速率但又不影响氢气生成的量的是 A. KNO3 B. CH3COONa C. CuSO4 D. Na2CO3 |
|
| 10. | 详细信息 |
|
已知蓄电池在充电时作电解池,放电时作原电池。铅蓄电池上有两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“?”。关于标有“+”的接线柱,下列说法中正确的是 A. 充电时作阳极,放电时作正极 B. 充电时作阳极,放电时作负极 C. 充电时作阴极,放电时作负极 D. 充电时作阴极,放电时作正极 |
|
| 11. | 详细信息 |
下列各个装置中能组成原电池的是( ) A. A B. B C. C D. D |
|
| 12. | 详细信息 |
|
某原电池总反应的离子方程式为:2Fe3++Fe=3 Fe2+,能实现该反应的原电池是 A. 正极为铜,负极为铁,电解质溶液为FeCl2溶液 B. 正极为C,负极为铁,电解质溶液为Fe(NO3)3溶液 C. 正极为铁,负极为锌,电解质溶液为Fe2(SO4)3 D. 正极为银,负极为铁,电解质溶液为CuSO4溶液 |
|
| 13. | 详细信息 |
依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池 如图所示。下列说法正确的是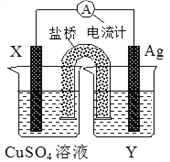 A. 银电极为负极 B. X电极是锌电极 C. 去掉盐桥电流计指针仍偏转 D. Y溶液为AgNO3溶液 |
|
| 14. | 详细信息 |
右图装置中发生反应的离子方程式为:Zn+2H+=Zn2++H2↑。下列说法错误的是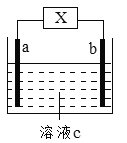 A. a、b不可能是同种材料的电极 B. X为电流计,c为稀盐酸,该装置为原电池 C. X为直流电源,c为稀硫酸,该装置为电解池 D. X为电流计,c为稀硫酸,a可能为铜电极,b可能为锌电极 |
|
| 15. | 详细信息 |
|
25℃时,水的电离达到平衡:H2O?H++OH?;△H>0,下列叙述正确的是 A. 将纯水加热到95℃,KW变大,PH不变,水仍呈中性 B. 向纯水中加入稀氨水,平衡逆向移动,c(OH?)降低 C. 向纯水中加入少量固体硫酸氢钠,c(H+)增 大,KW不变,影响水的电离平衡 D. 向纯水中加入醋酸钠或盐酸,均可抑制水的电离,KW不变 |
|
| 16. | 详细信息 |
|
把Ca(OH)2固体放入一定量的蒸馏水中,一定温度下达到平衡:Ca(OH)2(s) A. 溶液中Ca2+数目增多 B. 溶液中c(Ca2+)增大 C. 溶液pH值不变 D. 溶液pH值增大 |
|
| 17. | 详细信息 |
锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是(? )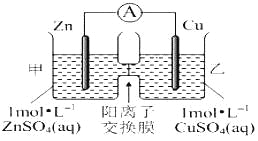 A. 铜电极上发生氧化反应 B. 电池工作一段时间后,甲池的C(SO42-)减小 C. 电池工作一段时间后,乙池溶液的总质量增加 D. 阳离子通过交换膜向正极移动,阴离子通过交换膜向负极移动,保持溶液中电荷平衡 |
|
| 18. | 详细信息 |
|
25℃时,在10mL浓度均为0.1mol/LNaOH和NH3?H2O混合溶液中,滴加0.1mol/L的盐酸,下列有关溶液中粒子浓度关系正确的是( ) A. 未加盐酸时:c(OH-)>c(Na+)= c(NH3?H2O) B. 加入10mL盐酸时:c(NH4+)+c(H+)=c(OH-) C. 加入盐酸至溶液pH=7时:c(Cl-) = c(Na+) D. 加入20mL盐酸时:c(Cl-)=c(NH4+)+c(Na+) |
|
| 19. | 详细信息 |
|
在25℃时,用蒸馏水稀释1 mol/L的醋酸溶液至0.01 mol/L,随着溶液的稀释,下列各项中始终保持增大的是 A. C. |
|
| 20. | 详细信息 |
用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定)。欲使溶液恢复到起始状态,可向溶液中加入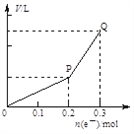 A. 0.1 mol CuO B. 0.05 mol Cu2(OH)2CO3 C. 0.1 mol Cu(OH)2 D. 0.1 mol CuCO3 |
|
| 21. | 详细信息 |
|
Mg-AgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式:2AgCl+ Mg = Mg2++ 2Ag+2Cl-。有关该电池的说法正确的是( ) A. Mg为电池的正极 B. 负极反应为AgCl+e-=Ag+Cl- C. 不能被KCl溶液激活 D. 可用于海上应急照明供电 |
|
| 22. | 详细信息 |
|
已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16,Ksp(Ag2CrO4)=2.0×10-12,则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是( ) A. AgCl>AgI>Ag2CrO4 B. AgCl>Ag2CrO4>AgI C. Ag2CrO4>AgCl>AgI D. Ag2CrO4>AgI>AgCl |
|
| 23. | 详细信息 |
|
(1)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈_______(填“酸性”,“中性”或“碱性”,下同),溶液中c(Na+) _______c(CH3COO-)(填“ >”或“=”或“<” )。 (2)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈__________,溶液中c(Na+) ___________c(CH3COO-) (填“ >” 或“=”或“<” ) (3)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈________. |
|
| 24. | 详细信息 |
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液。某研究小组将甲烷燃料电池作为电源,进行饱和氯化钠溶液电解实验,如图所示。回答下列问题: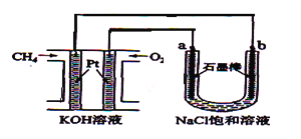 (1)甲烷燃料电池负极的电极反应为:____________________________。 (2)b电极上得到的气体是_______,电解氯化钠溶液的总反应方程式为 _____。 (3)若甲烷通入量为1 L(标准状况),且反应完全,则最多能产生的氯气体积为______L(标准状况)。 (4)以甲醇(CH3OH)为燃料的电池中,电解质溶液为碱性,则负极的电极反应为:负极_______________。 |
|
| 25. | 详细信息 |
某课外活动小组用如图装置进行实验,试回答下列问题: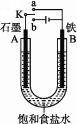 (1)若开始时开关K与a连接,则B极的电极反应为____________________。 (2)若开始时开关K与b连接,则B极的电极反应为____________________,总反应的离子方程式为____________________。 (3)有关上述实验,下列说法正确的是______。 A.溶液中Na+向A极移动 B.从A极处逸出的气体能使湿润的KI淀粉试纸变蓝 C.反应一段时间后加适量盐酸可恢复到电解前电解质的浓度 D.若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子 (4)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。  ①该电解槽的阳极反应为______________。 此时通过阴离子交换膜的离子数_____(填“大于”“小于”或“等于”)通过阳离子交换膜的离子数。 ②制得的氢氧化钾溶液从出口(填“A”、“B”、“C”或 “D”)________导出。 ③电解过程中阴极区碱性明显增强,用平衡移动原理解释原因__________________________。 |
|
| 26. | 详细信息 | ||||||||||
下表是25 ℃时某些弱酸的电离平衡常数。
|
|||||||||||
最近更新



