南菁高级中学高一化学2018年上学期期末考试试卷带答案和解析
| 1. | 详细信息 |
|
我国清代《本草纲目拾遗》中记叙无机药物335种,其中“强水”条目下写道:“性最烈,能蚀五金……其水甚强,五金八石皆能穿第,惟玻璃可盛。”这里的“强水”是指 A. 氨水 B. 硝酸 C. 醋 D. 卤水 |
|
| 2. | 详细信息 |
|
下列有关化学用语表示正确的是 A. 过氧化钠的电子式: B. 质子数为35、中子数为45的溴原子: C. 硫离子的结构示意图: D. H2O2的电子式: |
|
| 3. | 详细信息 | ||||||||||||||||||||||||||||||
下列关于物质的分类中,正确的是
|
|||||||||||||||||||||||||||||||
| 4. | 详细信息 |
如图所示,A处通入干燥Cl2,关闭B阀时,C处的红色布条看不到明显现象,打开B阀后,C处红色布条逐渐褪色,则D瓶中装的是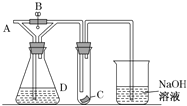 A. 浓H2SO4 B. NaOH溶液 C. 浓盐酸 D. 饱和NaCl溶液 |
|
| 5. | 详细信息 | |||||||||||||||||||||
将足量X气体通入Y溶液中,实验结果与预测的现象一致的组合是
|
||||||||||||||||||||||
| 6. | 详细信息 |
|
下列关于硅单质及其化合物的说法正确的是 ①硅是构成一些岩石和矿物的基本元素 ②水泥、玻璃、陶瓷都是硅酸盐产品 ③高纯度的硅单质广泛用于制作光导纤维 ④普通玻璃是氧化物,成分可表示为SiO2 ⑤粗硅制备单晶硅不涉及氧化还原反应 A. ①② B. ①②③ C. ①②③④ D. ②③④⑤ |
|
| 7. | 详细信息 |
|
将含有等体积NH3、CO2、NO的混合气体依次通过盛有H2SO4、Na2O2和Na2CO3溶液的装置,充分作用后,最后得到的气体是 A. CO2,NO B. NO,NH3 C. CO,O2 D. NO2,CO2 |
|
| 8. | 详细信息 |
|
A、B是短周期元素,最外层电子排布式分别为3s2,2s22p3。A与B形成的离子化合物加蒸馏水溶解后可使酚酞试液变红,同时有气体逸出,该气体可使湿润的红色石蕊试纸变蓝,则该化合物的分子量是 A. 38 B. 55 C. 100 D. 135 |
|
| 9. | 详细信息 |
|
下列各组离子中,在溶液中能大量共存的是( ) A. H+,OH-,Na+,SO42- B. Fe3+,Cl-,K+,I- C. Cu2+,NO3-,Na+,Cl- D. Ba2+,Cl-,K+,CO32- |
|
| 10. | 详细信息 |
下图所示的实验装置图正确且能达到相应实验目的的是 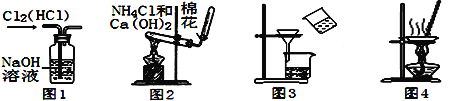 A. 用图1所示装置除去Cl2中的HCl B. 用图2所示装置实验室制NH3 C. 用图3所示装置分离MnO2和KCl D. 用图4所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
|
| 11. | 详细信息 |
|
下列离子方程式中正确的是 A. Na2O2 溶于水:Na2O2+H2O ==2Na++2OH-+O2↑ B. 向氧化铁中加入氢碘酸发生反应: Fe2O3+6HI == 2Fe2++I2 +3H2O +4I- C. 氯化铝溶液中加入过量氨水:Al3++4NH3·H2O == AlO D. 漂白粉溶液中通入过量的CO2:ClO- +CO2+H2O == HClO+HCO3- |
|
| 12. | 详细信息 | ||||||||||||||||||||||||||
下列各组物质中,满足表中图示物质在通常条件下能一步转化的全部组合是
|
|||||||||||||||||||||||||||
| 13. | 详细信息 |
|
下列氧化还原反应中,实际参加反应的氧化剂与还原剂的物质的量之比正确 ①KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O;1∶6 ②Fe2O3+2Al ③SiO2+3C ④3NO2+H2O===2HNO3+NO;2∶1 A. ①③ B. ②③ C. ②④ D. ①④ |
|
| 14. | 详细信息 |
|
CuSO4溶液中加入过量KI溶液,产生白色CuI沉淀,溶液变棕色。向反应后溶液中通入过量SO2,溶液变成无色。下列说法不正确的是 A. 滴加KI溶液时,KI被氧化,CuI是还原产物 B. 通入SO2后,溶液变无色,体现SO2的还原性 C. 整个过程发生了复分解反应和氧化还原反应 D. 上述实验条件下,物质的氧化性:Cu2+>I2>SO2 |
|
| 15. | 详细信息 |
|
在一定温度下,某浓度的硝酸与金属锌反应,生成NO2和NO的物质的量之比为1︰3。则要使1mol金属锌完全反应,需要HNO3的物质的量为 A. 0.8 B. 2.4 C. 2.6 D. 2.8 |
|
| 16. | 详细信息 |
|
在某100mL混合酸中,HNO3物质的量浓度为0.4mol/L,H2SO4物质的量浓度为0.2mol/L。向其中加入1.92g铜粉微热,待充分反应后,溶液中Cu2+物质的量浓度约为 A. 0.15mol/L B. 0.3mol/L C. 0.225mol/L D. 无法计算 |
|
| 17. | 详细信息 |
|
a升CO2气体通过足量Na2O2所得的气体与b升NO相混和时,可得到c升气体(相同状况),以下表达式中错误的是( ) A. 若a<b,则c>0.5(a+b) B. 若a>b,则c=0.5(a+b) C. 若a=b,则c=0.5(a+b) D. 若a<b,则c<0.5(a+b) |
|
| 18. | 详细信息 |
|
3.84g铜投入一定量浓HNO3中,铜完全溶解,生成气体颜色越来越浅,共收集到1344mL气体(标况)。将盛有此气体的容器倒扣在水中,通入标况下一定体积的O2,恰好使气体完全溶于水中,则通入O2的体积 A. 672mL B. 168mL C. 504mL D. 336mL |
|
| 19. | 详细信息 |
A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系: (1)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。写出②反应的离子方程式_________;④反应离子方程式__________。 (2)若A是应用最广泛的金属。④反应用到A,②⑤反应均用到同一种黄绿色气体单质。写出A与水高温下反应的化学方程式_______________________。④反应的离子方程式______________。D中加入氢氧化钠的现象__________。 (3)若A是太阳能电池用的光伏材料,B常用用于制作高档光学器材,C、D为钠盐,C的水溶液俗称泡花碱,D的溶液显碱性。④反应也是通入一种引起温室效应的主要气体。写出③反应的化学方程式________________________。⑤反应用到B,反应条件为高温,则⑤的化学方程式为____________________。 |
|
| 20. | 详细信息 |
|
已知X、Y、Z、W、L为五种短周期元素,非金属元素X最外层电子数与其周期序数相同,Y的最外层电子数是其所在周期数的2倍。Y在Z中充分燃烧能生成其最高价化合物YZ2。W+与Z2-具有相同的电子数。X在L中燃烧,产物XL溶于水得到一种强酸。请回答下列问题: (1)X在周期表中的位置是_____。请写出实验室制备单质L的化学方程式______,尾气处理的离子方程式____________。 (2)由X分别与Y、Z形成的最简单化合物的稳定性关系为___________________。 (3)由X、Y、Z、W组成的一种盐,在面食中有大量使用,在其水溶液中滴入由X、Y、Z形成的厨房中常见的一种酸,反应的离子方程式为______________。 |
|
| 21. | 详细信息 |
|
某汽车安全气囊的产气药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质。当汽车发生碰撞时,产气药剂产生大量气体使气囊迅速膨胀,从而起到保护作用。 (1)NaN3是气体发生剂,受热分解产生N2和Na,N2的电子式为____________。 (2)Fe2O3是主氧化剂,与Na反应生成的还原产物为_________________(已知该反应为置换反应),铁的外围电子排布式为_______________________: (3)KClO4是助氧化剂,反应过程中与Na作用生成KCl和Na2O。KClO4含有化学键的类型为______,K的原子结构示意图为_______________________。 (4)NaHCO3是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为______。 |
|
| 22. | 详细信息 |
|
为了测定某铜银合金的组成,将30.0g合金溶于80.0mL 13.5mol·L−1的浓HNO3中。待合金完全溶解后,收集到气体6.72L(标准状况下)并测得H+浓度为1mol·L−1。假设反应后溶液的体积为80.0mL,试计算: (1)被还原的硝酸的物质的量___________; (2)合金中银的质量分数___________。 (3)确定6.72L气体中各成分的物质的量___________。 |
|
| 23. | 详细信息 |
|
已知NH3和Cl2混合发生下列反应: 氨气少量时:①2NH3+3Cl2=N2+6HCl 氨气过量时:②8NH3+3Cl2=N2+6NH4Cl 现有Cl2和NH3共amol,混和后充分反应,气体物质的量变为bmol,问被氧化的NH3物质的量是多少? |
|
| 24. | 详细信息 |
| 一定量的浓硝酸与足量的铜反应(后期加热),得到对氢气的相对密度为28的混和气体,该气体通过水后,体积缩小了1/3,则混和气体中含NO2的体积百分含量为多少? | |
最近更新