2018届高三上学期第一次调研考试理综化学(广州市)
| 1. | 详细信息 |
|
《汉书》记载“高奴县有洧水可燃”,《梦溪笔谈》描述“洧水”是“予知其烟可用,试扫其烟为墨,黑光如漆,松墨不及也,此物必大行于世”。这里的“洧水”和“烟”是指 A. 汽油和炭黑 B. 石油和炭黑 C. 煤油和石墨 D. 油脂和焦炭 |
|
| 2. | 详细信息 |
|
设NA为阿伏加德罗常数的值。下列有关叙述正确的是 A. 28 g乙烯和环丙烷混合气体中的氢原子数为4NA B. 25℃时,pH=1的H3PO4溶液中含有H+的数目为0.1NA C. 3 mol H2与1 mol N2于密闭容器中充分反应后,其分子总数为4NA D. 标准状况下,2.24 L苯在O2中完全燃烧得到CO2分子数为0.6NA |
|
| 3. | 详细信息 |
|
通过不同的水处理方法可以得到不同质量标准的水,以满足人民生产、生活的用水需要。下列处理方法不正确的是 A. 用ClO2、O3代替氯气进行自来水消毒 B. 用高铁酸钠(Na2FeO4)处理水中的微生物和细菌 C. 用Na2SO4?10H2O等处理含有Mg2+、Ca2+的硬水 D. 用Na2S处理工业废水中的Cu2+、Hg2+等重金属离子 |
|
| 4. | 详细信息 |
|
W、X、Y、Z为四种短周期主族元素,在光照条件下W的简单氢化物与氯气反应生成油状液体,X的气态氢化物的水溶液呈碱性,Y原子半径是短周期主族元素原子中最大的,Z2-的电子层结构与氩相同。下列说法正确的是 A. 简单氢化物沸点:W>X B. 简单离子半径:Z >X>Y C. 工业上常用电解熔融Y的氧化物制取Y的单质 D. Y与Z形成化合物的水溶液可使蓝色石蕊试纸变红 |
|
| 5. | 详细信息 | ||||||||||||||||||||
将SO2分别通入四种不同溶液,对应的现象及结论都正确且两者具有因果关系的是
|
|||||||||||||||||||||
| 6. | 详细信息 |
三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,甲、乙均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。下列叙述正确的是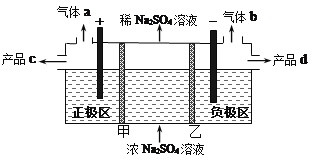 A. 甲为阳离子交换膜,通电后中间隔室的Na+离子向正极迁移 B. 通电后,同温同压下得到的气体a与气体b的体积比约为2:1 C. 通电后,得到的产品c是NaOH,产品d是H2SO4 D. 负极区发生的电极反应为2H2O +2e-=2OH-+H2↑,负极区溶液pH增大 |
|
| 7. | 详细信息 |
常温下,浓度均为0.10mol?L-1、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随lg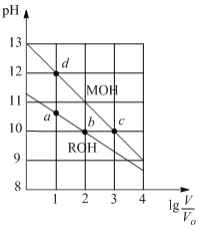 A. MOH的电离程度:c点大于d点 B. ROH溶液由a点到b点时, 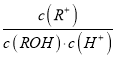 变大 变大C. pH=10时,MOH和ROH溶液中,c(M+)>c(R+) D. lg |
|
| 8. | 详细信息 |
|
水合草酸亚铁(FeC2O4?xH2O)是生产锂电池的原料,难溶于水,受热易分解。某化学兴趣小组对草酸亚铁的一些性质进行探究。回答下列问题: (1)实验室用硫酸亚铁溶液和草酸制备水合草酸亚铁,反应的化学方程式是_________。 (2)将水合草酸亚铁溶于适量盐酸。分别取2 mL此溶液于3支试管中,进行实验: ①第一支试管中加入几滴KSCN溶液,溶液不变红; ②第二支试管中加入几滴K3[Fe(CN)6]溶液,生成蓝色沉淀; ③第三支试管中加入几滴酸性KMnO4溶液,溶液紫红色褪去。 上述实验能证明水合草酸亚铁中存在Fe2+的是_________(填编号)。 (3)为测定水合草酸亚铁中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1 g。将样品装入石英玻璃管中,再次将装置A称重,记为m2 g。按下图连接好装置进行实验。  验步骤如下:a.打开K1和K2,缓缓通入N2;b.加热装置A一段时间;c.停止加热,冷却到室温;d.关闭K1和K2,称量A;e.重复上述步骤,直至A恒重,记为m3 g。 ①步骤b至步骤c继续通入N2的目的是 ________________。 ②根据实验数据记录,计算水合草酸亚铁化学式中结晶水数目x=______(列式表示)。 (4)为探究草酸亚铁的分解产物,将(3)中已恒重的装置A接入下图所示部分的装置(可重复选用)进行实验。打开K1和K2,缓缓通入N2,充分加热。实验后石英玻璃管中固体仅残留一种有磁性的黑色化合物。  ①写出草酸亚铁受热分解的化学方程式____________。 ②实验装置中,依次连接的合理顺序为A、____________。 |
|
| 9. | 详细信息 |
“一酸两浸,两碱联合”法是实现粉煤灰(含SiO2、Al2O3、Fe2O3、CaO、MgO等)综合利用的新工艺。工业流程如下: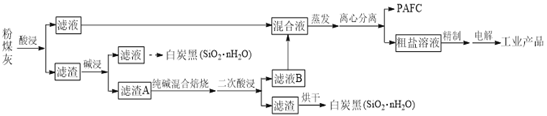 回答下列问题: (1)聚合氯化铝铁(PAFC)化学式为[Al2(OH)nCl6-n]m?[Fe2(OH)xCl6-x]y,是一种新型高效的净水剂,PAFC中铁元素的化合价为___________。 (2)“一酸两浸”中的酸是________________(填化学式)。? (3)实际工业中“酸浸”、“碱浸”均不能充分反应,滤渣A中主要含有SiO2、Al2O3。“纯碱混合焙烧”中,它们分别发生反应的化学方程式为__________、________。 (4)“滤液B”的主要溶质有_________(填化学式)。滤液混合后“蒸发”的作用是__________________。 (5)“电解”时阳极的电极反应式为_______________。 (6)PAFC、无水AlCl3、FeCl3?6H2O用量均为25 mg? 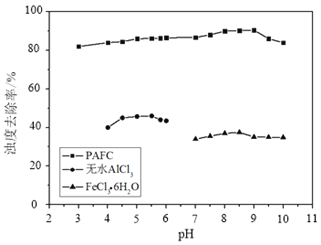 |
|
| 10. | 详细信息 |
|
氯化亚铜(CuCl)难溶于水,常用作催化剂、气体吸收剂及脱氯剂等。 (1)向一定比例的CuSO4、NaCl溶液中持续加入一定浓度的Na2SO3溶液可制得CuCl。加入的Na2SO3溶液体积与溶液pH关系如图所示。 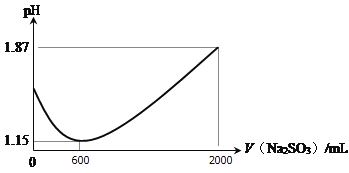 ① 0 ~ 600 mL时pH降低的原因是________________________(用离子方程式表示); ② 600 ~ 2000 mL的过程中有刺激性气味的气体产生,该气体是__________。 (2)CuCl的另一种制备原理是Cu2++Cu+2Cl-=2CuCl? K=5.85×106,向0.01 mol?L-1的CuCl2溶液中加入足量的铜,___(填“能”或“不能”)生成CuCl,写出计算过程_____。 (3)使用CuCl捕捉CO气体的反应为CuCl(s)+xCO(g) A.降低温度 B.增大压强 C.延长反应时间 D.把CuCl分散到疏松多孔的分子筛中 (4)已知: CuCl ①反应Cu++2Cl- ②用平衡移动原理解释CuCl易溶于浓盐酸的原因_____________________________。 |
|
| 11. | 详细信息 |
|
铬、钛及其化合物在工业上有重要用途,回答下列问题: (1)Cr基态原子价层电子的轨道表达式(电子排布图)为_________________________。 (2)氮化铬(CrN)在超级电容器领域具有良好的应用前景,可由CrCl3?6H2O与尿素[(NH2)2CO]反应先得到配合物Cr[OC(NH2)2]6Cl3,然后在通有NH3和N2混合气体的反应炉内热分解制得。尿素构成元素中电负性由大到小的顺序为_________,中心碳原子的杂化类型为_________;Cr[OC(NH2)2]6Cl3含有的化学键类型有__________________。 (3)氮化铬的晶体结构类型与氯化钠的相同,氮化铬熔点(1282℃)比氯化钠的高,主要原因是_________________________________________。 (4)钙钛矿(CaTiO3)型的结构可看作氧化物超导相结构的基本单元。 ①图A为立方钙钛矿(CaTiO3)结构的晶胞,晶胞边长为a nm。Ca处于晶胞的顶点,则Ti处于_________位置,O处于_________位置;与Ca紧邻的O个数为_________,Ti与O间的最短距离为____________________nm 。 ②在图B中画出立方钙钛矿晶胞结构的另一种表示(要求:Ti处于晶胞的顶点;  |
|
| 12. | 详细信息 |
科学家模拟足贝类足丝蛋白的功能,合成了一种对云母、玻璃、二氧化硅等材料具有良好粘附性的物质──化合物I,其合成路线如下: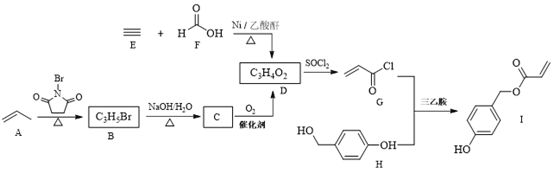 回答下列问题: (1)A的化学名称为___________________。 (2)由B生成C的化学方程式为_______________________________________________。 (3)由E和F反应生成D的反应类型为________________,由G和H反应生成I的反应类型为________________。 (4)D的结构简式为__________,仅以D为单体合成高分子化合物的化学方程式为___________________________________________________________。 (5)I的分子式为_____________________。 (6)X是I的同分异构体,能发生银镜反应,能与饱和碳酸氢钠溶液反应放出CO2,其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6:2:1:1。写出两种符合要求的X的结构简式___________________________________________。 |
|
最近更新



