高中化学人教版 必修1 第一章 从实验学化学 1.化学实验基本方法 混合物的分离和提纯
| 1. 选择题 | 详细信息 |
|
“粗盐提纯”实验中,下列操作正确的是(? ) A.过滤时用玻璃棒搅拌漏斗内的液体,以加速过滤 B.蒸发到析出晶体时才需要用玻璃棒搅拌 C.待溶液蒸干后即停止加热 D.当蒸发皿中出现较多量晶体时就应停止加热 |
|
| 2. 选择题 | 详细信息 |
|
进行过滤操作应选用的一组仪器是(? ) A.滤纸、烧杯、试管夹、漏斗、玻璃棒 B.烧杯、酒精灯、试管、漏斗 C.铁架台(附铁圈)、烧杯、漏斗、玻璃棒、滤纸 D.铁架台(附铁圈)、烧杯、漏斗、玻璃棒 |
|
| 3. 选择题 | 详细信息 |
|
下列叙述中,错误的是(? ) A.沙里淘金是利用金与沙的密度相差较大而将沙淘走,使金留下 B.化学上所指的杂质,有的本来无害且很有价值,即使有害无价值的也应设法变废为宝 C.检验某溶液时,将检测试剂一次加入全部溶液里 D.蒸发时加热到蒸发皿出现较多固体时即可 |
|
| 4. 选择题 | 详细信息 |
|
下列有关过滤和蒸发的操作中,正确的是(? ) A.过滤时,漏斗的下端管口紧靠烧杯内壁 B.为了加快过滤速度,可用玻璃棒搅动过滤器中的液体 C.当蒸发皿中的固体完全蒸干后,再停止加热 D.实验完毕后,用手直接取走蒸发皿 |
|
| 5. 选择题 | 详细信息 |
|
通过溶解、过滤、蒸发等操作,可将下列各组混合物分离的是(? ) A.硝酸钠、氢氧化钠 B.氧化铜、二氧化锰 C.氯化钾、二氧化锰 D.硫酸铜、氢氧化钙 |
|
| 6. 选择题 | 详细信息 |
|
分离下列混合物不能用过滤方法的是(? ) A.硫酸铜溶液与氢氧化钠溶液反应的生成物 B.铁粉和铜粉跟稀硫酸反应后的生成物 C.氢氧化钠溶液和盐酸反应后的生成物 D.用氯酸钾和二氧化锰的混合物加热制氧气后的剩余物质 |
|
| 7. 选择题 | 详细信息 |
|
欲除去下列物质中的杂质(括号内物质为杂质),所用试剂不正确的是(? ) A.KNO3溶液(K2SO4):适量Ba(NO3)2溶液 B.CaCO3粉末(CaCl2):过量盐酸 C.Cu粉(Zn粉):过量盐酸 D.CO2(O2):灼热的铜网 |
|
| 8. 选择题 | 详细信息 |
|
某固体NaOH因吸收了空气中的CO2而含有杂质,现在要将该固体NaOH配制成较纯的溶液,则其主要的实验操作过程应是(? ) A.溶解、加适量BaCl2溶液、过滤 B.溶解、加适量CaCl2溶液、过滤 C.溶解、加适量Ca(OH)2溶液、过滤 D.溶解、加适量盐酸、加热 |
|
| 9. 选择题 | 详细信息 |
某学生发现滴瓶中的溶液有悬浮物,拟用如图所示操作进行过滤,操作上错误的地方有(? ) A.4处 B.3处 C.2处 D.1处 |
|
| 10. 选择题 | 详细信息 |
|
下列说法不正确的是(? ) A.检验Cl-的试剂是硝酸银和硝酸 B.检验SO42-的试剂是氯化钡和盐酸 C.检验CO32-的试剂是盐酸、澄清石灰水和氯化钙 D.向溶液中加入BaCl2溶液后生成白色沉淀,即可证明有SO42- |
|
| 11. 选择题 | 详细信息 |
|
下列离子检验的方法正确的是(? ) A.某溶液中加硝酸银溶液生成白色沉淀,说明原溶液中有Cl- B.某溶液中加BaCl2溶液生成白色沉淀,说明原溶液中有SO42- C.某溶液中加NaOH溶液生成蓝色沉淀,说明原溶液中有Cu2+ D.某溶液加稀硫酸生成白色沉淀,说明原溶液中有Ba2+ |
|
| 12. 选择题 | 详细信息 |
|
下列的分离方法不正确的是(? ) A. 用过滤的方法除去食盐水中的泥沙 B. 用蒸馏的方法将自来水制成蒸馏水 C. 用酒精萃取碘水中的碘 D. 用分液的方法除去四氯化碳中的水 |
|
| 13. 选择题 | 详细信息 |
|
(双选)下列混合物的分离和提纯方法中,主要是从溶解性的角度考虑的是(? ) A. 蒸发 B. 蒸馏 C. 过滤 D. 萃取 |
|
| 14. 选择题 | 详细信息 |
|
为确定某溶液的离子组成,进行如下实验: ①取少量溶液滴加Ba(NO3)2溶液,产生白色沉淀 ②然后继续加入稀盐酸至溶液呈酸性,产生无刺激性气味且能使澄清石灰水变浑浊的气体;白色沉淀部分溶解 ③取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加AgNO3溶液,产生白色沉淀 根据实验,以下推测不正确的是(? ) A.一定有SO42- B.一定有CO32- C.不能确定Cl-是否存在 D.不能确定SO42-是否存在 |
|
| 15. 选择题 | 详细信息 |
下列图示的四种实验操作名称从左到右依次是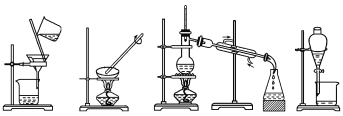 A.过滤、蒸发、蒸馏、分液 B.过滤、蒸馏、蒸发、分液 C.蒸发、蒸馏、过滤、分液 D.分液、蒸馏、蒸发、过滤 |
|
| 16. 选择题 | 详细信息 |
|
(2017?山东省寿光现代中学高一下学期第三学段质量监测)下列实验操作,正确的是 A. 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 B. 用蒸发的方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液全部加热蒸干 C. 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 D. 用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中 |
|
| 17. 选择题 | 详细信息 |
下图是实验室蒸馏装置图。可利用此装置将海水淡化,下列说法中正确的是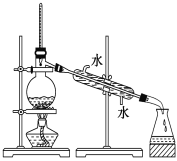 A.蒸馏时应将温度计插入海水中 B.蒸馏时冷水的流向应由上而下 C.利用此法淡化海水获得淡水质量高,但能耗大 D.蒸馏时温度计位置应在离液面2~3 mm 处 |
|
| 18. 选择题 | 详细信息 |
|
下列有关实验操作正确的是 A.蒸馏实验中温度计的水银球应插入液态混合物中 B.用酒精萃取碘水中的碘 C.分液时,打开旋塞,使下层液体从下口流出,上层液体从上口倒出 D.开始蒸馏时,应该先加热,再开冷凝水;蒸馏完毕,应先关冷凝水再撤酒精灯 |
|
| 19. 选择题 | 详细信息 |
|
现有三组溶液:①碘的饱和水溶液? ②汽油和氯化钠溶液? ③碳酸钙和水。分离以上各混合液的正确方法依次是 A. 萃取、分液、过滤 B. 萃取、分液、蒸馏 C. 分液、蒸馏、过滤 D. 蒸馏、萃取、过滤 |
|
| 20. 选择题 | 详细信息 |
|
下列说法正确的是 A.选择萃取剂将碘从碘水中萃取出来,这种萃取剂应具备的性质是不溶于水,且比水的密度大 B.选择萃取剂将碘从碘水中萃取出来,这种萃取剂应具备的性质是不溶于水,且比水的密度小 C.在使用分液漏斗进行分液时,上层液体经漏斗下口放出 D.选择萃取剂将碘从碘水中萃取出来,碘在四氯化碳中的溶解度比在水中的溶解度大 |
|
| 21. 选择题 | 详细信息 | |||||||||||||||
完成下列实验所需选择的装置或仪器都正确的是
|
||||||||||||||||
| 22. 选择题 | 详细信息 |
|
碘微溶于水,易溶于四氯化碳和酒精且碘易升华。现要将碘水中的碘分离出来,下列说法合理的是 A.碘易升华,可采用加热的方法将碘从溶液中升华出来 B.碘易溶于四氯化碳和酒精,所以可选用两种试剂中的任意一种进行萃取 C.四氯化碳比水重,酒精比水轻,所以用四氯化碳进行萃取比用酒精好 D.四氯化碳不溶于水,酒精溶于水,所以用四氯化碳萃取,不能用酒精 |
|
| 23. 选择题 | 详细信息 |
|
某同学根据苯和四氯化碳互溶、苯的密度比水小、四氯化碳的密度比水大的性质制作了如图所示的“液体积木”。在试管中注入CCl4,再加少量水,再小心加入少量苯,溶液可出现分三层的现象,然后再用漏斗向水层中加入少量胆矾溶液及少量碘水(如图所示)。下列说法正确的是 A.上中下三层的颜色分别为无色、蓝色、紫色 B.上中下三层的颜色分别为紫色、蓝色、紫色 C.振荡再静置后溶液分为两层,水在下层 D.振荡再静置后溶液仍分为三层 |
|
| 24. 实验题 | 详细信息 |
|
Ⅰ、实验室有如下仪器:①试管? ②烧杯? ③量筒? ④蒸发皿? ⑤锥形瓶? ⑥温度计? ⑦蒸馏烧瓶 ⑧分液漏斗。 回答下列问题: (1)可以直接加热的有____________(填序号,下同); (2)加热时必须垫上石棉网的有______________; (3)使用前必须查漏的有______________; Ⅱ、选取下列实验方法分离物质,将分离方法的序号填在横线上。 A.萃取分液法 B.结晶法 C.分液法 D.蒸馏法 E.过滤法 F.升华法 (1)________分离饱和食盐水与沙子的混合物。 (2)________分离水和汽油的混合物。 (3)________分离四氯化碳(沸点为76.75 ℃)和甲苯(沸点为110.6 ℃)的混合物。 (4)________分离NaCl和I2的固体混合物。 |
|
| 25. 实验题 | 详细信息 |
海藻中提取碘的流程如图,已知②中发生反应的化学方程式为:Cl2+2KI===2KCl+I2。请回答下列问题: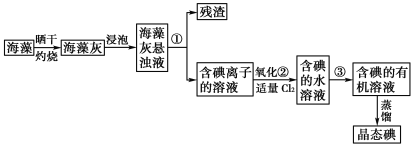 (1)指出提取碘的过程中有关实验操作①和③的名称:__________;________。 (2)在3 mL碘水中,加入1 mL四氯化碳,振荡、静置后,观察到试管里的分层现象是下图中的________(注:试管中深色区为紫红色溶液)。  (3)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏,指出如下图实验装置中的错误之处。(加热装置中烧杯底部已垫有石棉网) 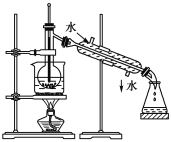 ①________________________________; ②________________________________。 |
|
| 26. 填空题 | 详细信息 |
|
除去下列物质中混有的少量杂质(杂质不要求回收),把适当的试剂、操作方法的序号写在相应的括号内。 a.加适量盐酸、过滤 b.加适量水、过滤、蒸发 c.加适量水、过滤 d.加热(高温或灼烧) e.加适量盐酸、蒸发 f.冷却热的饱和溶液、过滤 (1)碳酸钙中混有少量的碳酸钠 (? ) (2)氯化钾粉末中混有碳酸钾 (? ) (3)氧化钙中混有少量的碳酸钙 (? ) (4)二氧化锰中混有少量的炭粉 (? ) (5)硝酸钾中混有少量的食盐? (? ) |
|
| 27. 填空题 | 详细信息 |
|
有一包从海水中获得的粗盐,已经经过初步的提纯。课外活动小组对它的成分进行探究,并将粗盐进一步提纯。 探究一:这包粗盐中含有什么杂质? (1)根据海水的成分和初步提纯的实验操作,推断该粗盐中可能含有的杂质是CaCl2和MgCl2。 现在实验来验证这种推断:取样品并溶解,加入足量NaOH溶液,目的是检验有没有________;接着再加入数滴Na2CO3溶液,目的是检验有没有________。 实验证明:这包粗盐中含有的杂质是CaCl2。 探究二:这包粗盐中NaCl的质量分数是多少?按下面步骤继续进行实验: ①称取一定质量的样品;②将样品加水溶解,制成粗盐溶液;③向粗盐溶液中加入过量的某种试剂,过滤;④将沉淀洗涤后小心烘干,得到纯净的固体A;⑤滤液在进行某一操作后,移入蒸发皿进行蒸发,得到纯净的固体;⑥称量实验中得到的某种固体。 (2)步骤②③⑤中都使用到的仪器是________;它在步骤②和⑤的操作方法相同,但目的不同,在步骤②的目的是_________________,在步骤⑤的目的是______________________________; (3)步骤③中加入的试剂是________;步骤⑤中进行的“某一操作”是________________________________________,目的是____________________; (4)步骤⑥中你认为需要称量的固体是固体A还是固体B?________,你不选择另一种固体的理由是________________________________________________________________。 |
|
| 28. 填空题 | 详细信息 |
为了将混有K2SO4、MgSO4的KNO3固体提纯,并制得纯净的KNO3溶液,某同学设计如下实验方案: (1)操作①为________; (2)操作②~④加入的试剂可以为________; (3)如何判断SO已除尽,简述实验操作____________________ __________________________________________________________; (4)实验过程中产生的多次沉淀________(填“需要”或“不需要”)多次过滤,理由是 __________________________________________________________。 (5)该同学设计的实验方案________(填“合理”或“不合理”),理由是__________________________________________________。 |
|
| 29. 填空题 | 详细信息 | |||||||||||||||
|
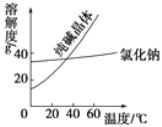
(1)阅读、分析下列两个材料: 材料一
材料二 |
||||||||||||||||
最近更新