2018еұҠй«ҳдёү10жңҲжңҲиҖғеҢ–еӯҰиҜ•еҚ·пјҲдёҠжө·еёӮж јиҮҙдёӯеӯҰпјү
| 1. | иҜҰз»ҶдҝЎжҒҜ |
|
еұһдәҺзү©зҗҶеҸҳеҢ–зҡ„жҳҜпјҲ? пјү A. йҮ‘еұһи…җиҡҖ B. е…үеҗҲдҪңз”Ё C. ж°§ж°”ж— иүІж— е‘і D. еҲҶзҰ»ж¶ІжҖҒз©әж°”жі•еҲ¶еҸ–ж°§ж°” |
|
| 2. | иҜҰз»ҶдҝЎжҒҜ |
|
й’ҷжҳҜжһ„жҲҗдәәдҪ“йӘЁйӘје’ҢзүҷйҪҝзҡ„йҮҚиҰҒжҲҗеҲҶпјҢиҝҷйҮҢзҡ„вҖңй’ҷвҖқжҳҜжҢҮпјҲ? пјү A. й’ҷеҚ•иҙЁ B. зўій…ёй’ҷ C. й’ҷеҺҹеӯҗ D. й’ҷе…ғзҙ |
|
| 3. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—зІ’еӯҗиғҪдҝқжҢҒж°®ж°”зҡ„еҢ–еӯҰжҖ§иҙЁзҡ„жҳҜпјҲ? пјү A. 2N B. N C. N2O D. N2 |
|
| 4. | иҜҰз»ҶдҝЎжҒҜ |
|
д»ҘдёӢеұһдәҺзәҜеҮҖзү©зҡ„жҳҜпјҲ? пјү A. еҶ°ж°ҙж··еҗҲзү© B. жҫ„жё…зҹізҒ°ж°ҙ C. еӨ§зҗҶзҹі D. ж¶ІжҖҒз©әж°” |
|
| 5. | иҜҰз»ҶдҝЎжҒҜ |
|
йҖҡиҝҮе®һйӘҢжөӢе®ҡеҮәз©әж°”з»„жҲҗзҡ„科еӯҰ家жҳҜпјҲ? пјү A. жі•еӣҪзҡ„жӢүз“Ұй”Ў B. иӢұеӣҪзҡ„жұӨе§Ҷз”ҹ C. з‘һе…ёзҡ„иҲҚеӢ’ D. ж„ҸеӨ§еҲ©зҡ„йҳҝдјҸеҠ еҫ·зҪ— |
|
| 6. | иҜҰз»ҶдҝЎжҒҜ |
|
зӣ®еүҚжҲ‘еӣҪи®ёеӨҡеҹҺеёӮе®ҡжңҹе…¬еёғз©әж°”иҙЁйҮҸжҠҘе‘ҠпјҢеңЁз©әж°”иҙЁйҮҸжҠҘе‘ҠдёӯпјҢ?иҲ¬дёҚж¶үеҸҠпјҲ пјү AпјҺдәҢж°§еҢ–зЎ« BпјҺдәҢж°§еҢ–зўі ? CпјҺж°®ж°§еҢ–еҗҲзү© DпјҺеҸҜеҗёе…Ҙйў—зІ’зү© |
|
| 7. | иҜҰз»ҶдҝЎжҒҜ |
|
з”ЁеҲҶеӯҗзҡ„и§ӮзӮ№и§ЈйҮҠдёӢеҲ—зҺ°иұЎпјҢй”ҷиҜҜзҡ„жҳҜпјҲ? пјү A. зғӯиғҖеҶ·зј©--еҲҶеӯҗеӨ§е°ҸйҡҸжё©еәҰзҡ„еҸҳеҢ–иҖҢж”№еҸҳ B. иҠұйҰҷеӣӣжәў--еҲҶеӯҗдёҚеҒңең°иҝҗеҠЁ C. йЈҹзү©и…җиҙҘ--еҲҶеӯҗеҸ‘з”ҹеҸҳеҢ– D. й…’зІҫжҢҘеҸ‘--еҲҶеӯҗй—ҙй—ҙйҡ”еҸҳеӨ§ |
|
| 8. | иҜҰз»ҶдҝЎжҒҜ |
|
еҠ зғӯж°Ҝй…ёй’ҫе’ҢдәҢж°§еҢ–й”°еҲ¶ж°§ж°”пјҢдәҢж°§еҢ–й”°еңЁеҢ–еӯҰеҸҚеә”еүҚеҗҺеҸ‘з”ҹеҸҳеҢ–зҡ„жҳҜпјҲ? пјү A. еңЁж··еҗҲзү©дёӯзҡ„иҙЁйҮҸзҷҫеҲҶеҗ«йҮҸ B. еҢ–еӯҰжҖ§иҙЁ C. з»„жҲҗ D. иҙЁйҮҸ |
|
| 9. | иҜҰз»ҶдҝЎжҒҜ |
|
е…ідәҺеҢ–еҗҲеҸҚеә”зҡ„еҸҷиҝ°жӯЈзЎ®зҡ„жҳҜпјҲ? пјү A. еҢ–еҗҲеҸҚеә”дёҖе®ҡжҳҜж°§еҢ–еҸҚеә” B. жңүж°§ж°”еҸӮеҠ зҡ„еҸҚеә”йғҪжҳҜеҢ–еҗҲеҸҚеә” C. з”ұдёӨз§ҚжҲ–дёӨз§Қд»ҘдёҠзҡ„зү©иҙЁз”ҹжҲҗеҸҰдёҖз§Қзү©иҙЁзҡ„еҸҚеә”еҸ«еҢ–еҗҲеҸҚеә” D. еҝ…йЎ»жңүж°§ж°”еҸӮеҠ дё”еҸӘиғҪз”ҹжҲҗдёҖз§Қзү©иҙЁзҡ„еҸҚеә”жүҚжҳҜеҢ–еҗҲеҸҚеә” |
|
| 10. | иҜҰз»ҶдҝЎжҒҜ |
|
еңЁд»ҘдёӢеҗ«ж°®е…ғзҙ зҡ„ж°”дҪ“дёӯпјҢеҢ–еҗҲд»·жңҖдҪҺзҡ„жҳҜпјҲ? пјү A. N2 B. NO C. NH3 D. NO2 |
|
| 11. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—жңүе…іе®һйӘҢзҺ°иұЎзҡ„жҸҸиҝ°пјҢй”ҷиҜҜзҡ„жҳҜпјҲ? пјү A. зЎ«еңЁж°§ж°”дёӯзҮғзғ§пјҢзҒ«з„°е‘ҲжҳҺдә®зҡ„и“қзҙ«иүІпјҢз”ҹжҲҗжңүеҲәжҝҖжҖ§ж°”е‘ізҡ„ж°”дҪ“ B. зЈ·еңЁз©әж°”дёӯзҮғзғ§зҒ«з„°е‘Ҳй»„иүІпјҢз”ҹжҲҗеӨ§йҮҸзҷҪзғҹ C. жңЁзӮӯеңЁж°§ж°”дёӯзҮғзғ§еҸ‘еҮәзҷҪе…үиҖҢеңЁз©әж°”дёӯзҮғзғ§еҲҷзҒјзғӯжҲҗзәўзғӯ D. й•ҒжқЎеңЁж°§ж°”дёӯзҮғзғ§пјҢзҒ«жҳҹеӣӣе°„пјҢз”ҹжҲҗй»‘иүІеӣәдҪ“ |
|
| 12. | иҜҰз»ҶдҝЎжҒҜ |
|
дёҺе®№з§Ҝзҡ„1/3жңүе…ізҡ„е®һйӘҢж“ҚдҪңжҳҜпјҲ? пјү A. з”ЁзәўзЈ·зҮғзғ§йҷӨеҺ»й’ҹзҪ©еҶ…з©әж°”дёӯзҡ„ж°§ж°” B. з»ҷй…’зІҫзҒҜдёӯж·»еҠ й…’зІҫ C. з”ЁеёҰзҒ«жҳҹзҡ„жңЁжқЎжЈҖйӘҢж°§ж°”жҳҜеҗҰйӣҶж»Ў D. з»ҷиҜ•з®ЎеҶ…зҡ„ж¶ІдҪ“еҠ зғӯ |
|
| 13. | иҜҰз»ҶдҝЎжҒҜ |
|
жҹҗеҢ–еӯҰеҸҚеә”A+B A. 20е…Ӣ B. 15е…Ӣ C. 10е…Ӣ D. 5е…Ӣ |
|
| 14. | иҜҰз»ҶдҝЎжҒҜ |
|
еҜ№зү©иҙЁзҡ„йҮҸзҡ„зҗҶи§ЈжӯЈзЎ®зҡ„жҳҜпјҲ? пјү A. зү©иҙЁзҡ„йҮҸе°ұжҳҜзү©иҙЁзҡ„иҙЁйҮҸзҡ„еҸҰдёҖз§ҚиЎЁиҫҫж–№ејҸпјҢеҚ•дҪҚжҳҜg/mol B. зү©иҙЁзҡ„йҮҸе°ұжҳҜзү©иҙЁзҡ„ж•°йҮҸпјҢж•°еҖјдёҠзӯүдәҺејҸйҮҸпјҢеҚ•дҪҚжҳҜmol C. зү©иҙЁзҡ„йҮҸе°ұжҳҜ6.02Г—1023дёӘеҫ®зІ’зҡ„иҙЁйҮҸпјҢеҚ•дҪҚжҳҜg D. зү©иҙЁзҡ„йҮҸжҳҜеӣҪйҷ…еҚ•дҪҚеҲ¶дёӯзҡ„дёҖдёӘзү©зҗҶйҮҸпјҢиЎЁзӨәеҗ«жңүдёҖе®ҡж•°зӣ®еҫ®зІ’зҡ„йӣҶдҪ“ |
|
| 15. | иҜҰз»ҶдҝЎжҒҜ |
|
SiO2жҳҜеҲ¶йҖ е…үеҜјзәӨз»ҙзҡ„дё»иҰҒеҺҹж–ҷпјҢдёӢеҲ—е…ідәҺSiO2зҡ„иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲ? пјү A. SiO2зҡ„ж‘©е°”иҙЁйҮҸжҳҜ60 B. 1mol SiO2дёӯеҗ«жңү1molO2 C. 1.5mol SiO2дёӯеҗ«жңү1.806Г—1024дёӘж°§еҺҹеӯҗ D. 1mol SiO2зҡ„иҙЁйҮҸжҳҜ60g/mol |
|
| 16. | иҜҰз»ҶдҝЎжҒҜ | ||||||||||||||||||
е°ҶдёҖе®ҡйҮҸзҡ„д№ҷйҶҮпјҲC2H5OHпјүе’Ңж°§ж°”зҪ®дәҺдёҖдёӘе°Ғй—ӯзҡ„е®№еҷЁдёӯеј•зҮғпјҢжөӢеҫ—еҸҚеә”еүҚеҗҺеҗ„зү©иҙЁзҡ„иҙЁйҮҸеҰӮдёӢиЎЁпјҡ
|
|||||||||||||||||||
| 17. | иҜҰз»ҶдҝЎжҒҜ |
|
еҸӘеҗ«жңүдёҖз§Қе…ғзҙ зҡ„зү©иҙЁпјҢдёҚеҸҜиғҪжҳҜпјҲ? пјү A. ж··еҗҲзү© B. зәҜеҮҖзү© C. еҚ•иҙЁ D. еҢ–еҗҲзү© |
|
| 18. | иҜҰз»ҶдҝЎжҒҜ |
|
з”ҳж°Ёй…ёзҡ„еҢ–еӯҰејҸдёәC2H5O2NпјҢе…ідәҺ0.5molC2H5O2Nи®Ўз®—з»“жһңй”ҷиҜҜзҡ„жҳҜпјҲ? пјү A. еҲҶеӯҗдёӘж•°зәҰдёәпјҡ3.01Г—1023 B. ејҸйҮҸпјҡ75 C. еҺҹеӯҗзҡ„зү©иҙЁзҡ„йҮҸзҡ„жҖ»е’Ңпјҡ4.5mol D. ж°§е…ғзҙ иҙЁйҮҸпјҡ16g |
|
| 19. | иҜҰз»ҶдҝЎжҒҜ |
жІ»зҗҶжұҪиҪҰе°ҫж°”жүҖж¶үеҸҠеҸҚеә”зҡ„йғЁеҲҶеҫ®и§ӮиҝҮзЁӢеҰӮдёӢеӣҫжүҖзӨәпјҢжңүе…іеҸҷиҝ°жӯЈзЎ®зҡ„пјҲ? пјү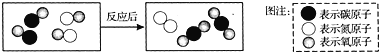 A. C. иҜҘеҸҚеә”жҳҜеҢ–еҗҲеҸҚеә” D. еҲҶеӯҗжҖ»ж•°еңЁеҸҚеә”еүҚеҗҺеҸ‘з”ҹеҸҳеҢ– |
|
| 20. | иҜҰз»ҶдҝЎжҒҜ |
еҚ•иҙЁMдёҺж°§ж°”еҸҚеә”дёәпјҡ2M+O2вҶ’2MOпјҢеҸӮеҠ еҸҚеә”зҡ„MдёҺз”ҹжҲҗзҡ„MOиҙЁйҮҸе…ізі»еҰӮеӣҫжүҖзӨәпјҢеҲҷMOзҡ„ж‘©е°”иҙЁйҮҸпјҲg/molпјүдёәпјҲ? пјү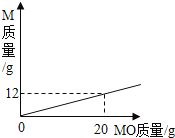 A. 24 B. 40 C. 48 D. 80 |
|
| 21. | иҜҰз»ҶдҝЎжҒҜ |
|
з”ЁеҢ–еӯҰиҜӯиЁҖиЎЁзӨәжҲ–еҶҷеҮәз¬ҰеҸ·иЎЁзӨәзҡ„еҗ«д№ү пјҲ1пјү2дёӘж°ҰеҺҹеӯҗ__________гҖӮпјҲ2пјү2molзҡ„зЎ«еҺҹеӯҗ__________гҖӮ пјҲ3пјү2дёӘзЎ«й…ёж №еҺҹеӯҗеӣў__________гҖӮпјҲ4пјү2SO2 ____________гҖӮ |
|
| 22. | иҜҰз»ҶдҝЎжҒҜ |
|
з”ЁеҢ–еӯҰз¬ҰеҸ·иЎЁзӨәпјҡ пјҲ1пјүеёёжё©дёӢеҜҶеәҰжңҖе°Ҹзҡ„ж°”дҪ“дёә_______пјӣ пјҲ2пјүең°еЈідёӯеҗ«йҮҸжңҖеӨҡзҡ„е…ғзҙ дёә_______пјҢз©әж°”дёӯеҗ«йҮҸжңҖеӨҡзҡ„е…ғзҙ дёә_________пјӣ пјҲ3пјүеҶҷеҮәең°еЈідёӯеҗ«йҮҸжңҖеӨҡзҡ„йҮ‘еұһе…ғзҙ пјҢ并表жҳҺе…¶еңЁеҢ–е’Ңзү©дёӯзҡ„еҢ–еҗҲд»·__________гҖӮ |
|
| 23. | иҜҰз»ҶдҝЎжҒҜ |
|
ж°®ж°”гҖҒж°§ж°”гҖҒж°Ұж°”гҖҒж°ҙи’ёж°”е’ҢдәҢж°§еҢ–зўійғҪжҳҜз©әж°”зҡ„жҲҗеҲҶпјҺиҜ·з”ЁеҢ–еӯҰејҸеЎ«еҶҷпјҡ пјҲ1пјүиғҪз”ЁдәҺжҠўж•‘з—…дәәпјҢдҫӣз»ҷе‘јеҗёзҡ„ж°”дҪ“жҳҜ____пјӣ пјҲ2пјүз©әж°”дёӯеҗ«йҮҸеҚҮй«ҳдјҡеј•иө·жё©е®Өж•Ҳеә”зҡ„ж°”дҪ“жҳҜ____пјӣ пјҲ3пјүеҚ з©әж°”дҪ“з§Ҝ78%пјҢеёёз”ЁдҪңз„ҠжҺҘйҮ‘еұһдҝқжҠӨж°”зҡ„жҳҜ____пјӣ пјҲ4пјүжҖ§иҙЁеҫҲзЁіе®ҡпјҢеҸҜз”ЁдәҺеЎ«е……жҺўз©әж°”зҗғжҲ–йЈһиүҮзҡ„ж°”дҪ“жҳҜ____пјӣ пјҲ5пјүзӮҺзғӯзҡ„еӨҸеӯЈд»ҺеҶ°з®ұжӢҝеҮәзҡ„йҘ®ж–ҷ瓶еӨ–еЈҒдёҠдјҡеҮқз»“дёҖеұӮе°Ҹж¶Іж»ҙпјҢиҜҙжҳҺз©әж°”дёӯеҗ«жңү____пјҺ |
|
| 24. | иҜҰз»ҶдҝЎжҒҜ |
| и‘Ўиҗ„зі–пјҲе…¶еҢ–еӯҰејҸдёәC6H12O6пјүжҳҜз”ҹе‘Ҫжҙ»еҠЁдёӯдёҚеҸҜзјәе°‘зҡ„зү©иҙЁпјҺи‘Ўиҗ„зі–з”ұ______з§Қе…ғзҙ з»„жҲҗпјҢеҗ„е…ғзҙ еҺҹеӯҗдёӘж•°жҜ”жҳҜ______пјӣ1дёӘи‘Ўиҗ„зі–еҲҶеӯҗдёӯе…ұеҗ«______дёӘеҺҹеӯҗпјӣи‘Ўиҗ„зі–дёӯиҙЁйҮҸеҲҶж•°жңҖй«ҳзҡ„е…ғзҙ дёә______пјӣ0.5molи‘Ўиҗ„зі–зҡ„иҙЁйҮҸдёә______gпјӣ0.1mol иҜҘзү©иҙЁдёӯзәҰеҗ«жңү______дёӘж°§еҺҹеӯҗгҖӮ | |
| 25. | иҜҰз»ҶдҝЎжҒҜ |
|
иҙЁйҮҸе®ҲжҒ’е®ҡеҫӢзҡ„е®ҡйҮҸз ”з©¶еҜ№еҢ–еӯҰ科еӯҰеҸ‘еұ•е…·жңүйҮҚеӨ§ж„Ҹд№үгҖӮ пјҲ1пјүдёӢеӣҫдёәжҹҗеҢ–еӯҰеҸҚеә”зҡ„еҫ®и§ӮжЁЎжӢҹеӣҫпјҢвҖңв—ӢвҖқе’ҢвҖң 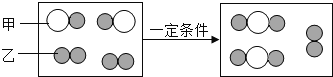 з”ұеҫ®зІ’з”ІвҖң пјҲ2пјүжҠҠm1gй•ҒеёҰж”ҫеңЁз©әж°”дёӯе®Ңе…ЁзҮғзғ§пјҢйҖҡиҝҮи®Ўз®—еҸҜзҹҘпјҢз”ҹжҲҗж°§еҢ–й•Ғm2gпјҲеҸӘиҖғиҷ‘дёҺж°§ж°”зҡ„еҸҚеә”пјҢдёӢеҗҢпјүпјҢеҲҷm1______m2пјҲеЎ«еӨ§дәҺжҲ–е°ҸдәҺжҲ–зӯүдәҺпјүгҖӮе°ҸеҳүеҗҢеӯҰеңЁеҒҡиҜҘе®һйӘҢж—¶пјҢи§ӮеҜҹеҲ°иҖҖзңјзҡ„зҷҪе…үпјҢеҶ’еҮәеӨ§йҮҸзҷҪзғҹпјҢз§°йҮҸж— иҜҜж—¶пјҢеҸ‘зҺ°m1пјһm2пјҢе…¶еҺҹеӣ еҸҜиғҪжҳҜ______гҖӮ |
|
| 26. | иҜҰз»ҶдҝЎжҒҜ |
вҖңз©әж°”дёӯж°§ж°”дҪ“з§ҜеҲҶж•°зҡ„жөӢе®ҡвҖқжңүеӨҡз§Қж–№жі•пјҢиҜ·жҢүиҰҒжұӮеӣһзӯ”дёӢеҲ—й—®йўҳпјҡеңЁзҮғзғ§еҢҷеҶ…зӣӣиҝҮйҮҸзәўзЈ·пјҢзәўзЈ·еҝ…йЎ»иҝҮйҮҸзҡ„еҺҹеӣ жҳҜ______пјҢзӮ№зҮғзәўзЈ·еҗҺз«ӢеҚіжҸ’е…ҘйӣҶ气瓶еҶ…пјҢеЎһзҙ§ж©Ўзҡ®еЎһзәўзЈ·зҮғзғ§зҡ„зҺ°иұЎжҳҜ____________пјҢе…¶еҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸдёә____________________гҖӮеҫ…зәўзЈ·зҒ«з„°зҶ„зҒӯпјҢйӣҶ气瓶еҶ·еҚҙиҮіе®Өжё©пјҢжү“ејҖжӯўж°ҙеӨ№пјҢи§ӮеҜҹеҲ°зҡ„зҺ°иұЎжҳҜ______пјҢиҜҘе®һйӘҢйҷӨдәҶеҫ—еҮәж°§ж°”еңЁз©әж°”дёӯзҡ„дҪ“з§ҜеҲҶж•°д№ӢеӨ–пјҢиҝҳиғҪеҫ—еҮәж°®ж°”е…·жңүзҡ„жҖ§иҙЁжҳҜ______пјҲд»»еҶҷдёҖзӮ№пјүпјӣиӢҘжөӢеҫ—з©әж°”дёӯж°§ж°”зҡ„дҪ“з§ҜеҲҶж•°зәҰдёә1/7пјҢеҲҷеҸҜиғҪзҡ„еҺҹеӣ жҳҜ______гҖӮ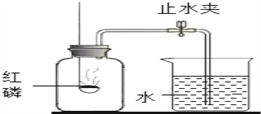 |
|
| 27. | иҜҰз»ҶдҝЎжҒҜ |
е°Ҹй—өеҗҢеӯҰжӢҘжңүдёӢеҲ—е®һйӘҢд»ӘеҷЁпјҡ пјҲ1пјүеҶҷеҮәд»ӘеҷЁеҗҚз§°пјҡc______гҖӮ пјҲ2пјүе®һйӘҢе®Өз”Ёж°Ҝй…ёй’ҫе’ҢдәҢж°§еҢ–й”°еҲ¶еҸ–ж°§ж°”пјҡ в‘ дёҠиҝ°д»ӘеҷЁдёӯдёҚйңҖиҰҒз”ЁеҲ°зҡ„жҳҜпјҲеЎ«еәҸеҸ·пјү_____гҖӮ в‘ЎеңЁз”ЁжҺ’ж°ҙ法收йӣҶж°§ж°”зҡ„иҝҮзЁӢдёӯпјҢеҲӨж–ӯйӣҶ气瓶дёӯж°§ж°”е·ІйӣҶж»Ўзҡ„зҺ°иұЎжҳҜ______гҖӮ A.йӣҶ气瓶дёӯж°ҙдҪҚдёӢйҷҚдәҶпјӣ B.еңЁж°ҙж§ҪдёӯеҮәзҺ°ж°”жіЎпјӣ C.е°ҶеёҰзҒ«жҳҹзҡ„жңЁжқЎж”ҫеңЁйӣҶ气瓶еҸЈпјҢжңЁжқЎеӨҚзҮғгҖӮ в‘ўиҰҒд»ҺеҸҚеә”еҗҺзҡ„еү©дҪҷеӣәдҪ“дёӯеӣһ收дәҢж°§еҢ–й”°пјҢйңҖиҰҒд»ҘдёӢж“ҚдҪңжӯҘйӘӨпјҡ______гҖҒ______гҖҒжҙ—ж¶ӨгҖҒзғҳе№ІгҖӮ в‘Је°Ҹй—өжҳҜеҗҰеҸҜд»Ҙз”Ёеҗ‘дёҠжҺ’з©ә气法收йӣҶж°§ж°”______пјҲеЎ«еҶҷжҳҜжҲ–еҗҰпјүгҖӮ в‘Өе°Ҹй—өиӢҘеңЁе®һйӘҢе®ӨеҲ©з”Ё12.25gж°Ҝй…ёй’ҫдёҺ3gMnO2ж··еҗҲеҠ зғӯпјҢеҲ—ејҸи®Ўз®—жңҖеӨҡеҸҜд»Ҙеҫ—еҲ°еӨҡе°‘зү©иҙЁзҡ„йҮҸзҡ„ж°§ж°”____________________________гҖӮ |
|
й«ҳдёӯеҢ–еӯҰ иҜ•еҚ·жҺЁиҚҗ
- 2017-2018е№ҙй«ҳдёҖдёҠеӯҰжңҹжңҹдёӯиҖғиҜ•еҢ–еӯҰиҜ•еҚ·пјҲж–°з–Ҷе…өеӣўз¬¬дәҢеёҲеҚҺеұұдёӯеӯҰпјү
- еӨ©жҙҘеёӮй«ҳдёҖеҢ–еӯҰжңҲиҖғжөӢйӘҢпјҲ2019е№ҙеҗҺеҚҠжңҹпјүе…Қиҙ№иҜ•еҚ·
- 2017-2018е№ҙй«ҳдәҢдёҠеӯҰжңҹжңҹдёӯиҖғиҜ•еҢ–еӯҰеңЁзәҝжөӢйӘҢпјҲеҶ…и’ҷеҸӨе·ҙеҪҰж·–е°”еёӮ第дёҖдёӯеӯҰпјү
- жң”е·һеёӮ2019е№ҙй«ҳдёҖеҢ–еӯҰдёҠеҶҢжңҲиҖғжөӢйӘҢе…Қиҙ№иҜ•еҚ·е®Ңж•ҙзүҲ
- 2017-2018е№ҙй«ҳдәҢ12жңҲжңҲиҖғеҢ–еӯҰиҖғйўҳеёҰзӯ”жЎҲе’Ңи§ЈжһҗпјҲжұҹиҘҝзңҒжҠҡе·һеёӮдёҙе·қеҢә第дёҖдёӯеӯҰпјү
- 2017-2018е№ҙй«ҳдёҖдёҠеӯҰжңҹжңҹдёӯиҖғиҜ•еҢ–еӯҰиҖғиҜ•йўҳпјҲе®ҒеӨҸиӮІжүҚдёӯеӯҰпјү
- 2017-2018е№ҙй«ҳдёҖдёҠеӯҰжңҹжңҲиҖғеҢ–еӯҰиҖғйўҳеёҰзӯ”жЎҲе’Ңи§ЈжһҗпјҲеұұиҘҝзңҒеә”еҺҝ第дёҖдёӯеӯҰж Ўпјү
- 2016-2017е№ҙй«ҳдёҖеүҚеҚҠжңҹеҢ–еӯҰжңҹдёӯиҖғиҜ•иҖғйўҳеёҰзӯ”жЎҲе’Ңи§ЈжһҗпјҲеҗүжһ—зңҒиҫҪжәҗеёӮжҷ®йҖҡй«ҳдёӯпјү
жңҖиҝ‘жӣҙж–°



