2019届初三上半期第二次月考理科综合化学考题(湖北省阳新实验中学)
| 1. | 详细信息 |
|
如图所示实验操作中,正确的是 A.  B. B.  C. C.  D. D. |
|
| 2. | 详细信息 |
如图是某元素的原子结构示意图和该元素在元素周期表中的单元格,下列说法不正确的是 A. 该元素属于金属元素 B. 该原子在化学变化中容易失去电子 C. 该原子的相对原子质量是47.87g D. 该原子的原子序数为22 |
|
| 3. | 详细信息 | |||||||||||||||
化学的眼光看世界,能够提高我们的科学素养.下列变化事实和相应解释不一致的是
|
||||||||||||||||
| 4. | 详细信息 |
|
下图是表示物质分子的示意图.图中 A.  B. B. 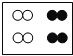 C. C.  D. D. 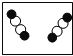 |
|
| 5. | 详细信息 | |||||||||||||||
在一个密闭容器中放入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表:
|
||||||||||||||||
| 6. | 详细信息 |
|
生活中处处有化学.现有以下常见的物质: A.明矾 B.活性炭 C.稀有气体 D.干冰. E. 金刚石 F.一氧化碳 请按要求填空(填上述相应物质的字母): (1)常用于冰箱除臭的是____. (2)可作灯泡填充气的是____. (3)可用来切割玻璃的是____; (4)有毒的气体是____; (5)用于人工降雨的是______. (6)可用于乡村或野外净水的是____. |
|
| 7. | 详细信息 |
(题文)水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任.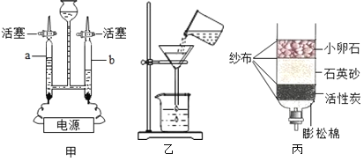 (1)下列“水”属于纯净物的是____(填序号) A.蒸馏水 B.河水 C.自来水 (2)用如图甲装置进行电解水的实验,b中收集到的气体是_____ ,该实验说明水是由________________组成的. (3)图乙进行的操作叫_______,其中存在的二处明显错误是: ①____________________;②_______________________ (4)阳新水资源丰富,但分布不均.有些村民用地下水作为生活用水,人们常用_________检验地下水是硬水还是软水;生活中可用_________的方法降低水的硬度. |
|
| 8. | 详细信息 |
|
用数字和化学符号表示下列意义: (1)相对分子质量最小的氧化物_____ (2)2个镁离子______ (3)氧化铁中铁元素的化合价________(4)氩气________ |
|
| 9. | 详细信息 |
老师为同学们提供了如图所示的实验装置: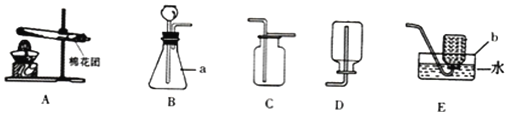 (1)写出仪器a的名称:a_______, (2)若用高锰酸钾制取氧气,反应的化学方程式为:____________________________,选择的发生装置为____(填代号),收集较纯净的氧气可选用_____装置(填代号). (3)若实验室用大理石制取二氧化碳,选择的发生装置是__(填序号),收集装置是_______(填序号),检验二氧化碳气体的化学方程式是__________________________. |
|
| 10. | 详细信息 | ||||||||||||
|
学校化学兴趣小组的同学知道二氧化锰能作过氧化氢(H2O2)分解的催化剂后,想再探究其他一些物质如氧化铜是否也可作过氧化氢分解的催化剂.请你参与他们的探究过程,并填写下列空白. (提出问题)氧化铜能不能作过氧化氢分解的催化剂呢? (作出猜想)氧化铜能作过氧化氢分解的催化剂. (实验验证)
|
|||||||||||||
| 11. | 详细信息 |
|
为了验证质量守恒定律.甲、乙、丙三位同学各做了一个实验. (1)甲同学用实验测定的数据有:木炭和坩埚的总质量mg;其燃烧后灰烬和坩埚的总质量为ng.m和n的关系为:m_____n(填“<”或“>”或“=”). (2)乙同学用实验测定的数据有:光亮的镁带的质量为xg;其在空气中完全燃烧之后生成的白色固体质量为yg. x和y的关系为:x____y(填“<”或“>”或“=”). (3)丙同学实验测定的数据有:锌、硫酸铜溶液和烧杯的总质量为ag;其反应后的混合物和烧杯的总质量为bg.a与b的关系为:a_____b(填“<”或“>”或“=”). (4)通过对三个实验的分析,你认为用有气体参加或生成的化学反应来验证质量守恒定律时,应___________,才能判定参加化学反应的反应物总质量和生成物总质量是否相等. |
|
| 12. | 详细信息 |
钙是维持人体正常功能所必需的元素.如图所示为某种补钙剂“钙尔奇”说明书的一部分.取1片钙尔奇,放入盛有10g稀盐酸的烧杯中,其中碳酸钙跟盐酸恰好完全反应(其他成分与盐酸不反应).烧杯内物质质量变为11.34g.试计算: (1)产生二氧化碳的质量是____. (2)每片钙尔奇中含碳酸钙的质量.(写出计算过程)____ |
|



