2016еұұдёңд№қе№ҙзә§дёӢеӯҰжңҹдәәж•ҷзүҲеҲқдёӯеҢ–еӯҰжңҲиҖғиҜ•еҚ·
| 1. | иҜҰз»ҶдҝЎжҒҜ |
|
е®һйӘҢе®ӨдёӯдёӢеҲ—зү©иҙЁеӣ жІЎжңүеҜҶе°ҒдҝқеӯҳиҖҢдҪҝиҙЁйҮҸеҮҸе°‘зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺжө“зЎ«й…ёВ В BпјҺз”ҹзҹізҒ°В В CпјҺзғ§зўұ DпјҺжө“зӣҗй…ё
|
|
| 2. | иҜҰз»ҶдҝЎжҒҜ |
|
й…ёе…·жңүй…ёзҡ„йҖҡжҖ§зҡ„еҺҹеӣ жҳҜпјҲгҖҖгҖҖпјү AпјҺй…ёйғҪиғҪз”өзҰ»еҮәH+В В BпјҺй…ёйғҪеҗ«жңүй…ёж № CпјҺй…ёдёӯйғҪеҗ«жңүж°ўе…ғзҙ DпјҺй…ёдёӯйғҪеҗ«жңүж°§е…ғзҙ
|
|
| 3. | иҜҰз»ҶдҝЎжҒҜ | ||||||||||
|
дёӢиЎЁжҳҜйғЁеҲҶеҶңдҪңзү©з”ҹй•ҝеҜ№еңҹеЈӨpHзҡ„иҰҒжұӮпјҺеҰӮжһңжҹҗең°еҢәз»ҸеёёйҷҚй…ёйӣЁпјҢеҲҷиҜҘең°еҢәжңҖдёҚйҖӮеҗҲз§ҚжӨҚзҡ„еҶңдҪңзү©жҳҜпјҲгҖҖгҖҖпјү
AпјҺеӨ§иұҶ BпјҺиҢ¶В В CпјҺзҺүзұі DпјҺ马й“ғи–Ҝ
|
|||||||||||
| 4. | иҜҰз»ҶдҝЎжҒҜ |
|
ж №жҚ®дёӢеҲ—е®һйӘҢзҺ°иұЎеҸҜд»ҘеҲӨж–ӯжҹҗжә¶ж¶ІдёҖе®ҡе‘ҲзўұжҖ§зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺеёёжё©дёӢпјҢжөӢеҫ—жә¶ж¶Ізҡ„pHпјң7В BпјҺжә¶ж¶Ідёӯж»ҙе…Ҙй…ҡй…һжҳҫзәўиүІ CпјҺжә¶ж¶Ідёӯж»ҙе…Ҙзҹіи•ҠжҳҫзәўиүІ DпјҺжә¶ж¶Ідёӯж»ҙе…Ҙй…ҡй…һдёҚжҳҫиүІ
|
|
| 5. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—е…ідәҺpHзҡ„иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺй…ёжә¶ж¶Ізҡ„pHи¶ҠеӨ§й…ёжҖ§и¶Ҡејә BпјҺзўұжә¶ж¶Ізҡ„pHеӨ§дәҺ7пјҢзӣҗжә¶ж¶Ізҡ„pHзӯүдәҺ7 CпјҺжөӢе®ҡжә¶ж¶Ізҡ„pHж—¶пјҢйңҖе…Ҳе°ҶpHиҜ•зәёж№ҝж¶Ұ DпјҺжөӢе®ҡдәәдҪ“еҶ…ж¶ІдҪ“зҡ„pHпјҢеҸҜд»ҘдәҶи§ЈдәәдҪ“зҡ„еҒҘеә·зҠ¶еҶө
|
|
| 6. | иҜҰз»ҶдҝЎжҒҜ |
|
жҺЁзҗҶжҳҜеҢ–еӯҰеӯҰд№ дёӯеёёи§Ғзҡ„жҖқз»ҙж–№жі•пјҺдёӢеҲ—жҺЁзҗҶжӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺзўұжҖ§жә¶ж¶ІиғҪдҪҝй…ҡй…һиҜ•ж¶ІеҸҳзәўпјҢж»ҙе…Ҙй…ҡй…һиҜ•ж¶ІеҗҺеҸҳзәўзҡ„жә¶ж¶ІдёҖе®ҡе‘ҲзўұжҖ§ BпјҺй”Ңе’Ңй“ңеқҮжҳҜйҮ‘еұһпјҢй”ҢдёҺзЁҖзЎ«й…ёеҸҚеә”з”ҹжҲҗж°ўж°”пјҢеҲҷй“ңд№ҹиғҪдёҺзЁҖзЎ«й…ёеҸҚеә”з”ҹжҲҗж°ўж°” CпјҺй…ёиғҪдҪҝзҹіи•ҠиҜ•ж¶ІеҸҳзәўпјҢCO2д№ҹиғҪдҪҝзҙ«иүІзҡ„зҹіи•ҠиҜ•ж¶ІеҸҳзәўпјҢжүҖд»ҘCO2жҳҜй…ё DпјҺжә¶ж¶Ідёӯжңүжҷ¶дҪ“жһҗеҮәпјҢе…¶жә¶иҙЁиҙЁйҮҸеҮҸе°ҸпјҢжүҖд»Ҙжә¶иҙЁзҡ„иҙЁйҮҸеҲҶж•°дёҖе®ҡеҮҸе°Ҹ
|
|
| 7. | иҜҰз»ҶдҝЎжҒҜ |
|
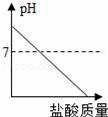
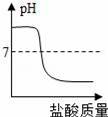
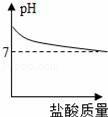
еңЁNa2CO3жә¶ж¶ІдёӯйҖҗжёҗеҠ е…Ҙзӣҗй…ёпјҢеҸҚеә”еҗҺжә¶ж¶ІpHйҡҸеҠ е…Ҙзӣҗй…ёиҙЁйҮҸеҸҳеҢ–зҡ„е…ізі»дёәпјҲгҖҖгҖҖпјү AпјҺ
|
|
| 8. | иҜҰз»ҶдҝЎжҒҜ |
|
й…ёдёҺзўұдҪңз”Ёз”ҹжҲҗзӣҗе’Ңж°ҙзҡ„еҸҚеә”пјҢеҸ«еҒҡдёӯе’ҢеҸҚеә”пјҺдёӢеҲ—еә”з”ЁдёҺдёӯе’ҢеҸҚеә”еҺҹзҗҶж— е…ізҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺз”ЁзҶҹзҹізҒ°е’ҢзЎ«й…ёй“ңй…ҚеҲ¶жіўе°”еӨҡж¶І BпјҺжңҚз”Ёеҗ«MgпјҲOHпјү2зҡ„иҚҜзү©жІ»з–—иғғй…ёиҝҮеӨҡ CпјҺж–Ҫз”ЁзҶҹзҹізҒ°ж”№иүҜй…ёжҖ§еңҹеЈӨ DпјҺз”ЁNaOHжә¶ж¶Іжҙ—ж¶ӨзҹіжІ№дә§е“Ғдёӯзҡ„ж®ӢдҪҷзЎ«й…ё
|
|
| 9. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—зү©иҙЁжә¶дәҺж°ҙпјҢжүҖеҫ—жә¶ж¶Ізҡ„pHеӨ§дәҺ7зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺCO2В BпјҺHClВ CпјҺNaCl DпјҺCaпјҲOHпјү2
|
|
| 10. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—жңүе…іж°ўж°§еҢ–й’ жҖ§иҙЁзҡ„иҜҙжі•й”ҷиҜҜзҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺж°ўж°§еҢ–й’ жңүи…җиҡҖжҖ§ BпјҺеӣәдҪ“ж°ўж°§еҢ–й’ жңүжҢҘеҸ‘жҖ§ CпјҺж°ўж°§еҢ–й’ иғҪеҗёж”¶дәҢж°§еҢ–зўіиҖҢеҸҳиҙЁ DпјҺеӣәдҪ“ж°ўж°§еҢ–й’ иғҪеҗёж”¶ж°ҙи’ёж°”иҖҢжҪ®и§Ј
|
|
| 11. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҗ„з»„зү©иҙЁжҢүй…ёгҖҒзўұгҖҒеҚ•иҙЁгҖҒж°§еҢ–зү©йЎәеәҸжҺ’еҲ—зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺH2SO4 Na2OВ В В CВ В В CO BпјҺMgпјҲOHпјү2В В CuSO4В В В CВ В В CO2 CпјҺKOHВ В HNO3В В O2В В SO3 DпјҺHClВ В NaOHВ В O2В В P2O5
|
|
| 12. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—е®һдҫӢдёҚеұһдәҺдёӯе’ҢеҸҚеә”зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺеңҹеЈӨй…ёеҢ–еҗҺеҠ е…ҘзҶҹзҹізҒ°ж”№иүҜ BпјҺиғғй…ёеҲҶжіҢиҝҮеӨҡзҡ„з—…дәәйҒөеҢ»еҳұжңҚз”Ёеҗ«жңүж°ўж°§еҢ–й“қзҡ„иҚҜзү©д»Ҙдёӯе’ҢиҝҮеӨҡиғғй…ё CпјҺиҡҠиҷ«еҸ®е’¬дәәзҡ„зҡ®иӮӨеҲҶжіҢеҮәиҡҒй…ёпјҢеҰӮжһңж¶Ӯеҗ«зўұжҖ§зү©иҙЁзҡ„иҚҜж°ҙе°ұеҸҜеҮҸиҪ»з—ӣз—’ DпјҺйҮ‘еұһиЎЁйқўй”ҲиҡҖеҗҺпјҢеҸҜз”ЁзЁҖзӣҗй…ёиҝӣиЎҢжё…жҙ—
|
|
| 13. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—жЈҖжөӢжҹҗжә¶ж¶ІpHзҡ„ж“ҚдҪңжӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺе°ҶpHиҜ•зәёжҠ•е…Ҙеҫ…жөӢж¶ІпјҢеҜ№з…§ж ҮеҮҶжҜ”иүІеҚЎиҜ»ж•° BпјҺз”Ёе№ІзҮҘгҖҒжҙҒеҮҖзҡ„зҺ»з’ғжЈ’иҳёеҸ–е°‘йҮҸеҫ…жөӢж¶ІпјҢжІҫеңЁзҪ®дәҺжҙҒеҮҖиЎЁйқўзҡҝзҡ„pHиҜ•зәёдёҠпјҢеҚҠеҲҶй’ҹеҶ…ж №жҚ®иҜ•зәёе‘ҲзҺ°йўңиүІпјҢеҜ№з…§ж ҮеҮҶжҜ”иүІеҚЎиҜ»ж•° CпјҺз”ЁзҺ»з’ғжЈ’иҳёеҸ–еҫ…жөӢж¶ІжІҫеңЁз”Ёи’ёйҰҸж°ҙж¶Ұж№ҝзҡ„pHиҜ•зәёдёҠпјҺеҜ№з…§ж ҮеҮҶжҜ”иүІеҚЎиҜ»ж•° DпјҺз”ЁзҺ»з’ғжЈ’иҳёеҸ–еҫ…жөӢж¶ІжІҫеңЁpHиҜ•зәёдёҠпјҢ3еҲҶй’ҹеҗҺеҜ№з…§ж ҮеҮҶжҜ”иүІеҚЎиҜ»ж•°
|
|
| 14. | иҜҰз»ҶдҝЎжҒҜ | ||||||||||
|
еёёи§ҒйЈҹзү©pHзҡ„иҝ‘дјјеҖјиҢғеӣҙеҰӮдёӢпјҡ
дёӢеҲ—иҜҙжі•дёӯпјҢдёҚжӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺйёЎиӣӢжё…жҳҫзўұжҖ§ BпјҺиғғй…ёиҝҮеӨҡзҡ„дәәеә”е°‘еҗғжіЎиҸң CпјҺж©ҳеӯҗжұҒиғҪдҪҝзҹіи•Ҡжә¶ж¶ІеҸҳзәўВ В DпјҺй…ёзүӣеҘ¶жҜ”ж©ҳеӯҗжұҒзҡ„й…ёжҖ§ејә
|
|||||||||||
| 15. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—жҪ®ж№ҝзҡ„ж°”дҪ“дёҚиғҪз”ЁеӣәдҪ“зҡ„ж°ўж°§еҢ–й’ е№ІзҮҘзҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺдёҖж°§еҢ–зўі BпјҺж°ўж°” CпјҺдәҢж°§еҢ–зўі DпјҺж°§ж°”
|
|
| 16. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҒҡжі•дёҚ科еӯҰзҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺз”Ёе№ІеҶ°дәәе·ҘйҷҚйӣЁВ В BпјҺз”ЁзҶҹзҹізҒ°з»ҷйұјеЎҳж¶ҲжҜ’ CпјҺжңҚз”Ёж°ўж°§еҢ–й’ жІ»иғғз—…В В DпјҺз”ЁйЈҹйҶӢйҷӨеҺ»ж°ҙеһў
|
|
| 17. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺзӣҗй…ёиғҪдҪҝзҙ«иүІзҹіи•ҠиҜ•ж¶ІеҸҳи“қ BпјҺжө“зЎ«й…ёйңІзҪ®дәҺз©әж°”дёӯпјҢжә¶иҙЁиҙЁйҮҸеҲҶж•°еҸҳеӨ§ CпјҺйңІзҪ®дәҺз©әж°”дёӯзҡ„еӣәдҪ“ж°ўж°§еҢ–й’ пјҢе…¶жҲҗеҲҶдёҚдјҡеҸ‘з”ҹеҸҳеҢ– DпјҺжү“ејҖжө“зӣҗй…ёзҡ„иҜ•еүӮ瓶пјҢ瓶еҸЈдјҡдә§з”ҹзҷҪйӣҫ
|
|
| 18. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҗ„з»„зү©иҙЁй—ҙзҡ„еҸҚеә”пјҢз”ұдәҺзҺ°иұЎдёҚжҳҺжҳҫйңҖиҰҒеҖҹеҠ©й…ёзўұжҢҮзӨәеүӮжүҚиғҪеҲӨж–ӯеҮәеҸҚеә”еҸ‘з”ҹзҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺй”ҢдёҺзЁҖзӣҗй…ёВ В BпјҺзғ§зўұжә¶ж¶ІдёҺзЁҖзЎ«й…ё CпјҺж°§еҢ–й“ҒдёҺзЁҖзЎ«й…ёВ В DпјҺзЎ«й…ёй“ңжә¶ж¶ІдёҺж°ўж°§еҢ–й’ жә¶ж¶І
|
|
| 19. | иҜҰз»ҶдҝЎжҒҜ |
|
е®һйӘҢе®ӨжңүдёӨ瓶еӨұеҺ»ж Үзӯҫзҡ„жә¶ж¶ІпјҢдёҖ瓶жҳҜзЁҖзӣҗй…ёпјҢеҸҰдёҖ瓶жҳҜж°ўж°§еҢ–й’ жә¶ж¶ІпјҢдёӢеҲ—иҜ•еүӮдёӯдёҚиғҪе°Ҷе®ғ们йүҙеҲ«еҮәжқҘзҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺй…ҡй…һиҜ•ж¶І BпјҺй•ҒжқЎ CпјҺж°ҜеҢ–й’ҫжә¶ж¶ІВ В DпјҺж°ҜеҢ–й“ңжә¶ж¶І
|
|
| 20. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҗ„з»„зү©иҙЁзҡ„жә¶ж¶Іж··еҗҲеҗҺпјҢдёҚиғҪеҸ‘з”ҹеҸҚеә”зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺNaClе’ҢH2SO4В BпјҺNaOHе’ҢHCl CпјҺNa2CO3е’ҢH2SO4 DпјҺAgNO3е’ҢNaCl
|
|
| 21. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еә”з”ЁеҸҠзӣёеә”еҺҹзҗҶпјҲз”ЁеҢ–еӯҰж–№зЁӢејҸиЎЁзӨәпјүйғҪжӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺз”ЁзЁҖзӣҗй…ёйҷӨеҺ»й”ҲВ Fe2O3+6HClв•җ2FeCl2+3H2O BпјҺз”ЁдәҢж°§еҢ–зўіеҲ¶зўій…ёйҘ®ж–ҷВ CO2+H2Oв•җH2CO3 CпјҺз”Ёз”өи§Јж°ҙзҡ„ж–№жі•жөӢе®ҡж°ҙзҡ„з»„жҲҗВ 2H2Oв•җ2H2вҶ‘+O2вҶ‘ DпјҺз”Ёж°ўж°§еҢ–й’ еҲ¶зўій…ёй’ В Na2CO3+CaпјҲOHпјү2в•җCaCO3вҶ“+2NaOH
|
|
| 22. | иҜҰз»ҶдҝЎжҒҜ |
|
иӢҘе°Ҷжө“зӣҗй…ёе’Ңжө“зЎ«й…ёж•һеҸЈж”ҫзҪ®еңЁз©әж°”дёӯпјҢдёҖж®өж—¶й—ҙеҗҺпјҢеҸҜд»ҘиӮҜе®ҡзҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺжә¶иҙЁзҡ„иҙЁйҮҸеҲҶж•°йғҪеҮҸе°Ҹ BпјҺжә¶еүӮиҙЁйҮҸйғҪеўһеӨ§ CпјҺжә¶ж¶ІиҙЁйҮҸйғҪеўһеӨ§В В DпјҺжә¶иҙЁиҙЁйҮҸйғҪеҮҸе°‘
|
|
| 23. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—жңүе…ізү©иҙЁзҡ„еҢ–еӯҰејҸгҖҒеҗҚз§°гҖҒдҝ—еҗҚдёҚе®Ңе…ЁеҜ№еә”зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺNaOHВ В В В ж°ўж°§еҢ–й’ В зғ§зўұВ BпјҺCaOВ В В ж°ўж°§еҢ–й’ҷВ В з”ҹзҹізҒ° CпјҺNa2CO3В В В зўій…ёй’ В В В зәҜзўұВ DпјҺNaClВ В ж°ҜеҢ–й’ В В В В йЈҹзӣҗ
|
|
| 24. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҜ№е®һйӘҢж„ҸеӨ–дәӢж•…зҡ„еӨ„зҗҶй”ҷиҜҜзҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺиӢҘдёҚж…Һе°ҶзҮғзқҖзҡ„й…’зІҫзҒҜзў°еҖ’пјҢжҙ’еҮәзҡ„й…’зІҫеңЁжЎҢдёҠзҮғзғ§пјҢеә”з«ӢеҲ»з”Ёж№ҝжҠ№еёғжү‘зӣ– BпјҺиӢҘдёҚж…Һе°Ҷзғ§зўұжә¶ж¶ІжІҫеҲ°зҡ®иӮӨдёҠпјҢиҰҒз”ЁиҫғеӨҡзҡ„ж°ҙеҶІжҙ—пјҢеҶҚж¶ӮдёҠзЎјй…ёжә¶ж¶І CпјҺиӢҘдёҚж…Һе°Ҷи…җиҡҖжҖ§иҚҜж¶Іжә…е…ҘзңјзқӣпјҢиҰҒе…Ҳз”ЁжүӢжҸүзңјзқӣпјҢеҶҚз«ӢеҚіз”Ёж°ҙеҶІжҙ— DпјҺиӢҘдёҚж…Һе°Ҷжө“зЎ«й…ёжІҫеҲ°зҡ®иӮӨжҲ–иЎЈжңҚдёҠпјҢеә”з«ӢеҚіз”ЁеӨ§йҮҸж°ҙеҶІжҙ—пјҢ然еҗҺж¶ӮдёҠ3%пҪһ5%зҡ„зўій…ёж°ўй’ жә¶ж¶І
|
|
| 25. | иҜҰз»ҶдҝЎжҒҜ |
|
зү©иҙЁзҡ„жҖ§иҙЁеҶіе®ҡе…¶з”ЁйҖ”пјҺдёӢеҲ—жңүе…ізү©иҙЁз”ЁйҖ”зҡ„иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺзғ§зўұз”ЁдәҺжІ»з–—иғғй…ёиҝҮеӨҡ BпјҺзўій…ёй’ҷз”ЁдҪңз„ҷеҲ¶зі•зӮ№зҡ„еҸ‘й…өзІү CпјҺз”ЁдәҡзЎқй…ёй’ жӣҝд»ЈйЈҹзӣҗзғ№и°ғйЈҹзү© DпјҺзҶҹзҹізҒ°з”ЁдәҺж”№иүҜй…ёжҖ§еңҹеЈӨ
|
|
| 26. | иҜҰз»ҶдҝЎжҒҜ |
|
пјҲ1пјүз”ЁдёӢеҲ—еӣӣз§Қе…ғзҙ пјҲOгҖҒHгҖҒCuгҖҒSпјүеҶҷеҢ–еӯҰејҸпјҡ й…ёгҖҖгҖҖпјӣзўұгҖҖгҖҖпјҢйқһйҮ‘еұһж°§еҢ–зү©гҖҖгҖҖ пјҲ2пјүдёҠиҝ°й…ёдёҺзўұеҸ‘з”ҹеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸпјҡгҖҖгҖҖпјҺ
|
|
| 27. | иҜҰз»ҶдҝЎжҒҜ |
|
жҢүиҰҒжұӮеЎ«еҶҷдёӢеҲ—еҶ…е®№пјҡ 2дёӘж°ўж°§ж №зҰ»еӯҗгҖҖгҖҖгҖҒ2дёӘж°ҜзҰ»еӯҗгҖҖгҖҖгҖҒ2дёӘзЎ«й…ёж №зҰ»еӯҗгҖҖгҖҖгҖҒ2дёӘй“өж №зҰ»еӯҗгҖҖгҖҖпјҺ
|
|
| 28. | иҜҰз»ҶдҝЎжҒҜ |
|
пјҲ1пјүеҗ‘зӣӣжңүж°ўж°§еҢ–й’ жә¶ж¶Ізҡ„й”ҘеҪўз“¶йҮҢж»ҙе…ҘеҮ ж»ҙй…ҡй…һжә¶ж¶ІпјҢжә¶ж¶ІеҸҳжҲҗгҖҖгҖҖиүІпјҢpHгҖҖгҖҖ7пјҲеЎ«вҖңпјһвҖқгҖҒвҖңпјңвҖқжҲ–вҖң=вҖқпјүпјҢйҖҗж»ҙеҗ‘й”ҘеҪўз“¶дёӯж»ҙе…Ҙзӣҗ酸并жҢҜиҚЎпјҢи§ӮеҜҹеҲ°зҡ„зҺ°иұЎжҳҜгҖҖгҖҖпјҢжә¶ж¶Ізҡ„pHгҖҖгҖҖпјҲеЎ«вҖңеўһеӨ§вҖқжҲ–вҖңеҮҸе°ҸвҖқпјүпјҺ пјҲ2пјүжңүдёҖ瓶жә¶ж¶ІpHжҳҜ4.5пјҢеҰӮжһңиҰҒдҪҝжә¶ж¶Ізҡ„pHеҚҮй«ҳпјҢеҸҜд»Ҙз”ЁгҖҖгҖҖзҡ„ж–№жі•пјҺ
|
|
| 29. | иҜҰз»ҶдҝЎжҒҜ |
|
й“Ғй”Ҳзҡ„дё»иҰҒжҲҗеҲҶжҳҜпјҲеЎ«еҢ–еӯҰејҸпјүгҖҖгҖҖпјҢе°ҶдёҖжһҡз”ҹй”Ҳзҡ„й“Ғй’үж”ҫе…Ҙи¶ійҮҸзҡ„зЁҖзӣҗй…ёдёӯпјҢдҪ йҰ–е…Ҳи§ӮеҜҹеҲ°зҡ„зҺ°иұЎжҳҜгҖҖгҖҖпјҢеҢ–еӯҰж–№зЁӢејҸдёәгҖҖгҖҖпјҢиҝҮдёҖдјҡе„ҝпјҢдҪ иҝҳеҸҜд»Ҙи§ӮеҜҹеҲ°зҡ„зҺ°иұЎжҳҜгҖҖгҖҖпјҢиҜ·еҶҷеҮәжңүе…іеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸгҖҖгҖҖпјҺ
|
|
| 30. | иҜҰз»ҶдҝЎжҒҜ |
|
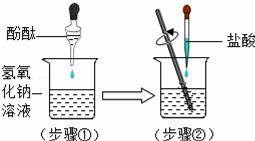
жҹҗе…ҙи¶Је°Ҹз»„з”ЁеӣҫзӨәиЈ…зҪ®еҒҡй…ёзўұдёӯе’ҢеҸҚеә”е®һйӘҢпјҢиҜ•еӣһзӯ”пјҡ пјҲ1пјүз”Ёиғ¶еӨҙж»ҙз®ЎеҗёеҸ–зӣҗй…ёйҖҗж»ҙеҠ е…Ҙзғ§жқҜдёӯпјҢеҪ“жә¶ж¶ІеҲҡеҘҪз”ұгҖҖгҖҖиүІеҸҳжҲҗгҖҖгҖҖиүІпјҢеҒңжӯўеҠ е…Ҙзӣҗй…ёпјҺеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸдёәпјҡгҖҖгҖҖпјҺ пјҲ2пјүе®һйӘҢ пјҲ1пјүдёӯпјҢжҹҗеҗҢеӯҰдёҚе°ҸеҝғеҸҲеӨҡеҠ дәҶеҮ ж»ҙзӣҗй…ёпјҢиҝҷж—¶жә¶ж¶Ізҡ„pHгҖҖгҖҖ7пјҺ пјҲ3пјүиӢҘиҰҒйҷӨеҺ»е®һйӘҢдёӯиҝҮйҮҸзҡ„зӣҗй…ёеҸҜйҖүз”Ёзҡ„зү©иҙЁжҳҜгҖҖгҖҖпјҲеЎ«еҢ–еӯҰејҸпјүпјҺ
|
|
| 31. | иҜҰз»ҶдҝЎжҒҜ |
|
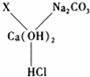
е°Ҹж”ҝеҗҢеӯҰеңЁеӨҚд№ CaпјҲOHпјү2еҢ–еӯҰжҖ§иҙЁж—¶пјҢеҪ’зәіеҮәдәҶCaпјҲOHпјү2дёҺе…¶е®ғзү©иҙЁй—ҙзӣёдә’еҸҚеә”зҡ„е…ізі»еҰӮеӣҫпјҲеӣҫдёӯвҖңп№Јп№ЈвҖқиЎЁзӨәзӣёиҝһзҡ„дёӨз§Қзү©иҙЁиғҪеҸ‘з”ҹеҸҚеә”пјүпјҺ пјҲ1пјүиӢҘXжҳҜдёҺе…¶е®ғдёүз§ҚдёҚеҗҢзұ»еҲ«зҡ„еҢ–еҗҲзү©пјҢеҲҷXеҸҜд»ҘжҳҜгҖҖгҖҖпјҺ пјҲ2пјүж №жҚ®еӣҫжүҖзӨәзҡ„зү©иҙЁй—ҙе…ізі»пјҢеҶҷеҮәе…¶дёӯдёӨдёӘеҢ–еӯҰж–№зЁӢејҸпјҡ в‘ гҖҖгҖҖпјӣВ В В В В В В в‘ЎгҖҖгҖҖпјҺ
|
|
| 32. | иҜҰз»ҶдҝЎжҒҜ |
|
зҺ°жңүзӣҗй…ёгҖҒж°ўж°§еҢ–й’ гҖҒж°ўж°§еҢ–й’ҷдёү瓶йҒ—еӨұж Үзӯҫзҡ„жә¶ж¶ІпјҢдёәдәҶйүҙеҲ«иҝҷдәӣжә¶ж¶ІпјҢе°Ҷе®ғ们编еҸ·дёәAгҖҒBгҖҒCпјҢ并жҢүдёӢеӣҫжӯҘйӘӨиҝӣиЎҢе®һйӘҢпјҢи§ӮеҜҹеҲ°д»ҘдёӢзҺ°иұЎпјҡ
пјҲ1пјүеҶҷеҮәиҜ•еүӮзҡ„еҗҚз§°в‘ жҳҜгҖҖгҖҖпјӣв‘ЎжҳҜгҖҖгҖҖпјҺ пјҲ2пјүеҶҷеҮәдёүз§Қжә¶ж¶Ізҡ„еҢ–еӯҰејҸпјҡAгҖҖгҖҖгҖҒBгҖҖгҖҖгҖҒCгҖҖгҖҖпјҺ пјҲ3пјүеҶҷеҮәз”ҹжҲҗзҷҪиүІжІүж·Җзҡ„еҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸгҖҖгҖҖпјҺ пјҲ4пјүеҶҷеҮәAдёҺBеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸпјҡгҖҖгҖҖпјҺ пјҲ5пјүжң¬е®һйӘҢеҰӮжһңе°ҶжӯҘйӘӨв‘ дёҺжӯҘйӘӨв‘Ўйў еҖ’пјҢиғҪеҗҰиҫҫеҲ°е®һйӘҢзӣ®зҡ„пјҹгҖҖгҖҖпјҺ
|
|
| 33. | иҜҰз»ҶдҝЎжҒҜ |
|
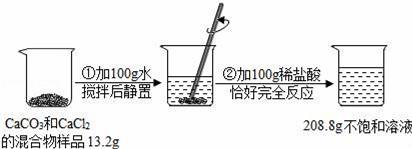
иҜ·ж №жҚ®еҰӮеӣҫжүҖзӨәзҡ„е®һйӘҢиҝҮзЁӢе’ҢжҸҗдҫӣзҡ„ж•°жҚ®пјҢиҜ•еӣһзӯ”дёӢеҲ—й—®йўҳпјҡ
пјҲ1пјүеңЁз¬¬в‘ЎжӯҘе®һйӘҢж“ҚдҪңдёӯпјҢи§ӮеҜҹеҲ°зҡ„дёҖйЎ№е®һйӘҢзҺ°иұЎжҳҜпјҡгҖҖгҖҖпјҺ пјҲ2пјү第①жӯҘе®һйӘҢж“ҚдҪңеҗҺпјҢзғ§жқҜдёӯжә¶ж¶ІйҮҢеҗ«жңүзҡ„жә¶иҙЁжҳҜпјҲеҶҷеҢ–еӯҰејҸпјүгҖҖгҖҖпјҺ пјҲ3пјүи®Ўз®—еҺҹж··еҗҲзү©ж ·е“ҒдёӯCaCl2зҡ„иҙЁйҮҸпјҲеҶҷеҮәи®Ўз®—иҝҮзЁӢпјҢз»“жһңзІҫзЎ®иҮі0.1gпјүпјҺ
|
|
- ж№–еҚ—зңҒж°ёе·һеёӮ2021е№ҙдёӯиҖғеҢ–еӯҰйўҳеҗҢжӯҘи®ӯз»ғе…Қиҙ№иҜ•еҚ·
- 2019е№ҙе№ҝдёңзңҒж·ұеңіеёӮзҰҸз”°еҢәдёӯиҖғдёҖжЁЎеҢ–еӯҰйўҳе…Қиҙ№иҜ•еҚ·
- 2019еұҠеҲқдёүдёҠеҶҢжңҹжң«иҖғиҜ•еҢ–еӯҰйўҳејҖеҚ·жңүзӣҠпјҲеҶ…и’ҷеҸӨиҮӘжІ»еҢәе·ҙеҪҰж·–е°”еёӮд№ҢжӢүзү№еүҚж——пјү
- д№қе№ҙзә§еҢ–еӯҰ2019е№ҙдёҠеҚҠжңҹиҜҫж—¶з»ғд№ еңЁзәҝзӯ”йўҳ
- ж№–еҢ—зңҒжҒ©ж–ҪеёӮзҷҪжқЁеқӘй•ҮеҲқзә§дёӯеӯҰ2020-2021е№ҙеҲқдёүдёҠжңҹжңҹжң«еҢ–еӯҰйўҳе…Қиҙ№иҜ•еҚ·еңЁзәҝжЈҖжөӢ
- жү¬е·һеёӮ2020е№ҙд№қе№ҙзә§еҢ–еӯҰеҗҺеҚҠжңҹжңҲиҖғжөӢйӘҢеёҰзӯ”жЎҲдёҺи§Јжһҗ
- еӣӣе·қзңҒеҮүеұұе·һ2020е№ҙдёӯиҖғеҢ–еӯҰйўҳеёҰзӯ”жЎҲе’Ңи§Јжһҗ
- 2019еұҠд№қе№ҙзә§дёӢеӯҰжңҹдёӯиҖғдёҖжЁЎеҢ–еӯҰиҖғиҜ•пјҲеҗүжһ—зңҒй•ҝжҳҘеёӮдёңеҢ—еёҲеӨ§йҷ„еұһдёӯеӯҰпјү
 В BпјҺ
В BпјҺ