2015-2016学年湖南省衡阳市耒阳市冠湘学校九年级(下)第二次段考化学试卷带解析
| 1. | 详细信息 |
|
下列属于化学变化的是( ) A.滴水成冰 B.蜡烛成灰 C.木已成舟 D.铁杵成针
|
|
| 2. | 详细信息 |
|
下列基本实验操作的图示不正确的是( ) A. 检查装置气密性 B. C. 稀释浓硫酸 D. 过滤
|
|
| 3. | 详细信息 |
|
健康饮食均衡营养是青少年健康成长的重要保证.下列物质中富含维生素的是( ) A.大豆和花生 B.瘦肉和鸡蛋 C.蔬菜和水果 D.米饭和馒头
|
|
| 4. | 详细信息 |
|
下列有关实验现象描述正确的是( ) A.细铁丝在空气中剧烈燃烧,火星四射,生成红色物质 B.硫在空气中燃烧发出蓝紫色火焰,生成无色无味的气体 C.在碳酸钠溶液中加入无色酚酞溶液,溶液变红色 D.将光亮的铜丝插入稀硫酸中,溶液由无色变为蓝色
|
|
| 5. | 详细信息 |
|
下列关于物质的性质和用途说法正错误的是( ) A.石墨有滑腻感,可以做电极 B.氮气化学性质不活泼,可用于食品防腐 C.活性炭有吸附性,可吸附异味 D.金刚石的硬度大,可切割玻璃
|
|
| 6. | 详细信息 |
|
下列关于微观粒子的说法正确的是( ) A.物质是分子或原子构成的 B.分子和原子都在不停地运动 C.吹胀气球时分子间的间隔变大 D.分子和原子在化学变化中都可再分
|
|
| 7. | 详细信息 |
|
水是生命之源,下列有关水的说法正确的是( ) A.水是由氢气和氧气组成的混合物 B.天然水中硬水属于混合物,软水属于纯净物 C.长期饮用蒸馏水不利于身体健康 D.自来水厂净水过程包括:沉淀、吸附、蒸馏
|
|
| 8. | 详细信息 |
|
下列灭火方法不合理的是( ) A.酒精洒在桌面上燃烧,立即用湿抹布扑灭 B.油锅着火,泼水灭火 C.森林发生火灾,砍掉部分树木,形成隔离带 D.纸箱着火,用水浇灭
|
|
| 9. | 详细信息 |
|
分析推理是化学学习中常用的思维方法.下列分析推理正确的是( ) A.浓硫酸具有吸水性,所以浓盐酸也具有吸水性 B.O2和O3的分子构成不同,所以它们的化学性质不同 C.离子是带电荷的微粒,所以带电荷的微粒一定是离子 D.酸雨的pH小于7,所以pH小于7的雨水一定是酸雨
|
|
| 10. | 详细信息 |
|
化学反应前后,下列各项中肯定没有变化的是:①原子的数目 ②分子的数目 ③元素的种类 ④物质的总质量 ⑤物质的种类 ⑥原子的种类( ) A.①③④⑤⑥ B.①③④⑥ C.①②④⑥ D.①③⑤
|
|
| 11. | 详细信息 |
|
”塑化剂”的主要成分是邻苯二甲酸二辛酯,其化学式为C24H38O4,下列说法错误的是( ) A.它是一种有机物 B.邻苯二甲酸二辛酯是由碳原子、氢原子、氧原子构成 C.它是由碳、氢、氧三种元素组成 D.一个邻苯二甲酸二辛酯分子中含66个原子
|
|
| 12. | 详细信息 |
|
三月中旬,湖南媒体报道,不法商贩用具有漂白防腐作用的焦亚硫酸钠(化学式为Na2S2O5)处理生姜,使生姜变得又黄又亮,从而谋取利益.过量的焦亚硫酸钠会严重危害人体健康.Na2S2O5中硫元素的化合价为( ) A.﹣2 B.+2 C.+4 D.+6
|
|
| 13. | 详细信息 |
|
对下列有水生成的四个化学方程式的反应类型,判断不正确的是( ) ①2H2+O2 ③H2+CuO A.①是化合反应 B.②是分解反应 C.③是置换反应 D.④是复分解反应
|
|
| 14. | 详细信息 |
|
黑火药的主要成分是硝酸钾、木炭粉、硫磺粉等,点燃时发生爆炸的化学方程式为:2KNO3+S+3C A.N2 B.NO2 C.NO D.N2O
|
|
| 15. | 详细信息 |
|
下列有关溶液的说法,正确的是( ) A.溶液都是无色的 B.溶液中溶质不一定只有一种,但溶剂只有一种 C.形成溶液的溶质都是固体 D.饱和溶液就是浓溶液
|
|
| 16. | 详细信息 |
|
在一定条件下,一氧化碳、木炭都能与氧化铜发生发应,下列叙述正确的是( ) A.反应产生的气体都有毒 B.反应中都有红色固体生成 C.反应类型都是置换反应 D.反应的生成物不同
|
|
| 17. | 详细信息 |
|
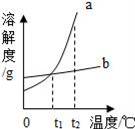
a,b两种物质的溶解度曲线如图所示.下列说法不正确的是( )
A.将t1℃时b的饱和溶液加水可变为不饱和溶液 B.将t2℃时a的饱和溶液降温至t1℃,溶液质量不变 C.t2℃时,两种物质的饱和溶液中溶质质量分数a>b D.将t2℃时a、b的饱和溶液分别降温至t1℃,两溶液的溶质质量分数相等
|
|
| 18. | 详细信息 |
|
下列物质的除杂(括号中是杂质),所用的试剂或方法正确的是( ) A.CO2(CO):点燃 B.Fe(Cu):加硫酸铜溶液 C.NaCl(Na2 CO3):加适量稀盐酸 D.CaCO3(CaO):加足量稀盐酸
|
|
| 19. | 详细信息 |
|
鉴别物质是化学知识的一项重要应用,下列各组溶液,加入括号中的试剂后,不能鉴别出的是( ) A.K2SO4和BaCl2:(Na2CO3 ) B.HNO3和Na2CO3:( HCl ) C.CuCl2和K2SO4:(NaOH ) D.AgNO3和KCl:(K NO3)
|
|
| 20. | 详细信息 |
|
有甲、乙、丙、丁四种金属,将它们分别投入到相同的稀盐酸中,只有丙、丁的表面有气泡产生,且丙产生的气泡比丁快;再将乙投入到甲的盐酸液中,乙的表面有甲析出.则四种金属的活动性顺序正确的是( ) A.甲>乙>丙>丁 B.丙>丁>乙>甲 C.丙>丁>甲>乙 D.无法判断
|
|
| 21. | 详细信息 |
|
质量守恒定律是帮助我们认识化学反应实质的重要理论,在化学反应aA+bB═cC+dD 中,下列说法正确的是( ) A.化学计量数a与b之和一定等于c与d之和 B.反应物A与B的质量比一定等于C与D是质量比 C.若A和C都是盐,则一定是复分解反应 D.若xgA与xgB反应生成C与D的质量之和不一定等于2xg
|
|
| 22. | 详细信息 |
|
生活中的下列物品,主要材料属于合成材料的是( ) A.全棉毛巾 B.塑料袋 C.不锈钢盆 D.青花瓷瓶
|
|
| 23. | 详细信息 |
|
为了让天更蓝、地更绿、水更淸,下列建议不可行的是( ) A.严禁随意焚烧秸秆,以减少PM2.5的排放 B.大力开发和使用风能、太阳能,减少使用化石燃料 C.禁止使用化肥农药,以防止水体污染 D.分类回收垃圾.以促进资源再生和利用
|
|
| 24. | 详细信息 |
|
(1)水是生命之源,请写出水电解的化学方程式: ,其产物中最理想的燃料是 ,理由是 . (2)实验室制取氢气的化学方程式是: ,请你写一条“H2”表示的意义: .
|
|
| 25. | 详细信息 |
|
请写出相应的化学符号. (1)氯酸钾 ; (2)两个甲烷分子 ; (3)3个铁原子 ; (4)4个铵根离子 ; (5)氧化铁中,铁元素的化合价为+3 .
|
|
| 26. | 详细信息 |
|
现有六种物质:A.磁铁矿石 B.氧化钙 C.氢氧化铝 D.熟石灰 E.酒精 F.食盐(填序号) (1) 可用作厨房调味剂; (2) 可用于冶金; (3) 是实验室常用的燃料; (4) 可用治疗胃酸过多. (5) 可用作食品干燥剂.
|
|
| 27. | 详细信息 |
|
(1)某同学没吃早餐就来参加考试,出现乏力、疲倦甚至昏迷等症状,他缺少的营养素是 . (2)化学元素对人体健康有重要的影响.人体缺铁会引起 ,为了全民的健康,我推广使用强化铁酱油,这里的“铁”是指 (填“单质”“元素”或“原子”),此外,缺 易患坏血病.
|
|
| 28. | 详细信息 |
|
如图中A、B、C、D是四种粒子的结构示意图.请回答下列问题:
(1)A中x= ;A粒子的化学式是 . (2)由B粒子的结构示意图可知,B粒子的名称是 . (3)以上四种结构示意图所表示的粒子中,表示离子的是 A(填字母代号).
|
|
| 29. | 详细信息 |
|
1)工业上炼铁用一氧化碳还原氧化铁的化学方程式: . (2)过多的CO2会引起温室效应,绿色植物的 能吸收二氧化碳;科学家发现,以CO2和NH3为原料在高温高压条件下可以合成尿素[化学式是CO(NH2)2],同时会生成水,请写出该反应的化学方程式: .请你提出一条合理的建议以减缓温室效应: .
|
|
| 30. | 详细信息 |
|
某中学化学兴趣小组在老师的指导下,实验员提供了如下器材和若干化学药品,进行气体的制备和性质的探究,邀请你一同参加.
(1)写出图中标号a仪器的主要用途 . (2)实验室制取少量氢气,且操作相对简易时,发生装置最好选用 (填字母),组装好仪器后,应先 ,再添加药品. (3)实验室常用过氧化氢溶液制取氧气,该反应的化学方程式是 ,实验室若要制取干燥的氧气,收集氧气前先将气体通过H装置,H装置中的X是 (填“浓盐酸”“浓硫酸”或“氢氧化钠溶液”),其理由是 ,气体通过H时应从 (填“b”或“c”)端进入.
|
|
| 31. | 详细信息 |
|
在浓硫酸的催化作用下,固体草酸(H2C2O4)受热分解生成碳的氧化物和水.某化学课外兴趣小组对生成物中碳的氧化物种类进行了如下实验探究: 【提出问题】生成物中有哪几种碳的氧化物? 【实验猜想】猜想1:只有CO; 猜想2:只有 ; 猜想3:含有CO和CO2. 【设计实验】基于猜想3,依据CO和CO2的性质,兴趣小组同学设计了如下实验:
【实验探究】 (1)观察到 (填字母)装置中的澄清石灰水变浑浊,证明草酸分解有CO2气体生成. (2)有两种实验现象都能分别证明草酸分解的气体中含有CO: ①C装置中澄清石灰水不变浑浊,F装置中 ; ②E装置中出现 的现象. 【实验结论】通过实验探究证明:猜想3成立. 草酸分解的化学方程式是 . 【问题讨论】 (1)B装置的作用是 ; (2)D装置的作用是 ; (3)装置末端酒精灯的作用是 .
|
|
| 32. | 详细信息 |
|
日常使用的金属材料大多属于合金,黄铜是以锌作为添加元素的铜合金.制造弹壳的黄铜中只含有锌和铜.现将22g弹壳放在盛有100g稀硫酸的烧杯中(硫酸足量),当弹壳不再溶解后,烧杯中混合物的质量是121.8g,计算(请在答题卡相应位置写出计算过程,计算结果保留一位小数): (1)反应中产生的氢气的质量. (2)弹壳中铜的质量为. (3)反应后所得溶液中硫酸锌的质量分数.
|
|