2016河南高三下学期人教版高中化学月考试卷
| 1. | 详细信息 |
|
下列物质的水溶液能导电,但属于非电解质的是 ( ) A.CH3CH2COOH B.Cl2 C.NH4HCO3 D.SO2 |
|
| 2. | 详细信息 | ||||||||
|
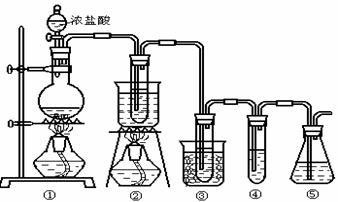
在实验室中可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。 图中: ①为氯气发生装置;②的试管里盛有15mL 30% KOH 溶液.并置于热水浴中; ③的试管里盛有15mL 8 % NaOH 溶液.并置于冰水浴中; ④的试管里加有紫色石蕊试液; ⑤为尾气吸收装置。
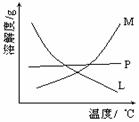
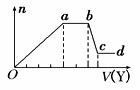
请填写下列空白: (1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过______(填写仪器名称)向烧瓶中加入适量的浓盐酸。实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有_________(填写下列编号字母)的净化装置。 A.碱石灰 B.饱和食盐水 C.浓硫酸 D.饱和碳酸氢钠溶液 (2)比较制取氯酸钾和次氯酸钠的条件.二者的差异是 。反应完毕经冷却后,②的试管中有大量晶体析出。下图中符合该晶体溶解度曲线的是_______(填写编号字母);从②的试管中分离出该晶体的方法是 (填写实验操作名称)。
(3)本实验中制取次氯酸钠的离子方程式是: 。 (4)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白:
|
|||||||||
| 3. | 详细信息 | ||||||||||||||||||||||||||
|
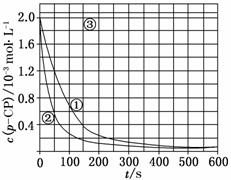
Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响。 [实验设计] 控制p-CP的初始浓度相同,恒定实验温度在298 K或313 K(其余实验条件见下表),设计如下对比实验。 (1)请完成以下实验设计表(表中不要留空格)。
[数据处理] 实验测得p-CP的浓度随时间变化的关系如上图。 (2)请根据上图实验①曲线,计算降解反应50~150 s内的反应速率: v(p-CP)=________mol·L-1·s-1。 [解释与结论] (3)实验①、②表明温度升高,降解反应速率增大。但温度过高时反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因:_____________________________ (4)实验③得出的结论是:pH等于10时,________。 [思考与交流] (5)实验时需在不同时间从反应器中取样,并使所取样品中的反应立即停止下来。根据上图中的信息,给出一种迅速停止反应的方法:________。 |
|||||||||||||||||||||||||||
| 4. | 详细信息 |
|
孔雀石主要成分是Cu2(OH)2CO3,还含少量难溶的FeCO3及Si的化合物,实验室以孔雀石为原料制备硫酸铜晶体的步骤如下:
(1)步骤Ⅰ中涉及的反应用离子方程式表示为_____________________________。 (2)为将溶液中Fe2+氧化成Fe3+步骤Ⅱ中加入的试剂①最好是__________(填代号)。 a.KMnO4 b.H2O2 c.Fe粉 d.KSCN (3)步骤Ⅳ获得硫酸铜晶体,需要经过_________、_________、过滤等操作。 (4)孔雀石与焦炭一起加热可以生成Cu及其它无毒物质,写出该反应的化学方程式_____________。 (5)测定硫酸铜晶体(CuSO4·xH2O)中结晶水的x值:称取2.5g硫酸铜晶体,加热至质量不再改变时,称量粉末的质量为1.6g。则计算得x=______ |
|
| 5. | 详细信息 |
|
为了确定某物质是否变质,所选试剂(括号内物质)达不到实验要求的是( ) A.氢氧化钠是否变质(BaC12) B.FeSO4是否被氧化(KSCN) C.KI是否被氧化(淀粉溶液) D.K2SO3是否被氧化(BaC12) |
|
| 6. | 详细信息 |
|
下列各组物质中,分子数相同的是( ) A.2L SO2和2L CO2 B. 标准状况下1mol氧气和22.4L水 C. 9g水和标准状况下11.2L CO2 D.0.2molH2S和2.24LHCl |
|
| 7. | 详细信息 |
|
下面的能级表示中正确的是 A.1p B.2d C.3f D.4 s |
|
| 8. | 详细信息 |
|
氧气的摩尔质量为32.0 g·mol-1,由此求出的标准状况下氧气的密度可能是( ) A.1.5 g·L-1 B.1.43 g·L-1 C.1.293 g·L-1 D.1.2 mg·L-1 |
|
| 9. | 详细信息 |
|
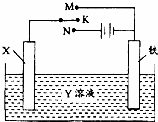
利用图装置,可以完成很多电化实验。下列有关此装置的叙述中,不正确的是( )
A.若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阳极的阴极保护法 B.若X为碳棒,Y为NaCl溶液,开关K置于N处,可减缓铁的腐蚀,溶液中的阳离子向铁电极移动 C.若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动 D.若X为铜棒,Y为硫酸铜溶液,开关K置于N处,铁棒质量将增加,溶液中铜离子浓度将减小 |
|
| 10. | 详细信息 |
|
下列说法中正确的是( ) A.在Na2CO3溶液中滴入酚酞试液,呈红色 B.(NH4)2SO4溶液中c(NH C.FeCl3溶于水使溶液呈酸性,从而抑制水的电离 D.将Al2(SO4)3溶液蒸干得到Al(OH)3固体 |
|
| 11. | 详细信息 |
|
下列说法不正确的是 A.用四氯化碳可以萃取乙酸水溶液中的乙酸 B.元素分析可以鉴定有机物的实验式 C.红外光谱分析可以鉴定有机物中含有的官能团或化学键 D.核磁共振氢谱分析可以鉴定有机物中不同化学环境的氢原子及它们的数目比 |
|
| 12. | 详细信息 |
|
含溶质24g 的3mol·L-1NaOH溶液,现欲配制成1mol·L-1NaOH溶液,应取原溶液与蒸馏水的体积比约为 A.1∶2 B.1∶3 C.2∶1 D.2∶3 |
|
| 13. | 详细信息 |
|
下列与化学反应能量变化相关的叙述正确的是 A.生成物总能量一定低于反应物总能量 B.放热反应的反应速率总是大于吸热反应的反应速率 C.盖斯定律,可计算某些难以直接测量的反应的焓变 D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件的△H不同 |
|
| 14. | 详细信息 |
|
下列分子中的中心原子杂化轨道的类型相同的是 A.CO2与H2O B. BeCl2与BF3 C.CH4与NH3 D.C2H2与C2H4 |
|
| 15. | 详细信息 |
|
高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化性更强,无二次污染的绿色水处理剂。工业制高铁酸钠的方法有如下两种: ①湿法制备的主要反应方程式为:Fe(OH)3+ ClO—+ OH— → FeO42—+ Cl—+ H2O ②干法制备的主要反应方程式为: FeSO4+ Na2O2 → Na2FeO4+ Na2O+ Na2SO4 + O2↑ (均未配平) 下列有关说法不正确的是 A.高铁酸钠中铁显+6价 B.湿法制备的反应方程式中,氧化剂和还原剂的物质的量之比为3∶2 C.干法中每生成1 mol Na2FeO4转移4 mol电子 D.K2FeO4处理水时,不仅能消毒杀菌,还能除去水体中的H2S、NH3等,生成的Fe(OH)3还能吸附水中的悬浮杂质 |
|
| 16. | 详细信息 |
|
相同质量的C6H6、C7H8、C4H10、C3H6完全燃烧时,耗氧量最多的是 A.C6H6 B.C7H8 C.C4H10 D.C3H6 |
|
| 17. | 详细信息 |
|
研究课上,老师让同学们各自选题进行计算,其结果正确的是 A、甲同学:0.2 mol MgO,经计算,其质量为0.2 g B、乙同学:9.03×1023个O2,经计算,O2物质的量为1.5 mol C、丙同学:标准状况下,5.6 L 水的体积,经计算为 0.25 mol D、丁同学: 将30 mL0.5mol·L-1 NaOH溶液加水稀释到500mL,经计算,稀释后溶液中NaOH的物质的量浓度为0.04mol·L-1 |
|
| 18. | 详细信息 | ||||
|
某无色稀溶液X中,可能含有如表所列离子中的某几种。
取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(V)的关系如图所示 A.若Y是盐酸,则X中一定含有CO32-、SiO32-、AlO2-和Na+ B.若Y是NaOH溶液,则X中一定含有Al3+、Fe3+、NH4+、Cl- C.若Y是NaOH溶液,则ab段发生反应的离子方程式为:NH4++OH-=NH3↑+H2O D.若Y是NaOH溶液,则X中的Al3+、Mg2+、NH4+ 物质的量之比为1:1:2 |
|||||
| 19. | 详细信息 |
|
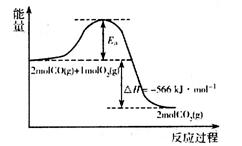
工业尾气SO2、NO2是污染大气、形成酸雨的罪魁祸首。请回答下列问题: (1)用CO可以消除SO2污染。已知一定条件下,2CO(g)+O2(g)==2CO2(g)的能量变化如图所示,由固体S单质生成l molSO2(g)的焓变为
在相同条件下,CO与SO2反应生成单质S与CO2的热化学方程式为______________。 (2)异氰酸(化学式:HNCO,C为+4价)可用于消除尾气中的NO2。其反应原理为: HNCO+NO2→N2+CO2+ ①上述反应的氧化剂是____________。 ②配平后方框内应填写____________。 ③每处理33.6LNO2(标准状况),反应中转移电子的物质的量为____________。 |
|
| 20. | 详细信息 |
|
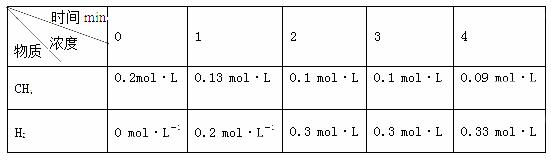
CO和H2的混合气体俗称合成气,是一种重要的工业原料气,工业上利用天然气(主要成分为CH4)与水进行高温重整制备合成气。 CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.1KJ/mol (1)在一定温度下,向体积为2L的密闭容器中充入0.40mol CH4和0.60mol H2O(g),测得CH4(g)和H2(g)的物质的量浓度随时间变化如下表所示:
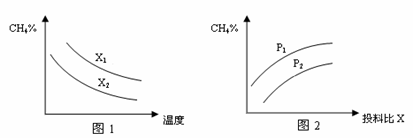
①计算该反应第一次达平衡时的平衡常数计算式K=_______ ②3min时改变的反应条件可能是________(只填一种条件的改变即可)。 (2)已知温度、压强、投料比X[n(CH4)/n(H2O)]对该反应的影响如图所示。
①图1中的两条曲线所示投料比的关系X1____X2(填“=”、“>”或“<”下同)。 ②图2中两条曲线所示的压强比的关系:P1____P2。 (3) 以天然气(设杂质不参与反应)、KOH溶液为原料可设计成燃料电池: ①放电时,负极的电极反应式为 _________________ ②设装置中盛有的 KOH溶液,在反应后恰好生成KHCO3溶液,则该溶液中各离子浓度由大到小的关系为________________ |
|
| 21. | 详细信息 |
|
按要求回答下列问题: (1)设NA为阿伏加德罗常数,一个Cl2分子的质量为 g;水煤气(CO 和H2的混合物)中含氢气的体积分数约为75%、CO的体积分数约为25%,则该水煤气的平均摩尔质量约为 。 (2)质量分数为29.8%的KCl溶液,其密度为1.15g/cm3,则500mL该溶液中KCl的物质的量为 。 |
|
| 22. | 详细信息 |
|
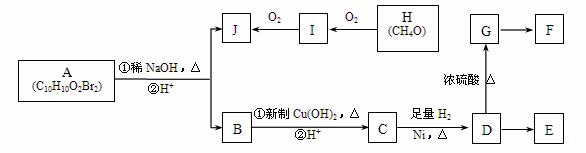
如下图转化关系能合成E、F两种有机高分子化合物,其中E为缩聚产物,F为加聚产物。A中含有苯环(苯环上的一硝基代物仅一种),A的核磁共振氢谱图中四个吸收峰的面积之比为1∶2∶6∶1;J能发生银镜反应;C中滴入浓溴水能产生白色沉淀;G能使溴的四氯化碳溶液褪色。
已知以下信息: a.在稀碱溶液中,溴苯难以发生水解反应; b.两个羟基同时连在同一碳原子上的结构是不稳定的,它将自动发生脱水反应, 如:CH3CH(OH)2→→CH3CHO + H2O。 回答下列问题: (1)I中官能团的名称为 。 (2)H的结构式为 。 (3)D→G的反应类型是 。 (4)1molB与足量Cu(OH)2反应可生成 gCu2O。 (5)F的结构简式为 。 (6)写出下列反应的方程式: ①A与足量稀NaOH溶液共热的离子方程式 。 ②D→E的化学方程式 。 (7)C的同系物中满足下列条件的同分异构体种类有 种(不考虑立体异构)。 ①分子式为C8H8O3 ②既含有酚羟基又含有羧基 |
|
| 23. | 详细信息 |
|
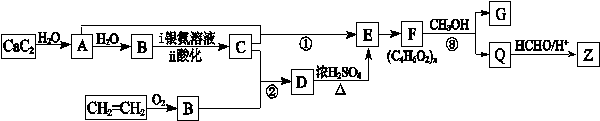
合成纤维Z的吸湿性接近于棉花。合成Z的流程图如下所示:
已知:下列反应中R、R′、R″代表烃基
(1)A的电子式为____________。 (2)E的名称为____________。 (3)反应①的化学方程式是____________。 (4)下列说法正确的是____________。 a.反应②的反应类型为加成反应 b.D能与Na、NaOH、NaHCO3反应 c.Q是一种水溶性很好的高分子化合物 d.G在酸性或碱性环境中均能水解 (5)E有多种同分异构体,与E具有相同官能团的有____________种(不含E),其中核磁共振氢谱显示有3种氢原子,且能发生银镜反应的结构简式是____________。 (6)合成纤维Z含有六元环状结构, Z的结构简式是___________。 |
|
| 24. | 详细信息 |
|
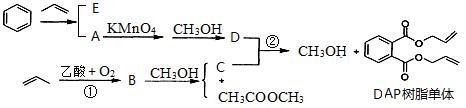
丙烯可用于合成应用广泛的DAP树脂单体。下列反应流程中的反应条件和少量副产物省略。
已知: RCOOR’+R’’OH→RCOOR’’+R’OH(R、R’、R’’代表烃基)
(1).DAP树脂单体的分子式为 。B中所含官能团的名称是 , B→C的反应类型 。 (2).E的相对分子质量为162,分子中有三种化学环境不同的氢。写出E的结构简式 。 (3).请写出反应②的化学方程式 。 (4).D有多种同分异构体,符合下列条件的同分异构体有 种。 A.能与NaOH溶液反应 B.苯环上只有两个相同的取代基,且苯环上的一氯代物有两种 (5).以丙烯为原料,其他无机试剂任选,写出制备硝化甘油的合理流程图,注明试剂条件。注:合成路线的书写格式参照如下实例流程图: CH3CHO |
|