2019еұұиҘҝй«ҳдёҖдёӢеӯҰжңҹдәәж•ҷзүҲ(2019)й«ҳдёӯеҢ–еӯҰжңҲиҖғиҜ•еҚ·
| 1. | иҜҰз»ҶдҝЎжҒҜ |
|
11HгҖҒ21HгҖҒ31HгҖҒH+гҖҒH2жҳҜпјҲгҖҖгҖҖпјү гҖҖВ В AпјҺж°ўзҡ„дә”з§ҚеҗҢдҪҚзҙ В В В В В В В В В В В В В В В В В В В В В В В BпјҺдә”з§Қж°ўе…ғзҙ В В В В В В гҖҖВ В CпјҺиҙЁеӯҗж•°йғҪзӣёеҗҢзҡ„зІ’еӯҗВ В В В В В В В В В В В В В В DпјҺж°ўе…ғзҙ зҡ„дә”з§ҚдёҚеҗҢзІ’еӯҗВ В
|
|
| 2. | иҜҰз»ҶдҝЎжҒҜ |
|
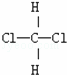
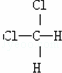
дёӢеҲ—иЎЁзӨәзү©иҙЁз»“жһ„зҡ„еҢ–еӯҰз”ЁиҜӯжӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү гҖҖВ В AпјҺд№ҷзғҜзҡ„з»“жһ„з®ҖејҸпјҡCH2CH2В В В В В В В В В В В В В В BпјҺNaClзҡ„з”өеӯҗејҸпјҡ гҖҖВ В CпјҺй•ҒзҰ»еӯҗзҡ„з»“жһ„зӨәж„Ҹеӣҫпјҡ
|
|
| 3. | иҜҰз»ҶдҝЎжҒҜ |
|
й’ҙеҲ¶жҳҜйқһеёёе№ҝжіӣзҡ„ж”ҫе°„жәҗпјҢеңЁеҢ»з–—дёҠеёёиӮәзҷҢе’ҢиӮҝзҳӨж”ҫе°„жІ»з–—пјҺжңүе…і гҖҖAпјҺиҙЁйҮҸж•°дёә27 В В В В BпјҺиҙЁеӯҗж•°дёә60 В В В В CпјҺдёӯеӯҗж•°дёә33В В В В В В В DпјҺж ёз”өиҚ·ж•°дёә33
|
|
| 4. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҢ–еӯҰејҸдёҺжҢҮе®ҡзү©иҙЁзҡ„дё»иҰҒжҲҗеҲҶеҜ№еә”жӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү гҖҖВ В AпјҺSiO2п№Јп№ЈеҲҡзҺүВ В В В В В В В В В В В В BпјҺCH4п№Јп№Јж°ҙз…Өж°” гҖҖВ В CпјҺNa2CO3п№Јп№Је°ҸиӢҸжү“ В В В В В В В В DпјҺNaOHп№Јп№Јзғ§зўұ
|
|
| 5. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—зү©иҙЁдә’дёәеҗҢеҲҶејӮжһ„дҪ“зҡ„дёҖз»„жҳҜпјҲгҖҖгҖҖпјү гҖҖВ В AпјҺCH3OCH3е’Ң CH3CH2OHВ В В В В BпјҺз”Ізғ·е’Ңд№ҷзғ· гҖҖВ В CпјҺ35ClдёҺ37ClВ В В В В В В В В В В В В В В В DпјҺзҷҪзЈ·е’ҢзәўзЈ·
|
|
| 6. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—е…ідәҺзғ·зғғзҡ„иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү гҖҖВ В AпјҺдёҷзғ·пјҲC3H8пјүеҸ‘з”ҹеҸ–д»ЈеҸҚеә”з”ҹжҲҗзҡ„C3H7Clзҡ„з»“жһ„еҸӘжңүдёҖз§Қ гҖҖВ В BпјҺдёҷзғ·еҲҶеӯҗдёӯдёүдёӘзўіеҺҹеӯҗеңЁдёҖжқЎзӣҙзәҝдёҠ гҖҖВ В CпјҺеҲҶеӯҗдёӯеҗ«жңүе…ӯдёӘзўіеҺҹеӯҗзҡ„зғ·зғғеңЁеёёжё©дёӢдёәж¶ІжҖҒзү©иҙЁ гҖҖВ В DпјҺзғ·зғғзҡ„еҲҶеӯҗдёәзӣҙй“ҫејҸз»“жһ„пјҢдёҚеҸҜд»ҘеёҰж”Ҝй“ҫ
|
|
| 7. | иҜҰз»ҶдҝЎжҒҜ |
|
з”ЁNAиЎЁзӨәйҳҝдјҸеҠ еҫ·зҪ—еёёж•°зҡ„еҖјпјҢдёӢеҲ—иҜҙжі•дёӯжӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү гҖҖВ В AпјҺ1molN2жүҖеҗ«жңүзҡ„еҺҹеӯҗж•°дёәNA гҖҖВ В BпјҺж ҮеҮҶзҠ¶еҶөдёӢпјҢ22.4Lж°ҙдёӯеҗ«жңүзҡ„ж°ҙеҲҶеӯҗж•°дёәNA гҖҖВ В CпјҺж ҮеҮҶзҠ¶еҶөдёӢпјҢ22.4Lж°ҜеҢ–ж°ўжүҖеҗ«зҡ„еҺҹеӯҗж•°дёәNA гҖҖВ В DпјҺ24gO2еҲҶеӯҗе’Ң24gO3еҲҶеӯҗжүҖеҗ«зҡ„ж°§еҺҹеӯҗж•°зӣ®зӣёзӯү
|
|
| 8. | иҜҰз»ҶдҝЎжҒҜ |
|
иӢҘиҰҒдҪҝ2mol CH4е®Ңе…Ёе’ҢCl2еҸ‘з”ҹеҸ–д»ЈеҸҚеә”пјҢдё”з”ҹжҲҗзҡ„еӣӣз§Қж°Ҝд»Јзү©зҡ„зү©иҙЁзҡ„йҮҸзӣёеҗҢпјҢеҲҷжүҖйңҖCl2зҡ„зү©иҙЁзҡ„йҮҸдёәпјҲгҖҖгҖҖпјү гҖҖВ В AпјҺ5molВ В В В В В BпјҺ4molВ В В В В В В В В CпјҺ3molВ В В В В В В В В DпјҺ2mol
|
|
| 9. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—зү©иҙЁдёӯпјҢдёҚеұһдәҺжңүжңәзү©зҡ„жҳҜпјҲгҖҖгҖҖпјү гҖҖВ В AпјҺе°ҝзҙ В В В В В В BпјҺй…’зІҫВ В В В В В В В В CпјҺиӢҸжү“В В В В В В В В В DпјҺеЎ‘ж–ҷ
|
|
| 10. | иҜҰз»ҶдҝЎжҒҜ |
|
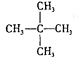
дёӢеҲ—еҗ„еҜ№зү©дҪ“дёӯеұһдәҺеҗҢеҲҶејӮжһ„дҪ“зҡ„жҳҜпјҲгҖҖгҖҖпјү гҖҖВ В AпјҺ126CдёҺ136CВ В В В В В В BпјҺO2дёҺO3гҖҖ CпјҺ
|
|
| 11. | иҜҰз»ҶдҝЎжҒҜ |
|
з¬ҰеҗҲдёӢеҲ—еҲҶеӯҗејҸзҡ„жңүжңәзү©жІЎжңүеҗҢеҲҶејӮжһ„зҺ°иұЎзҡ„жҳҜпјҲгҖҖгҖҖпјү гҖҖВ В AпјҺCH4В В В В В В В BпјҺC4H8В В В В В В В В В В CпјҺC4H10В В В В В В В В В DпјҺC5H12
|
|
| 12. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—жңүе…ізғ·зғғзҡ„еҸҷиҝ°дёӯпјҢжӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү в‘ еңЁзғ·зғғеҲҶеӯҗдёӯпјҢжүҖжңүзҡ„еҢ–еӯҰй”®йғҪжҳҜеҚ•й”®гҖҖ в‘Ўзғ·зғғдёӯйҷӨз”Ізғ·еӨ–пјҢеҫҲеӨҡйғҪиғҪдҪҝй…ёжҖ§KMnO4жә¶ж¶Ізҡ„зҙ«иүІиӨӘеҺ»гҖҖ в‘ўеҲҶеӯҗйҖҡејҸдёәCnH2n+2зҡ„зғғдёҚдёҖе®ҡжҳҜзғ·зғғгҖҖ в‘ЈжүҖжңүзҡ„зғ·зғғеңЁе…үз…§жқЎд»¶дёӢйғҪиғҪдёҺж°Ҝж°”еҸ‘з”ҹеҸ–д»ЈеҸҚеә” в‘Өе…үз…§жқЎд»¶дёӢпјҢд№ҷзғ·йҖҡе…Ҙжәҙж°ҙдёӯпјҢеҸҜдҪҝжәҙж°ҙиӨӘиүІпјҺ гҖҖВ В AпјҺв‘ в‘ўв‘ӨВ В В В BпјҺв‘Ўв‘ўВ В В В В В В В В CпјҺв‘ в‘ЈВ В В В В В В В В DпјҺв‘ в‘Ўв‘Ј
|
|
| 13. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—зү©иҙЁеңЁдёҖе®ҡжқЎд»¶дёӢеҸҜдёҺд№ҷзғ·еҸ‘з”ҹеҢ–еӯҰеҸҚеә”зҡ„жҳҜпјҲгҖҖгҖҖпјү гҖҖAпјҺж°Ҝж°”В В В В BпјҺжәҙж°ҙ гҖҖВ В CпјҺж°Ҝж°ҙ В В В В DпјҺй…ёжҖ§й«ҳй”°й…ёй’ҫжә¶ж¶І
|
|
| 14. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—зғ·зғғеңЁе…үз…§дёӢдёҺж°Ҝж°”еҸҚеә”пјҢеҸӘз”ҹжҲҗдёҖз§ҚдёҖж°Ҝд»Јзғғзҡ„жҳҜпјҲгҖҖгҖҖпјү гҖҖВ В AпјҺжӯЈдёҒзғ·В В В В В В В BпјҺејӮдёҒзғ·В В В В CпјҺз”Ізғ·В В В В В В В DпјҺдёҷзғ·
|
|
| 15. | иҜҰз»ҶдҝЎжҒҜ |
|
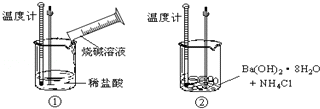
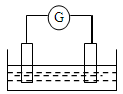
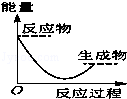
е°ҶжҹҗеӣәдҪ“ж°ўж°§еҢ–зү©MдёҺNH4ClзҪ®дәҺеҰӮеӣҫжүҖзӨәзҡ„иЈ…зҪ®пјҲзҺ»з’ғзүҮдёҺзғ§жқҜеә•йғЁд№Ӣй—ҙжңүдёҖи–„еұӮж°ҙпјүдёӯж··еҗҲеҸҚеә”еҗҺпјҢз”ЁжүӢжӢҝиө·зғ§жқҜж—¶пјҢеҸ‘зҺ°зҺ»з’ғзүҮдёҺзғ§жқҜзІҳеңЁдёҖиө·пјҢеҲҷиҜҘеҸҚеә”жүҖеҜ№еә”зҡ„иғҪйҮҸеҸҳеҢ–е…ізі»еӣҫжҳҜпјҲгҖҖгҖҖпјү гҖҖВ В AпјҺ CпјҺ
|
|
| 16. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҸҚеә”дёӯдёҚеұһдәҺж”ҫзғӯеҸҚеә”зҡ„жҳҜпјҲгҖҖгҖҖпјү гҖҖВ В AпјҺй…ёзўұдёӯе’ҢеҸҚеә”В В В В В В В В BпјҺNH4Clжҷ¶дҪ“дёҺBaпјҲOHпјү2вҖў8H2Oжҷ¶дҪ“еҸҚеә” гҖҖВ В CпјҺй•ҒжқЎзҡ„зҮғзғ§В В В В В В В В В В DпјҺжҙ»жіјйҮ‘еұһдёҺй…ёзҡ„еҸҚеә”
|
|
| 17. | иҜҰз»ҶдҝЎжҒҜ |
|
е·ІзҹҘпјҡNO2пјҲgпјү+SO2пјҲgпјү гҖҖВ В AпјҺдҪ“зі»еҺӢејәдҝқжҢҒдёҚеҸҳВ В В В В В В В В В В BпјҺж··еҗҲж°”дҪ“йўңиүІдҝқжҢҒдёҚеҸҳ гҖҖВ В CпјҺSO3дёҺNOзҡ„дҪ“з§ҜжҜ”дҝқжҢҒдёҚеҸҳгҖҖВ DпјҺжҜҸж¶ҲиҖ—1molSO2пјҢеҗҢж—¶з”ҹжҲҗ1molNO
|
|
| 18. | иҜҰз»ҶдҝЎжҒҜ |
|
е°ҶзӣӣжңүNH4HCO3зІүжң«зҡ„е°Ҹзғ§жқҜж”ҫе…Ҙзӣӣжңүе°‘йҮҸйҶӢй…ёзҡ„еӨ§зғ§жқҜдёӯпјҺ然еҗҺеҗ‘е°Ҹзғ§жқҜдёӯеҠ е…Ҙзӣҗй…ёпјҢеҸҚеә”еү§зғҲпјҢйҶӢй…ёйҖҗжёҗеҮқеӣәпјҺз”ұжӯӨеҸҜи§ҒпјҲгҖҖгҖҖпјү гҖҖВ В AпјҺNH4HCO3е’Ңзӣҗй…ёзҡ„еҸҚеә”жҳҜж”ҫзғӯеҸҚеә” гҖҖВ В BпјҺиҜҘеҸҚеә”дёӯпјҢзғӯиғҪиҪ¬еҢ–дёәдә§зү©еҶ…йғЁзҡ„иғҪйҮҸ гҖҖВ В CпјҺеҸҚеә”зү©зҡ„жҖ»иғҪйҮҸй«ҳдәҺз”ҹжҲҗзү©зҡ„жҖ»иғҪйҮҸ гҖҖВ В DпјҺж–ӯиЈӮж—§еҢ–еӯҰй”®еҗёж”¶зҡ„жҖ»иғҪйҮҸе°ҸдәҺеҪўжҲҗж–°еҢ–еӯҰй”®ж”ҫеҮәзҡ„жҖ»иғҪйҮҸ
|
|
| 19. | иҜҰз»ҶдҝЎжҒҜ |
|
дёҖе®ҡжё©еәҰпјҢеҸҜйҖҶеҸҚеә”2NO2вҮҢ2NO+O2еңЁдҪ“з§Ҝеӣәе®ҡзҡ„еҜҶй—ӯе®№еҷЁдёӯеҸҚеә”пјҢиҫҫеҲ°е№іиЎЎзҠ¶жҖҒж Үеҝ—жҳҜпјҲгҖҖгҖҖпјү в‘ еҚ•дҪҚж—¶й—ҙеҶ…з”ҹжҲҗn mol O2пјҢеҗҢж—¶з”ҹжҲҗ2n mol NO2 в‘ЎеҚ•дҪҚж—¶й—ҙеҶ…з”ҹжҲҗn mol O2пјҢеҗҢж—¶з”ҹжҲҗ2n mol NO в‘ўз”ЁNO2гҖҒNOгҖҒO2зҡ„зү©иҙЁзҡ„йҮҸжө“еәҰеҸҳеҢ–иЎЁзӨәзҡ„еҸҚеә”йҖҹзҺҮзҡ„жҜ”дёә2пјҡ2пјҡ1 в‘Јж··еҗҲж°”дҪ“зҡ„еҺӢејәдёҚеҶҚж”№еҸҳ в‘Өж··еҗҲж°”дҪ“зҡ„йўңиүІдёҚеҶҚж”№еҸҳ в‘Ҙж··еҗҲж°”дҪ“зҡ„е№іеқҮж‘©е°”иҙЁйҮҸдёҚеҶҚж”№еҸҳпјҺ гҖҖВ В AпјҺв‘ в‘Јв‘Өв‘ҘВ В BпјҺв‘ в‘Ўв‘ўв‘ӨВ В В В В CпјҺв‘Ўв‘ўв‘Јв‘ҘВ В В В В DпјҺд»ҘдёҠе…ЁйғЁ
|
|
| 20. | иҜҰз»ҶдҝЎжҒҜ |
|
йҮ‘еҲҡзҹідёҺзҹіеўЁжҳҜзўізҡ„дёӨз§ҚеҗҢзҙ ејӮеҪўдҪ“пјҢеңЁ100kPaж—¶пјҢ1molзҹіеўЁиҪ¬еҢ–дёәйҮ‘еҲҡзҹіиҰҒеҗёж”¶1.895kJзҡ„зғӯйҮҸпјҢдёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү гҖҖ AпјҺйҮ‘еҲҡзҹіжҜ”зҹіеўЁзЁіе®ҡгҖҖВ В В В В В В В В В В В В В В В В BпјҺзҹіеўЁжҜ”йҮ‘еҲҡзҹізЁіе®ҡ гҖҖ CпјҺ1molзҹіеўЁжҜ”1molйҮ‘еҲҡзҹізҡ„жҖ»иғҪйҮҸй«ҳгҖҖDпјҺ1molйҮ‘еҲҡзҹіз”ҹжҲҗ1molзҹіеўЁиҰҒеҗёж”¶зғӯйҮҸ
|
|
| 21. | иҜҰз»ҶдҝЎжҒҜ |
|
е·ІзҹҘеҸҚеә”в‘ 2BrO3-+Cl29Br2+2ClO3- в‘Ў5C12+I2+6H2O92HIO3+10HCl В В В в‘ўClO3-+5C1-+6H+93Cl2+3H2OпјҢдёӢеҲ—зү©иҙЁж°§еҢ–иғҪеҠӣејәејұйЎәеәҸжӯЈзЎ®зҡ„жҳҜ(В В В ) В AпјҺClO3-п№ҘBrO3-п№ҘIO3-п№ҘC12В В В В В В BпјҺBrO3-п№ҘC12п№ҘClO3-п№ҘIO3- В CпјҺBrO3-п№ҘClO3-п№ҘC12п№ҘIO3-В В В В В В DпјҺC12п№ҘBrO3-п№ҘClO3-п№ҘIO3-
|
|
| 22. | иҜҰз»ҶдҝЎжҒҜ |
|
еҶіе®ҡеҢ–еӯҰеҸҚеә”йҖҹзҺҮзҡ„ж №жң¬еӣ зҙ жҳҜпјҲгҖҖгҖҖпјү гҖҖВ В AпјҺжё©еәҰе’ҢеҺӢејә В В В В В В В В В В В В В В В В В В В В В В BпјҺеҸҚеә”зү©зҡ„жө“еәҰ гҖҖВ В CпјҺеҸӮеҠ еҸҚеә”зҡ„еҗ„зү©иҙЁзҡ„жҖ§иҙЁВ В В В В В В В DпјҺеӮ¬еҢ–еүӮзҡ„еҠ е…Ҙ
|
|
| 23. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—з»“и®әжҳҜд»ҺжҹҗеҗҢеӯҰзҡ„笔记жң¬дёҠж‘ҳеҪ•зҡ„пјҢдҪ и®Өдёәе…¶дёӯиӮҜе®ҡжӯЈзЎ®зҡ„жҳҜ(гҖҖгҖҖ) в‘ еҫ®зІ’еҚҠеҫ„ClпјҚпјһS2пјҚпјһSпјһFгҖҖв‘Ўж°ўеҢ–зү©зҡ„зЁіе®ҡжҖ§ HFпјһHClпјһH2SпјһH2SeгҖҖв‘ўиҝҳеҺҹжҖ§S2пјҚпјһClпјҚпјһBrпјҚпјһIпјҚгҖҖв‘Јж°§еҢ–жҖ§ Cl2пјһSпјһSeпјһTeгҖҖв‘Өй…ёжҖ§ H2SO4пјһHClO4пјһH2SeO4гҖҖв‘Ҙеҫ—з”өеӯҗиғҪеҠӣFпјһClпјһBrпјһI AпјҺеҸӘжңүв‘ В В В В В В В В В BпјҺв‘ в‘ўв‘ЈВ В В В В В В В CпјҺв‘Ўв‘Јв‘ҘВ В В В В В В В DпјҺеҸӘжңүв‘Ҙ
|
|
| 24. | иҜҰз»ҶдҝЎжҒҜ |
|
еңЁCпјҲsпјү+CO2пјҲgпјүвҮҢ2COпјҲgпјүеҸҚеә”дёӯпјҢеҸҜдҪҝеҸҚеә”йҖҹзҺҮеўһеӨ§зҡ„жҺӘж–ҪжҳҜпјҲгҖҖгҖҖпјү в‘ еўһеӨ§еҺӢејәгҖҖв‘ЎеўһеҠ зӮӯзҡ„йҮҸгҖҖв‘ўйҖҡе…ҘCO2гҖҖв‘ЈжҒ’еҺӢдёӢе……е…ҘN2гҖҖв‘ӨжҒ’е®№дёӢе……е…ҘN2гҖҖв‘ҘйҖҡе…ҘCOпјҺ гҖҖВ AпјҺв‘ в‘ўв‘ЈВ В В В В BпјҺв‘Ўв‘Јв‘ҘВ В В В В CпјҺв‘ в‘ўв‘ҘВ В В В В DпјҺв‘ўв‘Өв‘Ҙ
|
|
| 25. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—зҰ»еӯҗж–№зЁӢејҸй”ҷиҜҜзҡ„жҳҜпјҲгҖҖгҖҖпјү гҖҖAпјҺзЎ«й…ёжә¶ж¶ІдёҺж°ўж°§еҢ–й’Ўжә¶ж¶Іж··еҗҲпјҡBa2++SO42п№Ј=BaSO4вҶ“ гҖҖBпјҺзҹізҒ°зҹіжә¶дәҺзӣҗй…ёдёӯCaCO3+2H+=Ca2++CO2вҶ‘+H2O гҖҖCпјҺзўій…ёж°ўй’ жә¶ж¶ІдёҺзЎқй…ёеҸҚеә”пјҡHCO3п№Ј+H+=H2O+CO2вҶ‘ В DпјҺж°§еҢ–й“ҒдёҺзЁҖзЎ«й…ёеҸҚеә”пјҡFe2O3+6H+=2Fe3++3H2O
|
|
| 26. | иҜҰз»ҶдҝЎжҒҜ | ||||||||||||||||||||
|
дёӢеҲ—еӣӣж”ҜиҜ•з®ЎдёӯпјҢеңЁдёҚеҗҢжқЎд»¶дёӢеҸҚеә”пјҡFe + 2HCl = FeCl2 + H2вҶ‘ еҲӨж–ӯдә§з”ҹH2зҡ„еҸҚеә”йҖҹзҺҮжңҖеҝ«зҡ„жҳҜпјҲВ В В В пјү
|
|||||||||||||||||||||
| 27. | иҜҰз»ҶдҝЎжҒҜ |
|
еҸҚеә”4NH3(g)+5O2пјҲgпјүпјқ4NOпјҲgпјү+6H2OпјҲgпјүеңЁ2еҚҮеҜҶй—ӯе®№еҷЁдёӯиҝӣиЎҢ1еҲҶй’ҹеҗҺпјҢNH3еҮҸе°‘дәҶ0.12 molпјҢеҲҷе№іеқҮжҜҸз§’й’ҹжө“еәҰеҸҳеҢ–жӯЈзЎ®зҡ„жҳҜ пјҲВ В В В В пјү AпјҺH2Oпјҡ0.002 molВ·LпјҚ1В В В В В В В В В В В В В В В В В BпјҺNOпјҡ0.001 molВ·LпјҚ1 CпјҺNH3пјҡ 0.002 molВ·LпјҚ1В В В В В В В В В В В В В В В В DпјҺO2пјҡ0.0025 molВ·LпјҚ1
|
|
| 28. | иҜҰз»ҶдҝЎжҒҜ |
|
е°Ҷ0пјҺ1 mol N2е’Ң0пјҺ3 mol H2зҪ®дәҺеҜҶй—ӯе®№еҷЁдёӯеҸ‘з”ҹеә”:N2+3H2 AпјҺеўһеӨ§еҺӢејәпјҢеҸҚеә”йҖҹзҺҮеҮҸе°ҸВ В В В В В BпјҺжңҖз»ҲеҸҜз”ҹжҲҗ0пјҺ2 mol NH3 CпјҺеҚҮй«ҷжё©еәҰпјҢеҸҚеә”йҖҹзҺҮеўһеӨ§ DпјҺеҪ“VжӯЈпјҲN2пјү:V жӯЈ (H2)=1пјҡ3ж—¶пјҢдёҖе®ҡиҫҫеҢ–еӯҰе№іиЎЎзҠ¶жҖҒ
|
|
| 29. | иҜҰз»ҶдҝЎжҒҜ |
|
C4H10зҡ„дёҖж°ҜеҸ–д»Јзү©е…ұжңү(В В В В В ) AпјҺ1з§ҚВ В В В В В В В В В В BпјҺ2з§ҚВ В В В В В В В В В В В В CпјҺ3з§ҚВ В В В В В В В В В В В DпјҺ4з§Қ
|
|
| 30. | иҜҰз»ҶдҝЎжҒҜ |
|
жҹҗеҗҢеӯҰеҜ№дёҖж— иүІйҖҸжҳҺжә¶ж¶ІиҝӣиЎҢеҲҶжһҗеҫ—еҮәиҜҘжә¶ж¶Ідёӯеҗ«жңүдёӢеҲ—жҹҗз»„зҰ»еӯҗпјҢдҪ и®ӨдёәиҜҘз»„зҰ»еӯҗеә”иҜҘжҳҜпјҲгҖҖгҖҖпјү гҖҖВ В AпјҺAl3+гҖҒNO3п№ЈгҖҒK+гҖҒSO42п№ЈВ В В В В В В В В В В В В В В BпјҺВ В В Ca2+гҖҒH+гҖҒCO32п№ЈгҖҒAlO2п№Ј гҖҖВ В CпјҺOHп№ЈгҖҒSO42п№ЈгҖҒNH4+гҖҒAl3+ В В В В В В В DпјҺ Fe3+гҖҒMg2+гҖҒNO3п№ЈгҖҒClп№Ј
|
|
| 31. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҸҚеә”дёӯпјҢй“Ғе…ғзҙ иў«ж°§еҢ–зҡ„жҳҜпјҲВ В В В В пјү В AпјҺFeS+2HCl9FeCl2+2H2SвҶ‘В В В В В BпјҺFe+H2S049FeS04+H2вҶ‘ В CпјҺFeO+2HCl9FeCl2+H20В В В В В В В DпјҺFe203+3CO92Fe+3C02вҶ‘
|
|
| 32. | иҜҰз»ҶдҝЎжҒҜ |
|
йҷӨеҺ»Na2CO3еӣәдҪ“дёӯе°‘йҮҸNaHCO3зҡ„жңҖдҪіж–№жі•жҳҜпјҲВ В В В В пјү В AпјҺеҠ е…ҘйҖӮйҮҸзӣҗй…ёВ В В В В В В В В В В В В В BпјҺеҠ е…ҘNaOHжә¶ж¶І В CпјҺеҠ зғӯВ В В В В В В В В В В В В В В В В В В В В В DпјҺй…ҚжҲҗжә¶ж¶ІеҗҺйҖҡдәәCO2
|
|
| 33. | иҜҰз»ҶдҝЎжҒҜ |
|
иғҪиҜҒжҳҺзЎ…й…ёзҡ„й…ёжҖ§ејұдәҺзўій…ёй…ёжҖ§зҡ„е®һйӘҢдәӢе®һжҳҜ В AпјҺCO2жә¶дәҺж°ҙеҪўжҲҗзўій…ёпјҢSiO2йҡҫжә¶дәҺж°ҙВ BпјҺCO2йҖҡдәәеҸҜжә¶жҖ§зЎ…й…ёзӣҗдёӯжһҗеҮәзЎ…й…ёжІүж·Җ В CпјҺй«ҳжё©дёӢSiO2дёҺзўій…ёзӣҗеҸҚеә”з”ҹжҲҗC02В В В В DпјҺCO2жҳҜж°”дҪ“пјҢSiO2жҳҜеӣәдҪ“
|
|
| 34. | иҜҰз»ҶдҝЎжҒҜ |
|
жңүaгҖҒbгҖҒcгҖҒdеӣӣз§Қе…ғзҙ гҖӮaгҖҒbзҡ„йҳізҰ»еӯҗдёҺcгҖҒdзҡ„йҳҙзҰ»еӯҗе…·жңүзӣёеҗҢзҡ„з”өеӯҗеұӮз»“жһ„пјӣaзҡ„йҳізҰ»еӯҗзҡ„жӯЈз”өиҚ·ж•°е°ҸдәҺbзҡ„йҳізҰ»еӯҗзҡ„жӯЈз”өиҚ·ж•°пјҢcзҡ„йҳҙзҰ»еӯҗзҡ„иҙҹз”өиҚ·ж•°еӨ§дәҺdзҡ„йҳҙзҰ»еӯҗзҡ„иҙҹз”өиҚ·ж•°гҖӮеҲҷе®ғ们зҡ„зҰ»еӯҗеҚҠеҫ„зҡ„е…ізі»жҳҜпјҲВ В пјүВ В В В В В В В AпјҺaпјһbпјһcпјһdВ В В В BпјҺcпјһdпјһa>bВ В В В В CпјҺcпјһaпјһdпјһbВ В В В DпјҺbпјһaпјһdпјһc
|
|
| 35. | иҜҰз»ҶдҝЎжҒҜ | |||||||||||||||
|
еҮ з§Қзҹӯе‘Ёжңҹе…ғзҙ зҡ„еҺҹеӯҗеҚҠеҫ„еҸҠдё»иҰҒеҢ–еҗҲд»·еҰӮдёӢиЎЁпјҡ
дёӢеҲ—еҸҷиҝ°жӯЈзЎ®зҡ„жҳҜ(гҖҖгҖҖ) AпјҺXгҖҒYе…ғзҙ зҡ„йҮ‘еұһжҖ§X<Y BпјҺдёҖе®ҡжқЎд»¶дёӢпјҢZеҚ•иҙЁдёҺWзҡ„еёёи§ҒеҚ•иҙЁзӣҙжҺҘз”ҹжҲҗZW2 CпјҺYзҡ„жңҖй«ҳд»·ж°§еҢ–зү©еҜ№еә”зҡ„ж°ҙеҢ–зү©иғҪжә¶дәҺзЁҖж°Ёж°ҙ DпјҺдёҖе®ҡжқЎд»¶дёӢпјҢWеҚ•иҙЁеҸҜд»Ҙе°ҶZеҚ•иҙЁд»Һе…¶ж°ўеҢ–зү©дёӯзҪ®жҚўеҮәжқҘ
|
||||||||||||||||
| 36. | иҜҰз»ҶдҝЎжҒҜ |
|
жңүдёӢеҲ—еҗ„з»„еҫ®зІ’жҲ–зү©иҙЁпјҡ AпјҡC60е’ҢC70пјӣВ В Bпјҡ Dпјҡ в‘ гҖҖгҖҖгҖҖгҖҖгҖҖгҖҖз»„дёӨз§Қеҫ®зІ’дә’дёәеҗҢдҪҚзҙ пјӣ в‘ЎгҖҖгҖҖгҖҖгҖҖгҖҖгҖҖз»„дёӨз§Қзү©иҙЁдә’дёәеҗҢзҙ ејӮеҪўдҪ“пјӣ в‘ўгҖҖгҖҖгҖҖгҖҖгҖҖгҖҖз»„дёӨз§Қзү©иҙЁеұһдәҺеҗҢзі»зү©пјӣ в‘ЈгҖҖгҖҖгҖҖгҖҖгҖҖгҖҖз»„дёӨзү©иҙЁдә’дёәеҗҢеҲҶејӮжһ„дҪ“пјӣ в‘ӨгҖҖгҖҖгҖҖгҖҖгҖҖгҖҖз»„дёӨзү©иҙЁжҳҜеҗҢдёҖзү©иҙЁпјҺ
|
|
| 37. | иҜҰз»ҶдҝЎжҒҜ |
|
В пјҲ1пјүеҢ–еӯҰејҸдёәC8Hmзҡ„зғ·зғғпјҢmеҖјзӯүдәҺгҖҖгҖҖгҖҖгҖҖгҖҖгҖҖпјӣCnH22зҡ„зғ·зғғпјҢnеҖјзӯүдәҺгҖҖгҖҖгҖҖгҖҖгҖҖгҖҖпјҺ пјҲ2пјүжҹҗеҗҢеӯҰиҝӣиЎҢеҰӮдёӢе®һйӘҢпјҢжҺўз©¶еҢ–еӯҰеҸҚеә”дёӯзҡ„иғҪйҮҸеҸҳеҢ–пјҺйҖҡиҝҮе®һйӘҢжөӢеҮәпјҢеҸҚеә”еүҚеҗҺв‘ зғ§жқҜдёӯзҡ„жё©еәҰеҚҮй«ҳпјҢв‘Ўзғ§жқҜдёӯзҡ„жё©еәҰйҷҚдҪҺпјҺз”ұжӯӨеҲӨж–ӯNaOHжә¶ж¶Іи·ҹзӣҗй…ёзҡ„еҸҚеә”жҳҜгҖҖгҖҖгҖҖгҖҖгҖҖгҖҖпјҲеЎ«вҖңеҗёзғӯвҖқжҲ–вҖңж”ҫзғӯвҖқпјүеҸҚеә”пјҢBaпјҲOHпјү2вҖў8H2Oи·ҹNH4Clзҡ„еҸҚеә”жҳҜгҖҖгҖҖгҖҖгҖҖгҖҖгҖҖпјҲеЎ«вҖңеҗёзғӯвҖқжҲ–вҖңж”ҫзғӯвҖқпјүеҸҚеә”пјҺиҜ•еҶҷеҮәв‘ дёӯеҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸгҖҖгҖҖгҖҖгҖҖгҖҖгҖҖпјҺ
|
|
| 38. | иҜҰз»ҶдҝЎжҒҜ |
|
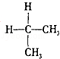
еҰӮеӣҫжҳҜеёёи§ҒеҺҹз”өжұ иЈ…зҪ®пјҢз”өжөҒиЎЁGеҸ‘з”ҹеҒҸиҪ¬пјҡ
пјҲ1пјүиӢҘдёӨдёӘз”өжһҒеҲҶеҲ«жҳҜZnгҖҒCu,з”өи§ЈиҙЁжә¶ж¶ІжҳҜзЁҖзЎ«й…ёпјҢжӯЈжһҒзҡ„з”өжһҒеҸҚеә”ејҸдёә___________________________пјӣеҰӮжһңжҠҠз”өи§ЈиҙЁжә¶ж¶ІжҚўжҲҗзЎ«й…ёй“ңжә¶ж¶ІпјҢеҲҷжӯЈжһҒзҡ„з”өжһҒеҸҚеә”ејҸдёә_____________________________гҖӮ пјҲ2пјүиӢҘжҖ»еҸҚеә”жҳҜ2FeCl3пјӢFeпјқ3FeCl2пјҢеҲҷеҸҜд»ҘеҒҡиҙҹжһҒжқҗж–ҷзҡ„жҳҜ________пјҢ иҙҹжһҒдёҠеҸ‘з”ҹзҡ„з”өжһҒеҸҚеә”жҳҜ________________________гҖӮ пјҲ3пјүиӢҘз”өи§ЈиҙЁжә¶ж¶ІжҳҜзЁҖзЎ«й…ёпјҢMgгҖҒAlдёӨз§ҚйҮ‘еұһеҒҡз”өжһҒпјҢеҲҷMgз”өжһҒзҡ„з”өжһҒеҸҚеә”ејҸдёә_____________пјӣ
|
|
| 39. | иҜҰз»ҶдҝЎжҒҜ |
|
AгҖҒBгҖҒCгҖҒD 4з§Қе…ғзҙ пјҢAе…ғзҙ жүҖеӨ„зҡ„е‘Ёжңҹж•°гҖҒдё»ж—ҸеәҸж•°гҖҒеҺҹеӯҗеәҸж•°еқҮзӣёзӯүпјӣBзҡ„еҺҹеӯҗеҚҠеҫ„жҳҜе…¶жүҖеңЁдё»ж—ҸдёӯжңҖе°Ҹзҡ„пјҢBзҡ„жңҖй«ҳд»·ж°§еҢ–зү©еҜ№еә”ж°ҙеҢ–зү©зҡ„еҢ–еӯҰејҸдёәHBO3пјӣCе…ғзҙ еҺҹеӯҗзҡ„жңҖеӨ–еұӮз”өеӯҗж•°жҜ”ж¬ЎеӨ–еұӮе°‘2дёӘпјӣCзҡ„йҳҙзҰ»еӯҗдёҺDзҡ„йҳізҰ»еӯҗе…·жңүзӣёеҗҢзҡ„з”өеӯҗжҺ’еёғпјҢдёӨе…ғзҙ еҸҜеҪўжҲҗеҢ–еҗҲзү©D2CгҖӮ (1) Bе…ғзҙ зҡ„еҗҚз§°дёә________пјӣ (2)AгҖҒBеҪўжҲҗзҡ„еҢ–еҗҲзү©зҡ„з”өеӯҗејҸдёә________________гҖӮ (3) Cзҡ„е…ғзҙ з¬ҰеҸ·дёә________пјҢCзҡ„жңҖй«ҳд»·ж°§еҢ–зү©зҡ„еҢ–еӯҰејҸдёә__________________гҖӮ (4) Dзҡ„жңҖй«ҳд»·ж°§еҢ–зү©еҜ№еә”зҡ„ж°ҙеҢ–зү©зҡ„еҢ–еӯҰејҸдёә____________________________гҖӮ
|
|
| 40. | иҜҰз»ҶдҝЎжҒҜ |
|
е°Ҷ1.0 mol Xж°”дҪ“е’Ң1.0 mol Yж°”дҪ“ж··еҗҲдәҺ2 Lзҡ„еҜҶй—ӯе®№еҷЁдёӯпјҢеҸ‘з”ҹеҸҚеә”2X(g)пјӢY(g) AпјҺеҚ•дҪҚж—¶й—ҙйҮҢпјҢж¶ҲиҖ—2 mol XпјҢеҗҢж—¶з”ҹжҲҗ2 mol W B.еҚ•дҪҚж—¶й—ҙйҮҢпјҢж¶ҲиҖ—2 mol XпјҢеҗҢж—¶д№ҹж¶ҲиҖ—дәҶ2 mol Z C.еҸҚеә”ж··еҗҲзү©дёӯеҗ„зү©иҙЁзҡ„жө“еәҰзӣёзӯү DпјҺеҸҚеә”ж··еҗҲзү©дёӯеҗ„зү©иҙЁзҡ„жө“еәҰдёҚеҶҚж”№еҸҳ
|
|
| 41. | иҜҰз»ҶдҝЎжҒҜ |
|
е°Ҷ6molAе’Ң5molBж··еҗҲж”ҫе…Ҙ4LеҜҶй—ӯе®№еҷЁдёӯпјҢеңЁдёҖе®ҡжқЎд»¶дёӢеҸ‘з”ҹеҸҚеә”пјҡ3AпјҲgпјү+BпјҲgпјүвҮҢ2CпјҲgпјү+xDпјҲgпјүпјҢз»Ҹ5minиҫҫеҲ°е№іиЎЎпјҢжӯӨж—¶Cзҡ„жө“еәҰдёә0.5molвҖўLп№Ј1пјҢжөӢеҫ—Dзҡ„е№іеқҮеҸҚеә”йҖҹзҺҮдёә0.15molвҖўLп№Ј1вҖўminп№Ј1пјҢеҲҷе№іиЎЎж—¶Aзҡ„зү©иҙЁзҡ„йҮҸжө“еәҰдёәгҖҖгҖҖгҖҖгҖҖгҖҖгҖҖпјҢBзҡ„е№іеқҮеҸҚеә”йҖҹзҺҮдёәгҖҖгҖҖгҖҖгҖҖгҖҖгҖҖпјҢxзҡ„еҖјдёәгҖҖгҖҖгҖҖгҖҖгҖҖгҖҖпјҺ
|
|
| 42. | иҜҰз»ҶдҝЎжҒҜ |
|
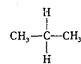
ж №жҚ®зі»з»ҹе‘ҪеҗҚжі•еҶҷеҮәдёӢеҲ—жңүжңәзү©зҡ„еҗҚз§° гҖҖпјҲ1пјү(CH3)2CHC(C2H5)2C(CH3)2C2H5 В В В В В В В В В В В В В В CH3В В В В В В В В В В В В В В В В В В В В В В В В В В В CH3В В В В В В В В В пјҲ2пјү CH3-CH-C-CH3В В В В В В В В В В В В В В В В В (3) CH3-CHпјҚCH2 пјҚCH3В В В В В В В В В В В В В CH3 CH3
|
|
| 43. | иҜҰз»ҶдҝЎжҒҜ |
|
В вҖңз«Ӣж–№зғ·вҖқжҳҜдёҖз§Қж–°еҗҲжҲҗзҡ„зғғпјҢе…¶еҲҶеӯҗејҸдёәжӯЈж–№дҪ“з»“жһ„пјҢе…¶зўіжһ¶з»“жһ„еҰӮеӣҫжүҖзӨәгҖӮ пјҲ1пјүз«Ӣж–№зғ·зҡ„еҲҶеӯҗејҸдёәВ В В В В В В В гҖӮ пјҲ2пјүиҜҘз«Ӣж–№зғ·зҡ„дёҖж°Ҝд»Јзү©е…·жңүзҡ„еҗҢеҲҶејӮжһ„дҪ“жңүВ В В В В з§ҚгҖӮ пјҲ3пјүиҜҘз«Ӣж–№зғ·зҡ„дәҢж°Ҝд»Јзү©е…·жңүзҡ„еҗҢеҲҶејӮжһ„дҪ“жңүВ В В В В з§ҚгҖӮ пјҲ4пјүиӢҘиҰҒдҪҝ1molиҜҘзғ·зғғзҡ„жүҖжңүж°ўеҺҹеӯҗе…ЁйғЁиў«ж°ҜеҺҹеӯҗеҸ–д»ЈпјҢйңҖиҰҒВ В В В В molж°Ҝж°”гҖӮ
|
|
- ејҖеҺҹеёӮж— зәёиҜ•еҚ·
- иҸҸжіҪеёӮ2018е№ҙй«ҳдәҢдёҠеҚҠе№ҙеҢ–еӯҰжңҹжң«иҖғиҜ•зҪ‘з»ңиҖғиҜ•иҜ•еҚ·
- ж–°з–Ҷ2020е№ҙй«ҳдәҢеҢ–еӯҰеҗҺеҚҠжңҹжңҹдёӯиҖғиҜ•ж— зәёиҜ•еҚ·
- йҳҶдёӯдёӯеӯҰ2018е№ҙй«ҳдёҖдёҠеҚҠжңҹеҢ–еӯҰжңҹдёӯиҖғиҜ•йҷ„зӯ”жЎҲдёҺи§Јжһҗ
- е№ҝе·һеёӮ2018е№ҙй«ҳдёҖдёҠеҚҠжңҹеҢ–еӯҰжңҹдёӯиҖғиҜ•еңЁзәҝзӯ”йўҳ
- дёҠжө·еӨҚж—Ұйҷ„дёӯй«ҳдёҖеҢ–еӯҰдёҠеҶҢжңҹдёӯиҖғиҜ•иҜ•еҚ·е®Ңж•ҙзүҲ
- 2019-2020е№ҙй«ҳдәҢдёӢеҶҢжңҹжң«иҖғиҜ•еҢ–еӯҰзҪ‘дёҠжЈҖжөӢж— зәёиҜ•еҚ·еёҰзӯ”жЎҲе’Ңи§ЈжһҗпјҲж№–еҚ—еёҲиҢғеӨ§еӯҰйҷ„еұһдёӯеӯҰпјү
- иҫҪе®ҒзңҒеӨ§иҝһеёӮйҮ‘жҷ®ж–°еҢә2020-2021е№ҙй«ҳдёҖдёӢеҚҠжңҹејҖеӯҰжЈҖжөӢеҢ–еӯҰйўҳе…Қиҙ№иҜ•еҚ·

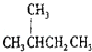
 В В В В В В В В В В В В В В В В В
В В В В В В В В В В В В В В В В В 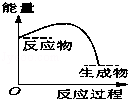 В В В
В В В 
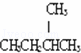
 В В В В В В В В В В В В E
В В В В В В В В В В В В E