天津市宝坻区2019年九年级化学下学期结课考试试卷及答案
| 1. | 详细信息 |
|
下列人体所必需的元素中,缺乏后会导致贫血的是( ) A.锌 B.钙 C.铁 D.碘
|
|
| 2. | 详细信息 |
|
下列属于有机合成材料的是( ) A.陶瓷 B.硬铝 C.塑料 D.钢筋混凝土
|
|
| 3. | 详细信息 |
|
下列化肥中,从外观即可与其他化肥相区别的是( ) A.磷矿粉 B.硝酸铵 C.硫酸钾 D.氯化钾
|
|
| 4. | 详细信息 |
|
某同学用pH试纸测定日常生活中的一些液体的pH.他的实验记录一定错误的是( ) A.肥皂水pH=10 B.纯碱溶液pH=11 C.橘子汁pH=4 D.食醋pH=7
|
|
| 5. | 详细信息 |
|
下列应用与中和反应原理无关的是( ) A.使用熟石灰改良酸性土壤 B.用消石灰和硫酸铜溶液配置波尔多液 C.用含氢氧化铝的药物治疗胃酸过多 D.用烧碱溶液洗涤石油产品中的残余硫酸
|
|
| 6. | 详细信息 |
|
下列物质敞口放置在空气中一段时间后,质量增加且没有变质的是( ) A.生石灰 B.浓硫酸 C.纯碱 D.火碱
|
|
| 7. | 详细信息 |
|
现将X、Y两种金属片分别插入硫酸铜溶液中,X无明显变化,Y表面有铜析出,则X、Y、Cu三种金属的活动性由强到弱的顺序是( ) A. X>Y>Cu B. Cu>X>Y C. X>Cu>Y D. Y>Cu>X
|
|
| 8. | 详细信息 |
|
下列物质的变化,必须是只通过加入盐的溶液才能一步实现的是( ) A. CuO→CuCl2 B. K2CO3→KCl C. CaCO3→CaCl2 D. K2SO4→KCl
|
|
| 9. | 详细信息 |
|
下列做法科学的是( ) A. 用盐酸可以去除生石灰中的少量CaCO3 B. 用灼烧法可以区别涤纶和羊毛 C. 用稀硫酸可以除去铁粉中混有的少量氧化铜 D. 用Ba(NO3)2溶液可以除去稀盐酸中少量的H2SO4
|
|
| 10. | 详细信息 |
|
推理是化学学习中常用的思维方法,下列推理正确的是( ) A. 酸性溶液的pH小于7,食醋呈酸性,故食醋的pH小于7 B. 酸能使紫色石蕊试剂变红,紫色石蕊试液中通入CO2后变红,故CO2是酸 C. 酸碱中和反应生成盐和水,所以有盐和水生成的反应一定是中和反应 D. 溶液中有晶体析出时,溶质质量减小,所以溶液的溶质质量分数一定减小
|
|
| 11. | 详细信息 |
|
分别将下列各组物质同时加入到足量水中,最终能得到无色、透明溶液的是 ( ) A. BaCl2 、Na0H、H2 S04 B. NaCl、 Na0H、 CuS04 C. HN03、NaCl、K2S04 D. FeCl3 、Na2S04 、KCl
|
|
| 12. | 详细信息 |
|
下列说法正确的是( ) A.在相同温度下同一物质的饱和溶液与不饱和溶液所含溶质的质量一定不相等 B.某KNO3溶液在室温下蒸发5g水析出ag晶体,再蒸发5g水又析出bg晶体,则a与b一定相等 C.将溶质质量分数为98%的浓硫酸稀释为49%的硫酸,加水的质量与所取浓硫酸的质量一定相等 D.已知Mg(OH)2和MgO的混合物中镁元素的质量分数为48%,取该混合物10g,加入适量的稀硫酸,恰好完全反应后所得溶液中溶质的质量一定为24g
|
|
| 13. | 详细信息 |
|
下列说法错误的是( ) A. 炉具清洁剂中的氢氧化钠具有强烈的腐蚀性 B. NaCl和NaNO2都有咸味,都可以用来调味 C. 用柠檬酸、果汁、白糖、水、小苏打等可制汽水 D. 碳酸钠俗称纯碱,常用于玻璃、造纸、洗涤剂的生产
|
|
| 14. | 详细信息 |
|
下列对露置在空气中已部分变质的氢氧化钠溶液样品进行的相关实验中,实验现象 及结论合理的是( ) A.取少量溶液样品,滴入氯化钡溶液,有白色沉淀生成 B.取一定量溶液样品,滴入稀盐酸,立即有大量气体产生 C.取一定量溶液样品,滴入适量的澄清石灰水,过滤,向滤液中滴加酚酞溶液,溶液变红,证明原样品中含有氢氧化钠 D.向溶液样品中加入适量的澄清石灰水至恰好完全反应,过滤,可除去样品中的杂质
|
|
| 15. | 详细信息 |
|
下列除杂方法(括号内为杂质)中正确的是( ) A.二氧化碳(一氧化碳):通入氧气,点燃 B.硝酸铜溶液(硝酸银):加入足量的铜粉,过滤 C.碳酸钙固体(氯化钙):加入足量的水溶解,过滤、洗涤、干燥 D.氢氧化钠溶液(碳酸钠):加入适量的稀盐酸至不再产生气泡
|
|
| 16. | 详细信息 | ||||||
|
我们的生活离不开化学。现有①烧碱②钛合金③熟石灰④盐酸 ⑤碳酸氢钠⑥纯碱,选择适当物质填空(填序号)。 (1)可用于制造人造骨骼的是 。 (2)广泛应用于肥皂、石油、造纸等的是 ; (3)除油污可作炉具清洁剂的是______________; (4)可用来改良酸性土壤的碱是 ; (5)焙制糕点所用的发酵粉的主要成分之一是 。 (6)人体胃液中含有的酸是 ;
|
|||||||
| 17. | 详细信息 |
|
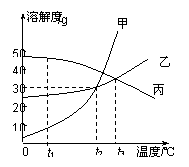
甲、乙、丙三种固体物质的溶解度曲线如右图所示。回答下列问题:
的顺序是 ; (2)t2℃时,甲和乙的溶解度 (填“相等” 或“不相等”); (3)t2℃时,甲物质的饱和溶液中溶质与溶剂的质量 比为 (写最简比); (4)t3℃时,将乙和丙两种物质的饱和溶液降低到t1℃,所得溶液中溶质的质量分数 大小关系为:乙 丙(填“>”、“<”或“=”)。
|
|
| 18. | 详细信息 |
|
写出下列反应的化学方程式: (1)氧化钙溶于水发生反应 ; (2)硝酸银溶液与铜丝反应 ; (3)用含氢氧化铝的药物治疗胃酸过多 ;
|
|
| 19. | 详细信息 |
|
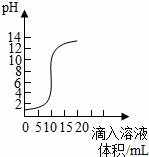
(2)根据图中曲线判断,该反应是将___ (填“氢氧化钙溶液”或“盐酸”)滴入另一溶液中.
|
|
| 20. | 详细信息 |
|
维生素C(C6H8O6)主要存在于 中,它能促进人体生长发育,增强人体对疾病的抵抗力。计算: (1)维生素C的相对分子质量 ; (2)维生素C中碳、氢两种元素的质量比 (写最简比); (3)维生素C中 元素的质量分数最大。
|
|
| 21. | 详细信息 |
|
金属材料与人类的生产和生活密切相关。请回答: (1)下列用品中,主要利用金属导电性的是 (填字母)。 A.铂金饰品 B.铁锅 C.铝导线 (2)为了验证铝、铜、银三种金属的活动性顺序,下列四种方案中可行的是 (填 序号)。 ①将铝、银分别浸入到硫酸铜溶液中 ②将银分别浸入到硫酸铝、硫酸铜溶液中 ③将铜、银分别浸入到硫酸铝溶液中 ④将铜分别浸入到硫酸铝、硝酸银溶液中 (3)在氯化铜和氯化亚铁的混合溶液中加入一定量的镁粉,充分反应后过滤,得到滤渣和滤液。①滤液中一定含有的溶质是 (填化学式);②向滤渣中滴加稀盐酸,有气泡产生,则滤渣中一定含有的物质是 (填化学式)。 (4)炼铁的原理是一氧化碳与氧化铁在高温条件下反应生成铁和二氧化碳,写出该反应的化学方程式 。 (5)露天放置的钢铁容易生锈,钢铁生锈实际是铁与空气中的 发生化学应, 若除去铁生锈可用稀盐酸请写出该反应的化学方程式 。 (6)工业生产中常用10%的稀盐酸来除铁制品表面的铁锈,实验室若要配制该盐酸200g,则需用量筒量取溶质质量分数为38%的浓盐酸(密度为1.19g/mL) mL(计算结果保留至0.1);实验室在配制10%的稀盐酸的过程中,除了用到量筒、胶头滴管外,还需要用到的玻璃仪器仪器有 。 (7)某钢铁厂每天需消耗4 900 t含Fe2O3 76%的赤铁矿石,该厂理论上可日产含Fe 98%的生铁的质量是 t。
|
|
| 22. | 详细信息 | ||||||
|
小婧同学在进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液滴加稀盐酸一会儿后,才发现忘记了滴加指示剂,因而无法确定盐酸与氢氧化钠是否恰好完全反应。为了证明这两种物质是否恰好完全反应,小婧从烧杯中取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液不变色。于是她得出“两种物质已恰好完全中和”的结论。 (1)你认为她的结论是否正确______,理由____________________________。 (2)写出该中和反应的化学方程____________________________________。 (3)请你另设计一个实验,探究上述烧杯中的溶液是否恰好完全中和,填写下表:
(4)综上所述,原溶液中的溶质只有 (填化学式),说明恰好中和。
|
|||||||
| 23. | 详细信息 |
|
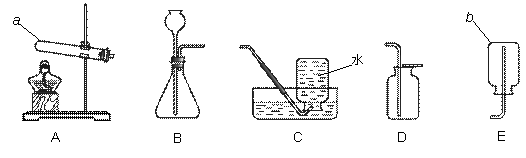
请结合下列实验装置,回答有关问题。
(2)实验室通过加热混有二氧化锰的氯酸钾固体制取氧气,在该反应中起催化作用的物质是 。 请写出实验室用高锰酸钾制取氧气的化学反应方程式 将装置A和C连接进行此实验,实验结束时,应先将导管移出水面,然后再熄灭 。 (3)实验室若用石灰石和稀盐酸制取并收集二氧化碳,选用的装置为 (填字母)。将二氧化碳通入盛有蒸馏水的试管中,该试管中溶液的pH 7(填“>”、“<”或“=”)。
|
|
| 24. | 详细信息 |
|
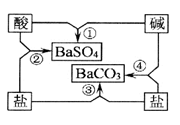
右图是常见酸、碱、盐之间的相互转化关系。 (1) 写出图中相应物质的化学式:酸 、碱 。
(2)写出图中反应②和④的化学方程式: ② ④
|
|
| 25. | 详细信息 |
|
80g质量分数为40%的氢氧化钠溶液与一定质量的氯化镁溶液混合,恰好完全反应,经过滤,得到滤液的质量为216.8g,请计算: (1)原氯化镁溶液中溶质的质量分数; (2)所得滤液中溶质的质量分数。(计算结果精确到0.1%)
|
|