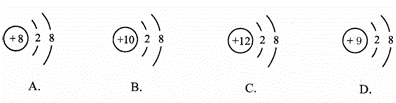广东省梅州市梅江区2018届九年级化学上学期第二次质检试题及答案
| 1. | 详细信息 |
|
下列叙述中不涉及到化学变化的是( ) A.使用火药 B.烧制陶瓷 C.粮食酿酒 D.制作石器
|
|
| 2. | 详细信息 |
|
某无土栽培的营养液中含有磷酸钾(K3PO4)。其中磷元素的化合价为 ( ) A. -3 B. +1 C. +3 D. +5
|
|
| 3. | 详细信息 |
|
.竹炭制品深受消费者欢迎,竹炭是竹子经过炭化处理后形成的多孔性材料,竹炭不具有的性质是 ( ) A. 黑色固体 B. 有吸附性 C. 易溶于水 D. 能够燃烧
|
|
| 4. | 详细信息 |
|
关于电解水实验的说法中正确的是( ) A. 实验证明水是由氢气和氧气组成的 B. 电解水时正极产生的是氧气 C. 水中氢、氧元素的质量比为2:1 D. 水分子是由氢分子和氧原子构成的
|
|
| 5. | 详细信息 |
|
下列关于碳单质的说法中正确的是 ( ) A. C60的相对分子质量为720 B.石墨很软,不能用于制石墨电极 C.木炭具有还原性,常温下可以将氧化铜中的铜还原出来 D.金刚石、石墨和C60都由碳元素组成,结构相同
|
|
| 6. | 详细信息 |
|
下列属于“空气污染指数”需要监测污染物是 ( ) A.氮气 B.二氧化碳 C.稀有气体 D.可吸入颗粒物
|
|
| 7. | 详细信息 |
|
地壳里含量最多的金属元素是 ( ) A.Fe B.O C.Al D.Si
|
|
| 8. | 详细信息 |
|
下列对于化学式“H20”的各种表述错误的是 ( ) A.表示水这种物质 B.表示水分子由氢元素和氧元素组成 C.表示1个水分子 D.表示1个水分子由2个氢原子和1个氧原子构成
|
|
| 9. | 详细信息 |
|
日常生活中见到的“加碘食盐”、“高钙牛奶”中的“碘、钙”应理解为 ( ) A.元素 B.原子 C.离子 D.分子
|
|
| 10. | 详细信息 |
|
在加压条件下,40m3的石油气(含丙烷、丁烷等气体)可以装入0.04m3的钢瓶中,这说明 ( ) A.分子的质量很小 B.分子由原子构成 C.分子在不断地运动 D.分子之间有间隔
|
|
| 11. | 详细信息 |
|
|
|
| 12. | 详细信息 |
|
下列四种物质中,属于化合物的是( ) A.河水 B.冰水混合物 C .自来水 D.液氧
|
|
| 13. | 详细信息 |
|
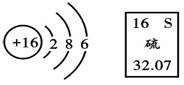
.根据右图的信息判断,下列说法正确的是 ( )
B.硫原子的核电荷数为16 C.硫原子的相对原子质量为32.07g D.在化学反应中,硫原子容易失去电子 |
|
| 14. | 详细信息 |
|
如图表示在一定条件下发生的某化学反应,则下列说法正确的是 ( )
B.该反应不符合质量守恒定律 C.该反应前后元素的种类发生了改变 D.两种反应物均为化合物
|
|
| 15. | 详细信息 | |||
|
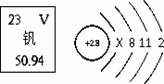
钒被誉为“合金中的维生素”。钒元素的部分信息如 “题15图”。请回答下列问题: (1)钒原子的质子数为__ _______ _,x=___________。 (2)钒属于__ _______ (填“金属”或“非金属”)元素; 钒的相对原子质量为__ _______ ____。 题15图
|
||||
| 16. | 详细信息 |
|
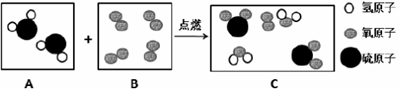
“题16图”是某反应的微观示意图。
题16图 请回答: (1)B框中的物质属于 (填序号:①化合物、②单质、③纯净物、④混合物)。 (2)此反应的化学方程式为 ,此图说明化学反应前后发生改变的微粒是 。
|
|
| 17. | 详细信息 |
|
用适当的数字和化学符号填空: (1)2个氢原子 (2)2个五氧化二磷分子 (3)氯化钠 (4)氧化镁中标出镁元素的化合价 (5)2个氮分子__________。
|
|
| 18. | 详细信息 |
|
铁丝在氧气里燃烧生成黑色的固体物质是 (填物质名称),反应的化学方程式是 ;在做这个实验时,应在盛氧气的集气瓶里预先放一些水或细沙,以防止 。
|
|
| 19. | 详细信息 |
|
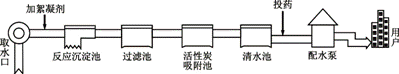
水是地球表面覆盖最多的物质,也是生命活动不可缺少的物质。 (1)写出实验室电解水反应的化学方程式: 。 (2)城镇自来水厂生产流程可用下图表示:
除去水中固态杂质的设备是 ;投药(多为ClO2)的作用是 。 (3)自然界的水多含有杂质。含有较多可溶性钙、镁化合物的水通常称为硬水,日常生活中用 区别软水和硬水;家庭生活中通过 方法降低水的硬度。
|
|
| 20. | 详细信息 |
|
某同学在敞口容器中做了两个实验:一是氧化汞(HgO)受热分解生成汞和氧气;二是铝粉在氧气中燃烧生成固体氧化铝。他准确称量了反应前后容器及所盛物质的质量,发现反应前后质量都发生了变化。请填空: (1)铝粉燃烧生成氧化铝的质量比参加反应铝粉的质量________(选填“大”、“小” 或“不变”)。 (2)你认为这两个反应是否遵循质量守恒定律?________(选填“是”或“否”)。 (3)请写出氧化汞受热分解的化学方程式________________________________。 (4)由质量守恒定律可知,化学反应前后,一定不变的是 。(填序号) ①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤元素种类 ⑥物质种类
|
|
| 21. | 详细信息 |
|
苯甲酸钠(C7H5O2Na)是一种食品添加剂,广泛用于食品工业中.请计算: (1)苯甲酸钠由 种元素组成;C7H5O2Na的相对分子质量是 。 (2)苯甲酸钠(C7H5O2Na)分子中碳、氢、氧原子个数比是 : : 。 (3)苯甲酸钠C7H5O2Na中,碳、氧两种元素的质量比是 : 。 (4)14.4g苯甲酸钠中含有钠元素质量是 g。
|
|
| 22. | 详细信息 | |||
|
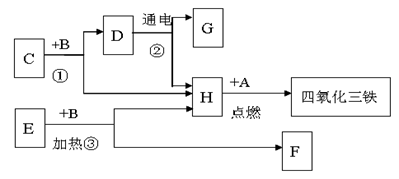
A~H都是初三化学前三个单元中的常见物质,A、B均为黑色粉末,C、D在常温时均呈液态,B和C混合立即产生大量的无色气体H,H能使带火星的木条复燃,加热E和B的混合物也有H气体生成,它们之间有如下的转化关系,且B在反应①和③中前后质量和化学性质均不变,试回答下列问题:
⑴ 写出下列物质的化学式。 A. D. G. F. ⑵ 写出E和B混合加热反应的化学方程式。 ___________________________________________
|
||||
| 23. | 详细信息 | |||||||||||||||||||||||||||
|
下图是实验室常用的实验装置,请回答有关问题:
A B C D E (1)装置C由导管、 和 (填仪器的名称)组成。装置A中试管口应放一团棉花,其作用是___________________________________________。 (2)用加热KMnO4的方法制取氧气,选用的发生和收集装置是 (填装置序号,下同);装入药品前,必须进行的第一步操作是________________________________。其反应的化学方程式是 ,该反应类型是 反应。 (3)若用大理石和稀盐酸来制取CO2,选用发生装置是 ,锥形瓶中应放的物质是 ,一般不用C装置收集CO2的原因是 。检验CO2的方法是 。(2分)
|
||||||||||||||||||||||||||||
| 24. | 详细信息 | ||||||||
|
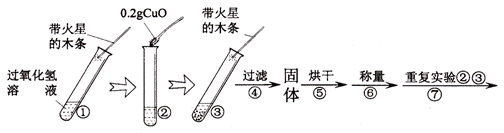
学习了MnO2对过氧化氢分 【猜想】Ⅰ、CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变。 Ⅱ、CuO参与反应产生O2 ,反应前后质量和化学性质发生了改变。 Ⅲ、CuO是反应的催化剂,反应前后 。 用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:
(1)填写下表:
(2)步骤①的目的是 。 (3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、 。 (4)过氧化氢能被CuO催化分解放出O2的化学方程式为 。
|
|||||||||
| 25. | 详细信息 |
|
化学兴趣小组为测定某石灰石样品中碳酸钙的质量分数,取26g石灰石样品放在烧杯中,然后向其中逐渐加入稀盐酸,使之与样品充分反应,恰好完全反应(杂质不参加反应)时,加入稀盐酸的质量为90g,反应后烧杯中物质的总质量为105g。 请计算: (1)反应生成二氧化碳的质量是 g。 (2)石灰石样品中碳酸钙的质量。
|
|