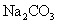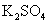2021-2022学年初中化学第十一单元练习试题含解析
| 1. | 详细信息 |
|
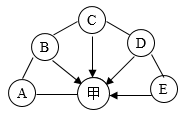
如图 A 、 B 、 C 、 D 、 E 是初中化学常见的单质、氧化物、酸、碱、盐五种不同类别的物质与甲物质的关系图,甲物质中两种元素的质量比为 3 : 8 , “ 一 ” 表示相连两物质能发生化学反应, “→” 表示一种物质一步转化成另一种物质。下列说法错误的是 A .固态的甲可以用于人工降雨 B .物质 D 可能为红色固体 C . A 一 B 的反应属于化合反应 D . A 和 C 两物质也可以发生化学反应 |
|
| 2. | 详细信息 |
|
明代宋应星所著的《天工开物》中记载: “ 西川有火井,事甚奇。其井居然冷水,绝无火气,但以长竹剖开去节,合缝漆布,一头插入井底,其上曲接,以口紧对釜脐,注卤水釜中,只见火意烘烘,水即滚沸。 ” 下列有关叙述错误的是 A . “ 火井 ” 中着火的物质属于可再生能源 B . “ 长竹剥开去节 ” 属于物理变化 C .文中涉及了蒸发结晶 D . “ 合缝漆布 ” 是确保气密性良好 |
|
| 3. | 详细信息 |
|
下列属于氮肥的是 A . CO ( NH 2 ) 2 B . HNO 3 C . NO 2 D . KNO 3 |
|
| 4. | 详细信息 |
|
宏观辨识与微观探析是化学学科的核心素养之一。对下列事实的微观解释不正确的是 A .氢气在氧气中燃烧生成水 —— 分子可分成原子,原子也可重新组合成新的分子 B .盐酸与碳酸盐反应会生成二氧化碳和水 —— 氢离子和碳酸根离子结合生成二氧化碳和水 C .氯化钠溶液中各部分密度和浓度都相同 —— 钠离子和氯离子在水中均匀分布 D .用湿润 pH 试纸测得某酸性溶液的 pH 值偏大 —— 稀释导致 H + 的数目减少,酸性减弱 |
|
| 5. | 详细信息 |
|
下列实验方案设计正确的是 A .用闻气味的方法鉴别硫酸钾和碳酸氢铵 B .用 pH 试纸测定正常雨水的 pH 值是否等于 5.6 C .在氧化铜中直接加入氢氧化钠溶液,可以制取氢氧化铜 D .除去氢氧化钠溶液中的氢氧化钡,可以加入过量的稀硫酸 |
|
| 6. | 详细信息 |
|
下列选项中各种溶质的溶液混合,无明显现象的是 A . NaOH 、 KCl 、 CuSO 4 B . KNO 3 、 AgNO 3 、 NaCl C . H 2 SO 4 、 K 2 SO 4 、 HNO 3 D . KCl 、 H 2 SO 4 、 Na 2 CO 3 |
|
| 7. | 详细信息 | |||||||||||||||
|
除去下列物质中的少量杂质,下列实验方案能达到目的的是
A . A B . B C . C D . D |
||||||||||||||||
| 8. | 详细信息 | ||||||||||||||||||
|
在一个密闭容器中放入 X 、 Y 、 Z 、 W 、 P 五种物质,在一定条件下发生化学反应,一段时间后,测得相关数据如下表,下列关于此反应的认识,正确的是
A . P 一定为该反应的催化剂 B .若 X 和 Y 为化合物,则该反应一定为复分解反应 C . m 的数值为 32 D .参加反应的 X 与 Y 的质量比为 1 : 4 |
|||||||||||||||||||
| 9. | 详细信息 |
|
氮肥可以促进作物茎、叶生长茂盛、叶色浓绿。下列关于尿素 [CO(NH 2 ) 2 ] 、碳酸氢铵、氯化铵、氨水 ( 通常含氨 17%) 的叙述正确的是 A .尿素、碳酸氢铵、氯化铵和氨水都属于铵态氮肥 B .氨水中含有大量的 OH - C .尿素是由 1 个碳原子、 4 个氢原子、 1 个氧原子和 2 个氮原子构成 D .四种氮肥中氯化铵的氮元素质量分数最高 |
|
| 10. | 详细信息 |
|
尿素 CO ( NH 2 ) 2 是一种重要的化学肥料,下列关于尿素的说法正确的 A .尿素属于复合肥 B .尿素中含有氢分子 C .氢、氮元素的质量比为 1:14 D .氮元素的质量分数最大 |
|
| 11. | 详细信息 | |||||||||||||||
|
下列实验方案不能达到实验目的的是
A . A B . B C . C D . D |
||||||||||||||||
| 12. | 详细信息 |
|
下列物质暴露在空气中,质量不会发生变化的是 A .浓 H 2 SO 4 B .生石灰 C .铁钉 D .石灰石 |
|
| 13. | 详细信息 |
|
下列物质,只用水无法鉴别的是 A . C . CaO 、 |
|
| 14. | 详细信息 |
|
下列各组溶液,需要添加其他试剂才能鉴别的是 A . HCl 、 CuSO 4 、 NaOH 、 NaCl B . K 2 SO 4 、 Na 2 CO 3 、 BaCl 2 、 HCl C . Na 2 CO 3 、 H 2 SO 4 、 HCl 、 NaNO 3 D . NaOH 、 NaCl 、酚酞、 HCl |
|
| 15. | 详细信息 |
|
在硫酸铜和硫酸的混合溶液中硫元素的质量分数占 9.6% ,向 100g 该混合溶液中加入 100g 氢氧化钠溶液恰好完全反应,下列分析不正确的是 A .反应后所得溶液中溶质的质量分数为 21.3% B .氢氧化钠溶液中钠元素质量为 13.8g C .氢氧化钠溶液中溶质的质量分数为 24% D .生成氢氧化铜沉淀的质量一定小于 29.4g |
|
| 16. | 详细信息 |
|
将铁粉加到一定量 AgNO 3 、 Cu(NO 3 ) 2 的混合溶液中,充分反应后过滤,所得滤渣中有红色固体,有以下四种说法: ① 向滤液中加盐酸,可能有白色沉淀 ② 滤液中可能只有 Cu 2+ 、 ③ 向滤渣中加盐酸,可能有气泡 ④ 所得滤液的质量一定比原混合液质量小 其中正确的是 A . ①② B . ①③ C . ③④ D . ②④ |
|
| 17. | 详细信息 |
|
推理是化学学习常用的思维方法,下列有关推理正确的是 A .氯化钠、碳酸钙等盐中都含有金属元素,所以盐中一定含有金属元素 B .碳酸盐能和酸反应产生气体,所以能和酸反应产生气体的物质一定是碳酸盐 C .中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 D .分子、原子都是不带电的微粒,但不带电的微粒不一定都是分子、原子 |
|
| 18. | 详细信息 |
|
下列俗名、化学名称、化学式对应正确的是 A .纯碱、氢氧化钠、 NaOH B .熟石灰、氢氧化钙、 Ca ( OH ) 2 C .生石灰、碳酸钙、 CaCO 3 D .水银、汞、 Ag |
|
| 19. | 详细信息 |
|
在阳台上用营养液进行无土栽培蔬菜,己成为城镇居民 “ 亲近自然,享受绿色生活 ” 的家庭时尚。下列化肥属于复合肥的是 A . K 2 SO 4 B . Ca 3 ( PO 4 ) 2 C . CO ( NH 2 ) 2 D . NH 4 H 2 PO 4 |
|
| 20. | 详细信息 |
|
下列物质或试剂在空气中敞口放置,因发生化学变化溶液质量减小的是 A .浓盐酸 B .氯化钠溶液 C .氢氧化钠溶液 D .澄清石灰水 |
|
| 21. | 详细信息 |
|
向一定质量的 Fe 2 O 3 中滴加稀盐酸,一段时间后,改为滴加 NaOH 溶液。固体质量随加入试剂质量的变化趋势如图所示: (1)a 点对应的现象是 ______ 。 (2)b 点对应的溶液的 pH 值 ______7 (填 “>” 或 “<” 或 “=” )。 (3)c 点对应的化学反应方程式是 ______ 。 (4)d 点时溶液中含有的溶质是 ______ 。 |
|
| 22. | 详细信息 |
|
生活中处处有化学知识,请根据题意回答相关问题 (1) 新型冠状病毒蔓延期间,为做好自我防护,要佩戴符合要求的口罩。活性炭口罩能有效阻隔氨、苯、甲醛等有害气体,因为活性炭具有 ______ 性。 (2) 电器着火,下列做法正确的是 ______ 。 A .用水浇灭 B .用干粉灭火器灭火 C .用湿棉被覆盖住电器 D .立即打开所有门窗 (3) 中药 “ 石灰 ” 是由生石灰和熟石灰混合而成,具有解毒蚀腐,敛疮止血、杀虫止痒的功效,写出生石灰变成熟石灰的反应方程式 ______ 。 |
|
| 23. | 详细信息 |
|
人类的衣、食、住、行都离不开化学,从所给的物质中选择一种填空 ( 填序号 ) : ① 氯化钠 ② 氮气 ③ 熟石灰 ④ 赤铁矿 ⑤ 盐酸 (1) 常用的食品调味剂是 ______________ 。 (2) 工业上高炉炼铁的原料之一是 ________________ 。 (3) 能用作食物保护气的是 ________________ 。 (4) 农业上改良酸性土壤的是 ______________ 。 (5) 人体中胃液中的酸 ______________ 。 |
|
| 24. | 详细信息 |
|
请根据所学知识回答下列问题。 (1) 用 pH 试纸测定白醋的酸碱度时,先用蒸馏水润湿试纸则测得结果与实际值相比 _________ (填 “ 偏大 ”“ 偏小 ” 或 “ 不变 ” )。 (2) 常见的酸如硫酸、盐酸等,它们有很多相似的化学性质的原因是在它们的水溶液里存在有相同的 __________ (填化学符号)。 (3) 金刚石和石墨物理性质差别大的本质原因是 ___________ 。 (4) 硫酸铬 [Cr 2 ( SO 4 ) 3 ]常用于印刷、陶瓷、制革等工业。硫酸铬溶液与氢氧化钠溶液能发生复分解反应,请你分析其原因是 ___________ 。 |
|
| 25. | 详细信息 |
|
在 H 、 O 、 C 、 S 、 Cl 、 Na 、 Ca 七种元素中选择适当的元素组成符合下列要求的物质,将化学式填入相应的空格中。 (1) 能导致人中毒的碳的氧化物 _________ 。 (2) 可用作干燥剂的酸 ___________ (写溶质的化学式)。 (3) 可用作补钙剂的盐 ___________ 。 |
|
| 26. | 详细信息 |
|
元素周期表是化学学习和研究的重要工具。如图是元素周期表的一部分。 (1) 从表中查出硅 (Si) 元素的相对原子质量为 ___________ ; (2)3 ~ 11 号元素中有 ________ 种属于金属元素。 (3) 位于第三周期第三族的元素的离子符号为 _________ 。 (4) 写出由五个原子构成且含有 10 个质子的分子的物质是 __________ (写名称)。 (5) 由原子序数为 8 、 11 、 16 三种元素组成的盐是 ________ (写化学式)。 |
|
| 27. | 详细信息 |
|
元素周期表是学习和研究化学的重要工具。下表是元素周期表的前三周期,完成下列问题。 (1) 画出 ④ 的原子结构示意图 ______ 。 (2)② 和 ⑤ 对应的单质相比, ______ (填序号)稳定。 (3) 写出由 ①③④ 元素组成盐的化学式 ______ 。 |
|
| 28. | 详细信息 |
|
化学知识与我们的生产生活息息相关,请从下列物质中选择相应字母填空。 A .明矾 B .氧气 C .石油 D .氦气 E. 小苏打 F. 石灰石 (1) 可作建筑材料的是 _________ 。 (2) 可支持燃烧的是 _________ 。 (3) 可作净水剂的是 ___________ 。 (4) 可作发酵粉的是 _________ 。 (5) 属于化石燃料的是 _________ 。 (6) 可作电光源的是 _________ 。 |
|
| 29. | 详细信息 |
|
为除去粗盐溶液中含有的少量 CaCl 2 、 MgCl 2 和 Na 2 SO 4 等可溶性杂质,得到纯净的 NaCl 某化学实验小组依次进行如下操作: ① 加入过量的氢氧化钡溶液 ② 加入过量的碳酸钠溶液 ③ 过滤 ④ 加适量稀盐酸 ⑤ 蒸发结晶。 (1) 写出操作 ① 中加入氢氧化钡溶液时反应的化学方程式 _____ 。 ( 写出一个即可,且微溶物不形成沉淀 ) (2) 请说明操作 ④ 中加入适量稀盐酸的作用 ______ 。 (3) 用所得纯净的 NaCl 配制 50g 溶质质量分数 2% 的氯化钠溶液,量取水时俯视量筒读数,对结果会造成什么影响? _____ 。 |
|
| 30. | 详细信息 |
|
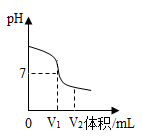
如图是氢氧化钠溶液与硫酸反应时,某化学小组利用数字化传感器测得反应过程中溶液 pH 变化的示意图。 (1) 写出有关反应的化学方程式 ______ 。 (2) 滴入溶液体积为 V 2 mL 时,为确定溶液中的溶质成分,加入氯化钡溶液行吗, ____ 说明理由 _____ 。 |
|