2018天津九年级上学期人教版初中化学月考试卷
| 1. | 详细信息 |
|
下列古代文明或工艺一定包含化学变化的是( ) A.在甲骨上刻文字 B.指南针指引航海 C.用泥土烧制陶瓷 D.用石块修筑长城
|
|
| 2. | 详细信息 |
|
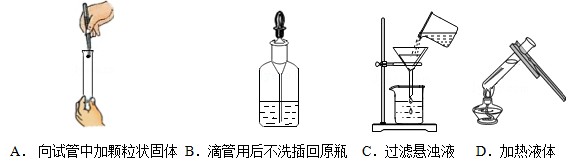
下列实验操作正确的是( )
|
|
| 3. | 详细信息 |
|
下列现象,可用分子的知识加以解释,其中正确的是( ) A.品红在水中扩散是因为分子在不断运动 B.温度计中的水银热胀冷缩是因为分子间间隔随温度变化而改变 C.水变成冰后水分子不再运动 D.气体易被压缩是因为气体分子间的间隔很小
|
|
| 4. | 详细信息 |
|
下列关于物质的性质和用途说法不正确的是( ) A.氮气用来保护粮食,是利用氮气常温下化学性质稳定 B.氧气用于火箭发射,是利用氧气的可燃性 C.稀有气体充入霓虹灯,是利用稀有气体通电能发出不同颜色的光 D.液氮可用于冷冻麻醉,是利用液氮气化时能吸收大量的热量
|
|
| 5. | 详细信息 |
|
某学生用量筒量取液体,将量筒平放且面对刻度线,初次仰视量筒内液体的凹液面, 读数为 a mL;随后又倒入部分该液体后,向下俯视凹液面最低处,读数为 b mL,则该学 生第二次倒入液体的实际体积是( ) A.大于(b-a)mL B.等于(b-a)mL C.小于(b-a)mL D.无法确定
|
|
| 6. | 详细信息 |
|
2017 年 5 月 9 日,中国科学院发布了 113 号、115 号、117 号及 118 号四种元素的 中文名称,其中一种元素在元素周期表中的信息如图所示,下列有关该元素说法错误的是
|
|
| 7. | 详细信息 |
|
我国古代典籍中有”银针验毒”的记载,“银针验毒”的反应原理之一是 4Ag+2H2S +O2=2X+2H2O。下列有关该反应的说法不正确的是( ) A.反应属于氧化反应 B.X 的化学式是 Ag2S C.反应前后元素的种类不变 D.反应前后所有元素的化合价都发生了变化
|
|
| 8. | 详细信息 |
|
下列说法错误的是( ) A.由一种元素的阳离子和另一种元素的阴离子构成的物质不一定是纯净物 B.核外电子总数相等的粒子一定是同一种元素 C.在化学变化中,分子可分原子不可再分,而离子可能再分 D.化学变化中,一定有新的粒子生成
|
|
| 9. | 详细信息 |
|
右图可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,下列说法中正确 的是( )
|
|
| 10. | 详细信息 |
|
水是生命之源,下列有关水的说法正确的是( ) A.水是由氢原子和氧原子构成 B.明矾可以使硬水转化为软水 C.蒸馏海水和电解水的过程中水发生的都是物理变化 D.爱护水资源主要从节约用水和防治水体污染两方面采取相应措施
|
|
| 11. | 详细信息 |
|
逻辑推理是学好化学的重要思维方法,下面是从小明同学学习笔记中摘录出来的一些 推理,你认为正确的是( ) A.氧化物中含有氧元素,所以含有氧元素的物质就是氧化物 B.由同种分子构成的物质是纯净物,所以纯净物一定由同种分子构成 C.同种元素的原子具有相同的质子数,所以具有相同质子数两种粒子一定是同种元素 D.当元素原子的最外层电子数达到 8 个电子时,元素的化学性质比较稳定,氖原子核外 最层电子数为 8,所以氖气的化学性质比较稳定
|
|
| 12. | 详细信息 |
|
扑尔敏(化学式为 C20H23ClN2O4)是最常见的抗过敏药,关于扑尔敏的说法错误的是 ( ) A.扑尔敏分子由 C、H、Cl、N、O 五种元素组成 B.扑尔敏中元素质量分数由大到小排在第二位的是氧元素 C.扑尔敏分子由 20 个碳原子、23 个氢原子、1 个氯原子、2 个氮原子和 4 个氧原子构成 D.该分子中碳、氢、氧原子个数比为 20:23:4
|
|
| 13. | 详细信息 |
|
.现有 CH4 和 C2H6(乙烷)组成的可燃性混合气体,该混合气体中碳元素的质量分数 可能是( ) A.65% B.70% C.78% D. 90%
|
|
| 14. | 详细信息 |
|
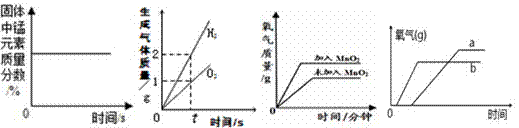
下列四个图像,能正确反映对应变化关系的是( ) A B C D A.加热一定量的高锰酸钾固体 B. 将水通电电解一段时间 C.用等质量、等浓度的双氧水制取氧气 D.加热两份质量相等的固体 a 和 b,a 是氯酸钾固体,b 是氯酸钾和二氧化锰的混合物
|
|
| 15. | 详细信息 |
|
下列对实验现象的描述错误的是( ) A.碳在氧气中燃烧发出白光,生成二氧化碳气体 B.镁在空气中燃烧发出耀眼的白光,生成白色固体 C.细铁丝伸入盛氧气的集气瓶中剧烈燃烧,火星四射,生产黑色固体 D.硫在空气中燃烧,发出淡蓝色火焰,生成有刺激性气味的气体
|
|
| 16. | 详细信息 |
|
用化学用语填空: (1)2 个亚铁离子 ; (2)保持氨气化学性质的最小粒子 ; (3)氯酸钾中氯元素的化合价 ; (4)3 个氮分子 ; (5)地壳中含量最高的金属元素与非金属元素,以及空气中含量最高的元素一起形成的 化合物是 .
|
|
| 17. | 详细信息 |
|
根据物质组成种类的多少可以把物质分为纯净物和混合物;而根据纯净物中 组成元素的多少又可以分成单质和化合物。现有以下物质:(用序号填空) ①生理盐水 ②液氮 ③干冰 ④高锰酸钾受热完全分解后的剩余固体物质 ⑤氯化钾 ⑥锰酸钾 ⑦稀有气体 ⑧冰水混合物 ⑨水银 ⑩胆矾 (1)属于混合物的是 (2)属于纯净物的是 (3)属于化合物的是 (4)属于单质的是 (5)属于氧化物的是
|
|
| 18. | 详细信息 |
|
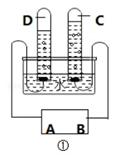
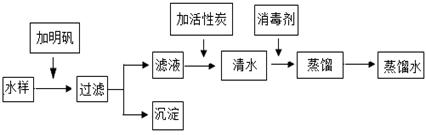
格. (1)图①所示为电解水实验,该实验说明水是由氢、氧元素组成的,该反 应的化学方程式是 。B 是电源的 极,试管 (填“C”或“D”)中的气体能燃烧,在点燃它之前需要 。 小明同学去旅游时,用瓶装了一些山泉水带回实验室,在老师的指导下按 下列流程进行实验,制取蒸馏水。
(2)小明进行过滤操作时,玻璃棒的作用是 ,下列做法错误的是 。 A.玻璃棒要靠在三层滤纸的一边 B.漏斗下端的管口要紧靠烧杯的内壁 C.滤纸的边缘要低于漏斗口 D.液面不要低于滤纸边缘 (3)向滤液中加入活性炭,利用其 性,除去水样中的色素和异味。 (4)检验水是硬水还是软水可用的物质是 。生.活.中将硬水软化常用的方法是 。清水中加消毒剂引起的变化属于 (填“物理”或“化 学”)变化。 (5)絮凝剂明矾在净水过程中作用是 明矾[其化学式为 KAl(SO4)2 ·12H2O]的相对分子质量为 ,明矾能与水反应生成氢氧化铝胶状物, 氢氧化铝的化学式为 。 (6)天津是一个严重缺水的城市,我们应当珍惜每一滴水。下列说法不利于节水的是 。 A.洗菜水浇花 B.使用节水龙头 C.用不间断的水刷碗 D.洗手擦肥皂时,关上水龙头
|
|
| 19. | 详细信息 |
|
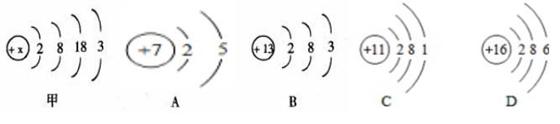
化学是在原子、分子水平上研究物质及其变化的科学。 (1)已知镓( Ga)的原子结构示意图如下图(甲)所示,则 x 的值为 ; (2)镓元素的化学性质与下列哪种元素的化学性质最相似 (在 A、B、C、D 图 中选择,填字母); (3)A、B、C、D 图示的四种元素最本质的区别是 ; (4)镓( Ga)与下图中 A 元素形成的化合物化学式为 ; (5)D 的离子结构示意图是 ,C 和 D 这两种元素组成的化合物是由 (填“原子”、“分子”或“离子”)保持化学性质的。
|
|
| 20. | 详细信息 |
|
由于铁丝在氧气中高温燃烧,部分熔化的铁没有及时反应便熔入到生成物 中。得到的黑色固体为 Fe3O4 和 Fe,若实验后,测定瓶底黑色固体中氧元素质量分数为 24%。则黑色固体中没有反应的铁质量占原铁丝质量约为 。(保留到 0.1%)
|
|
| 21. | 详细信息 |
|
写出下列反应的化学方程式 (1)高锰酸钾制氧气 (2)生成相对分子质量最小的氧化物的化合反应 (3)红磷燃烧
|
|
| 22. | 详细信息 |
|
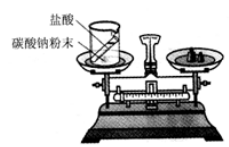
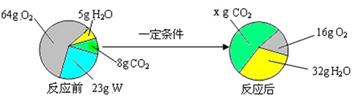
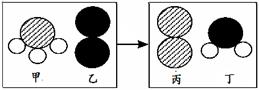
(1)甲组同学设计了如右图实验,图中试剂混合前后物质 的总质量分别表示为 m(前)、m(后)。 请根据图示回答: 甲组实验中,m(前)>m(后),原因是 ,若所用试剂不变,改进的 方法是 。 从微观的角度分析,化学变化中存在质量守恒定律的本质原因是 (2)乙组同学研究了物质 W 的组成。一定条件下,W 在密闭容器内发生反应前后各物质
其中,x= g, W 的化学式是 。
A.反应前后共有 4 种原子 B. B.该反应有单质生成 C.反应前后元素化合价都不变 D.化学变化中分子和原子均可再分 E. 该化学反应中,甲、丁两种分子的个数比是 2∶3
|
|
| 23. | 详细信息 |
|
如图是兴农化肥厂包装袋标签上的部分文字(假设该化 肥中杂质不含氮元素)。请你通过计算填空: (1)尿素中碳、氮、氧、氢元素的质量比是 。 (2) 克 CO(NH2)2 与 40克 NH4NO3 含氮量相等?
|
|
| 24. | 详细信息 |
|
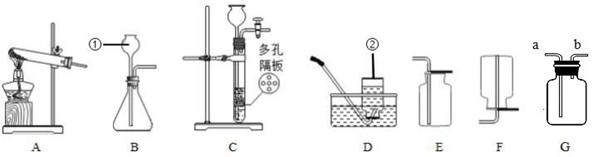
下列装置是实验室常用气体制备装置,据图回答问题:
(1)写出编号为①、②的仪器名称 、 (2)实验室制备气体时,应对装置先 ,选用 A 装置做制取氧气的发生装置,发 生反应的化学方程式为 。若选用装置 E 的方法收集氧气,则判断氧气 已收集满的方法是 。 (3)实验室用过氧化氢溶液和二氧化锰制备较纯净的氧气时,应选的收集装置为 (填字母),发生反应的化学方程式是 。该实验不能选择 C 装置作为发生装置的原因是 。二氧化锰在该反应中起 而使得反应很剧烈,据此提出实验安全注意事项或改进措施是 。(请 填写序号) ①改用能控制滴液速度的仪器; ②用小体积的锥形瓶; ③加热反应物; ④降低反应物浓度 (4)实验室制取氢气的化学反应原理是 ,若选用 C 作为氢 气的发生装置其优点是 _ _。当 G 装置中盛满水,氢气从 (填“a”或“b”)端导入,另外一端再加配 (填一种仪器名称)就 可以达到收集并测量氢气体积的目的。 (5) 在实验室里可用硫化亚铁固体和稀硫酸的反应来制取硫化氢气体,同时还生成了一 种在溶液中呈浅绿色的硫酸盐。该反应的化学方程式为 。在 通常情况下硫化氢是一种无色、有臭鸡蛋气味的有毒气体,密度比空气大且能溶于水。实 验室制取硫化氢应选择 (填字母)作为收集装置,并在通风橱中进行操作,还要 有尾气处理装置。
|
|
| 25. | 详细信息 | ||||||||||||||||||||
|
某兴趣小组同学对实验室制备氧气的条件进行如下探究实验。 (1)为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比实验: Ⅰ.将 x g KClO3 与 1.0 g MnO2 均匀混合加热; Ⅱ.将 3.0 g KClO3 与 1.0 g CuO 均匀混合加热在相同温度下,比较两组实验产生 O2 的 快慢。Ⅰ中 x 的值应为 ; (2)乙探究了影响双氧水分解速度的某种因素。实验数据记录如下:
上表格中要比较出Ⅰ、Ⅱ、Ⅲ三个实验的分解速度快慢,需要测定的是有关什么方面 的实验数据? 。
|
|||||||||||||||||||||