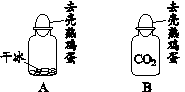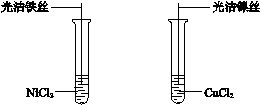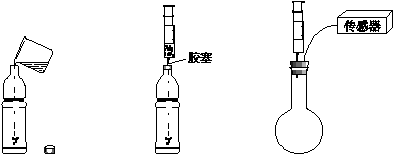北京市某中学2017届九年级化学下学期综合练习(二模)试题及答案
| 1. | 详细信息 |
|
A. 氧气 B. 氮气 C. 二
|
|
| 2. | 详细信息 |
|
下列是4种矿石(括号中为主要成分),其主要成分属于单质的是
铝土矿 金矿 白钨矿 辉铜矿 (Al2O3) (Au) (CaWO4) (Cu2S) A.铝土矿 B.金矿 C.白钨矿 D.辉铜矿
|
|
| 3. | 详细信息 |
|
下列金属中,不能与稀盐酸发生反应的是 A.Fe B.Cu C.Al D.Mg
|
|
| 4. | 详细信息 |
|
下列 A.可乐 B.食醋 C.牛奶 D.蒸馏水
|
|
| 5. | 详细信息 |
|
吸烟有害健康。原因之一是,香烟燃烧时能产生一种与血红蛋白结合能力很强的有毒气体,此气体是 A. H2 B.N2 C.CO2 D.CO
|
|
| 6. | 详细信息 |
|
废弃的易拉罐和塑料瓶属于 A.厨余垃圾 B.其他垃圾 C.可回收物 D.有害垃圾
|
|
| 7. | 详细信息 |
|
下列物质在氧气中燃烧,火星四射、生成黑色固体的是 A.木炭 B.铁丝 C.蜡烛 D.红磷
|
|
| 8. | 详细信息 |
|
下列食品中,富含蛋白质的是 A.橄榄油 B.蔬菜 C.米饭 D.牛肉
|
|
| 9. | 详细信息 |
|
下列微粒中,能表示2个氢原子的是 A.2H B.2H+ C.H2O D.2H2
|
|
| 10. | 详细信息 |
|
下列物质的用途中,只利用了其物理性质的是 A. 干冰用于人工降雨 B. 二氧化碳用作灭火 C. 盐酸用于金属表面的除锈 D. 氧气用于炼钢
|
|
| 11. | 详细信息 |
|
将密封良好的方便面从平原带到高原时,包装袋鼓起,是因为袋内的气体分子 A.质量增大 B.间隔增大 C.体积增大 D.个数增多
|
|
| 12. | 详细信息 |
|
用H2O、HgO、H2O2三种物质都可制得氧气,说明这三种物质的组成中都含有 A.氧元素 B.氧气 C.氧分子 D.氧离子
|
|
| 13. | 详细信息 | ||||
|
工业常用电解熔融Al2O3的方法冶炼铝,化学方程式为2Al2O3 A.化合反应 B.置换反应 C.分解反应 D.复分解反应
|
|||||
| 14. | 详细信息 |
|
.下图是元素周期表中的一格,依据图中的信息得到的下列认识不正确的是
B.该元素属于金属元素 C.该元素一个原子的原子核外有33个电子 D.该元素的相对原子质量为74.92
|
|
| 15. | 详细信息 |
|
已知:H2 + Cl2 A.分子的种类 B.原子的种类 C.分子的个数 D.各元素的质量
|
|
| 16. | 详细信息 |
|
能将烧碱溶液和澄清石灰水区分开来的是 A.紫色石蕊溶液 B.碳酸钠溶液 C.盐酸 D.无色酚酞溶液
|
|
| 17. | 详细信息 |
|
导电陶瓷是一种新型陶瓷,除能导电外,还具有耐高温、抗氧化、抗腐蚀等性能,广泛用作航天器、发动机的绝热材料。按陶瓷中导电的物质不同,有氧化锆(ZrO2)、二硅化钼(MoSi2)、碳化硅(SiC)、铬酸镧(LaCrO3)等类型。下列叙述不正确的是 A.导电陶瓷的化学性质稳定 B.铬酸镧是由三种元素组成 C.碳化硅中硅、碳元素的质量比为7:3 D.上述导电物质中属于氧化物的是ZrO2、MoSi2
|
|
| 18. | 详细信息 |
|
.从化学方程式4P+5O2 A.①② B.①③ C.①②③ D.②③
|
|
| 19. | 详细信息 |
|
右图是甲、乙两种固体物质的溶解度曲线。下列说法正确的是 A.t1℃时,甲的溶解度大于乙的溶解度 B.加入甲或升温都可以使接近饱和的甲溶液变 为饱和溶液 C.t2℃时,甲、乙各40 g分别加入到100g水中, 均能得到不饱和溶液 D.t2℃时,甲、乙各40 g分别加入到100g水中, 再升温至t3℃,两种溶液中溶质质量分数相等
|
|
| 20. | 详细信息 | ||||||||
|
.已知:Ca(HCO3)2
|
|||||||||
| 21. | 详细信息 |
|
用铁锅加工食品能为人体提供一定量的铁元素,对预防 有辅助作用。铁锅清洗后一般要擦干放置,可以减少 对铁锈蚀的影响。
|
|
| 22. | 详细信息 | ||||||
|
下表是
(1)除垢净使用过程中不能接触铁制品表面,其原因是 。 (2)强力去油剂使用时需要戴上橡胶手套,其原因是 。 (1)盐酸和铁反应腐蚀铁制品 (2)氢氧化钠有强腐蚀性 (1分)碳酸氢钠可用作抗酸药,中和胃里过多的盐酸,其原理是 (用化学方程式表示)。
|
|||||||
| 23. | 详细信息 |
|
燃料燃烧需要氧气,说明氧气具有的性质是 。
|
|
| 24. | 详细信息 | ||||
|
水常用来配制溶液。 请从27-A或27-B两题中任选1个作答,若两题均作答,按27-A计分。
能源、环境与人类的生活和社会发展密切相关。请回答28~30题。
|
|||||
| 25. | 详细信息 |
|
氢气被认为是最理想的清洁燃料,用化学方程式表示其原因______。
|
|
| 26. | 详细信息 |
|
汽车尾气中含有多种有害物质,带来很大的环境问题,其中二氧化硫带来的主要环境问题是______。
|
|
| 27. | 详细信息 |
|
乙炔(C2H2)气体常用于气焊和气割。乙炔可以通过电石(主要成分为CaC2)与水反应制取,反应的化学方程式为:CaC2 + 2H2O === Ca(OH)2 + C2H2↑。若含CaC2 64 kg的电石完全反应,可制取乙炔的质量为______ kg。 实践活动能开拓视野、创设独立思考和动手实践的机会,请
|
|
| 28. | 详细信息 |
|
某校同学在社会实践活动中去参观某生态农庄。
图1 图2 (1)生态农庄街道旁的路灯(如图1)每天有短时间光照就能使用,该路灯使用的新能源是 。 (2)下列农庄里使用的材料,属于有机合成材料的是 (填序号)。 A.农庄大门使用的原木 B.牲畜圈使用的铁质栏杆 C.蔬菜大棚使用的塑料膜 (3)农庄内将牲畜粪便、秸杆等发酵制得沼气(如图2),沼气的主要成分为甲烷,甲烷燃烧的化学反应方程式为 。
|
|
| 29. | 详细信息 |
|
实践课中,同学们进行了如下2个活动。
活动1 会动的鸡蛋 活动2 滴水生火 (1)活动1:如图A,向装有干冰的集气瓶中加入热水,观察到有大量白雾产生,鸡蛋在瓶口跳动,该实验说明干冰具有的性质是 。如图B,向充满CO2的瓶中加入少量氢氧化钠溶液,观察到瓶口的鸡蛋被吞入瓶中,其原因是 。 (2)活动2:用棉花包住少量过氧化钠(Na2O2)粉末,放在石棉网上,向棉花上滴水,观察到棉花发生燃烧。根据现象推知,过氧化钠与水能生成氧气并 。
|
|
| 30. | 详细信息 |
|
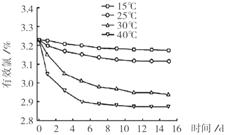
阅读下面科普短文。 1984年,地坛医院的前身北京第一传染病医院成功研制能迅速杀灭各类肝炎病毒的消毒液,定名为“84肝炎洗消液”,后更名为“84消毒液”。“84消毒液”是一种以次氯酸钠(NaClO)为主的高效消毒剂,呈无色或淡黄色液体,且具有刺激性气味,有效氯含量为5.5~6.5%。被广泛用于宾馆、旅游、医院、食品加工行业、家庭等场所的消毒。 空气中的CO2可以与NaClO反应得到次氯酸(HClO),反应的化学方程式为NaClO+CO₂+H₂O === NaHCO₃+HClO。HClO是一种比碳酸还弱的酸,但其具有极强的氧化性,能够将很多物质氧化,使其变性,因而能够起到消毒的作用。 NaClO不稳定,下图是对其稳定性的研究结果。
图1 温度对次氯酸钠溶液稳定性的影响 图2 pH对次氯酸钠溶液稳定性的影响 “84消毒液”在使用过程中要注意以下几点: ① 需25℃以下避光保存,宜现用现配,一次性使用,勿用50℃以上热水稀释。 ② 有一定的刺激性与腐蚀性,必须稀释以后才能使用,使用时应戴手套,避免接触皮肤,对金属有腐蚀作用。 ③ 漂白作用较强,对织物有漂白作用,慎用。如果浅色衣服染上其他颜色,也可以用其进行漂白。 ④ “84消毒液”是含氯消毒剂,消毒时容器必须加盖盖好,否则达不到消毒的效果。 ⑤ 不要把“84消毒液”与其他洗涤剂或消毒液混合使用,因为这样会加大空气中氯气的浓度而引起氯气中毒。 准确了解和正确使用各类清洁剂可以为我们创造一种健康、安全、方便的生活。 依据文章内容,回答下列问题: (1)“84消毒液”能够消毒的原因是______。 (2)勿用50℃以上热水稀释的原因是______。 (3)“84消毒液”除能够消毒,还具有的用途是______。 (4)下列有关“84消毒液”的说法中,正确的是 (填序号)。 A.对金属没有腐蚀作用 B.消毒时容器必须加盖盖好是因为易挥发出含氯物质 C.不要与其他洗涤剂或消毒剂混合使用是因为避免产生有毒的氯气 (5)对NaClO稳定性的研究结果是______。
|
|
| 31. | 详细信息 |
|
二氧化氯(ClO2)在生产、生活中具有广泛应用。 (1)ClO2可 ① ClO2中氯元素的化合价为 。 ② 工业生产NaClO2的主要反应的化学方程式为2ClO2+2X 通电 Cl2+2NaClO2,其中X的化学式为 。 (2)ClO2是国际上公认的安全、无毒的消毒剂,可以快速将剧毒的氰化物氧化。ClO2 与氰化氢(HCN)在气态下反应的微观示意图如下:
该反应生成的N2与CO
|
|
| 32. | 详细信息 |
|
按照如图所示进行中和反应实验。
(2)向烧杯中逐滴滴入盐酸至过量,在这个过程中,能够说明盐酸与氢氧化钠发生了化学反应的实验现象是 。 (3)实验后溶液pH (填“小于”“等于”或“大于”)7。
|
|
| 33. | 详细信息 | |||
|
我国发行的第五套人民币中,铸造1元、5角和1角硬币的主要材料含有铁、 镍(Ni)、铜等。 (1)选择铁、镍、铜等金属作为铸造硬币的原料,主要考虑的因素有 (答出一条即可)。 (2)如下图所示实验,观察到铁丝和镍丝表面均有固体析出,则上述三种金属的活动性由强到弱的顺序为 。
空气和水是人类宝贵的自然资源。请回答25~27题。
|
||||
| 34. | 详细信息 | |||
|
根据下图回答问题。
(1)实验室制取二氧化碳的化学方 (2)利用高锰酸钾制取氧气选用的发生装置是 (填序号),反应的化学方程式为 。
|
||||
| 35. | 详细信息 | |||
|
根据下图回答问题。
A B C (1)A处发生反应的化学方程式为 。 (2)观察到A和B两处的实验现象分别是 。 (3)实验时点燃C处酒精灯的目的是 。
|
||||
| 36. | 详细信息 | |||
|
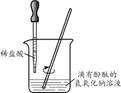
利用下图进行粗盐中难溶性杂质去除和配制一定质量分数氯化钠溶液的实验。
A.称量 B.溶解 C.蒸发 D.过滤 E.量取 (1)粗盐中难溶性杂质去除的主要操作顺序为 (选填序号)。
(3)配制l00 g溶质质量分数为10%的氯化钠溶液。如右图量取蒸馏水,最终会导致配制的溶液中溶质质量分数 (填“大于”或“小于”)10%。
|
||||
| 37. | 详细信息 | ||||||
|
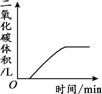
某化学小组同学用下图所示的三套装置进行二氧化碳性质的探究。 已知:15℃、101kPa下,1体积水约能溶解1体积的二氧化碳。
A B C (1)A和B中的塑料瓶容积相同,且充满CO2。将A的瓶盖打开,加入体积约为塑料瓶容积1/3的蒸馏水,旋紧瓶盖后充分振荡;向B中注入等体积的蒸馏水,充分振荡。 ① A中观察到的实验现象是_____。 ② B中塑料瓶无明显变化,其原因是_____。 (2)C装置用传感器测量瓶内气压变化。 ① 某同学检验C装置气密性时,进行了 ② 在圆底烧瓶中充满CO2,通过注射器向瓶中注入液体。下图乙是C装置测定的加入同体积水和氢氧化钠溶液的气压变化图像,其中表示氢氧化钠溶液与二氧化碳反应的曲线是_____(填①或②)。
甲 乙
|
|||||||
| 38. | 详细信息 | ||||||||||||||||||||||||||||||||||||||
|
某实验小组同学在向饱和碳酸钠溶液中逐滴加入稀盐酸时,开始时未观察到气泡。 【提出问题】开始时为什么没有出现气泡? 【查阅资料】碳酸钠溶液与稀盐酸的反应分两步进行:其中第一步反应的化学方程式为Na2CO3 + HCl ══ NaCl + NaHCO3,第二步为碳酸氢钠与盐酸反应。
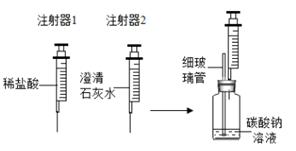
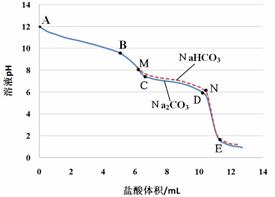
(1)澄清石灰水变浑浊的化学方程式为 。 (2)实验2中①的现象是 。 (3)实验2中②的操作是 。 (4)细玻璃管在实验中的主要作用是 。 【进行实验二】在老师的帮助下,同学们利用pH传感器对相同浓度的碳酸钠溶液(pH为12)、碳酸氢钠溶液(pH为8.2)与盐酸反应时,pH的变化与盐酸体积的关系进行了测定,并做了如下所示的对比图:
图中各线段实验现象如下表:
(5)在AB段,溶液中的溶质有 。 (6)分析图表,充分体现碳酸钠与稀盐酸第二步反应的是 段。 【反思与评价】 (7)若将碳酸钠溶液逐滴滴加到盐酸中,出现的现象是 。
|
|||||||||||||||||||||||||||||||||||||||
| 39. | 详细信息 |
|
自然界中的碳循环(部分)如右图所示。下列
A.碳循环中的“碳”指碳单质 B.碳循环对于保持自然界平衡具有重要作用 C.能吸收碳的自然资源主要有海洋、森林、土壤等 D.化石燃料的大量使用会使大气中二氧化碳的含量不断增加
|
|
| 40. | 详细信息 |
|
某烟气脱硫的工艺不仅能消除SO2,还能将其转化为石膏(CaSO4·2H2O)等产品,实现“变废为宝”。主要物质转化关系如下:
(1)设备1中加入原料水的目的是 。 (2)设备2中发生了复分解反应,反应的化学方程式为 。 (3)CaSO4中的氧元素来自原料 和水。
|
|
| 41. | 详细信息 |
|
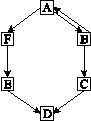
(1)A可供给呼吸,其化学式为_______。 (2)C俗称熟石灰,B转化成C的化学方程式为 。 (3)D的化学式为 。 (4)F转化为E的化学方程式为_______。
|
|
- 2017-2018年九年级上册化学期中考试考试(吉林省农安县第四中学)
- 2017届九年级化学专题复习:化学常用仪器和实验基本操作专题检测(山东省平邑县蒙阳新星学校)
- 2018届九年级人教版下册化学课堂训练:第八单元 课题1《金属材料》(河南省永城市龙岗中学)
- 2018届九年级上半期第三次月考化学试卷(新疆乌鲁木齐市第九十八中学)
- 2016-2017年九年级化学一模考试在线测验(辽宁省丹东市第七中学)
- 2018届九年级下册化学同步练习:第九单元 溶液(人教版)
- 广东2019年九年级化学上期月考测验试卷带解析及答案
- 2016-2017年九年级化学二模考试带参考答案和解析(期中)(湖北省孝感市孝南区)