2019江西高三上学期人教版(2019)高中化学月考试卷
| 1. | 详细信息 |
|
“中国名片”中航天、军事、天文等领城的发展受到世界瞩目,它们与化学有着密切联系。下列说法错误的是 A. “中国天眼”的“眼眶”是钢铁结成的圈梁,其属于黑色金属材料 B. “歼”飞机上大量使用的碳纤维是一种新型有机高分子材料 C. “神舟十一号”宇宙飞船返回舱外表面使用的高温结构陶瓷是新型无机非金属材料 D. “天宫二号”空间实验室的硅电池板将光能直接转换为电能
|
|
| 2. | 详细信息 |
|
设NA为阿伏加德罗常数的数值。下列叙述正确的是 A. 46g有机物C2H6O中含有极性共价键的数目一定为7NA B. 密闭容器中1molH2与1molI2制备HI,增加2NA个H-I键 C. 25℃,1LpH=13的Ba(OH)2溶液中OH-数为0.2NA D. 0.1molFe 在足量氧气中燃烧,转移电子数为4/15NA
|
|
| 3. | 详细信息 |
|
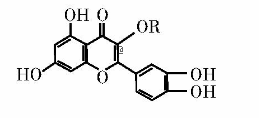
维生素P的结构如图所示,其中R为烷烃基,维生素P是一种营养增补剂。下列关于维生素P的叙述正确的是
A. 分子中的官能团有羟基、碳碳双键、醚键、酯基 B. 若R为甲基,则该物质的分子式可以表示为C16H14O7 C. 该化合物遇三氯化铁溶液发生显色反应 D. 1 mol该化合物与氢气加成所需氢气的物质的量最多是7 mol
|
|
| 4. | 详细信息 |
|
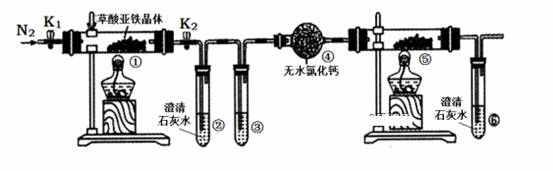
某同学用下图所示装置检验草酸亚铁晶体(FeC2O4·2H2O,淡黄色)受热分解的部分产物。下列说法正确的是( )
A. 通入N2的主要目的是防止空气中的水蒸气对产物检验产生影响 B. 若③和⑤中分别盛放足量NaOH溶液、CuO固体,可检验生成的CO C. 实验结束后,①中淡黄色粉末完全变成黑色,则产物一定为铁 D. 若将④中的无水CaC12换成无水硫酸铜可检验分解生成的水蒸气
|
|
| 5. | 详细信息 |
|
下列离子方程式书写正确的是( ) A.用漂白液将污水中的NH3氧化成N2:ClO-+2NH3===N2+Cl-+3H2O B.向NH4HCO3稀溶液中滴加过量Ca(OH)2溶液: NH C.酸性条件下,用H2O2将I-转化为I2:H2O2+2I-===I2+2OH- D.用少量的氨水吸收硫酸工业尾气中的SO2:SO2+NH3·H2O===NH
|
|
| 6. | 详细信息 |
|
短周期主族元素W、X、Y、Z的原子序数依次增大,它们的最外层电子数之和为22。W、Y同主族,X所处的周期数等于族序数,常温下Y的最高价氧化物对应的水化物可贮存在由X的单质制成的容器中。下列说法正确的是 A. 简单离子半径:X>Y>Z B.工业上可电解X与Z形成的化合物来制取X单质 C.Y的氢化物沸点比W的氢化物沸点高 D. W、Y两种元素形成的一种化合物能使酸性KMnO4溶液褪色
|
|
| 7. | 详细信息 |
|
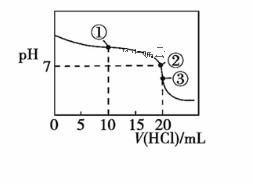
常温下,用0.100 0 mol·L-1的盐酸滴定20.00 mL未知浓度的氨水,滴定曲线如图所示,滴加20.00 mL盐酸时所得溶液中c(Cl-)=c(NH4+)+c(NH3·H2O)+c(NH3)。下列说法错误的是
A. 该氨水的浓度为0.1000 mol·L-1 B. 点①溶液中c(NH4+)+c(NH3·H2O)+c(NH3)=2c(Cl-) C. 点②溶液中c(NH4+)=c(Cl-) D. 点③溶液中c(Cl-)>c(H+)>c(NH4+)>c(OH-)
|
|
| 8. | 详细信息 |
|
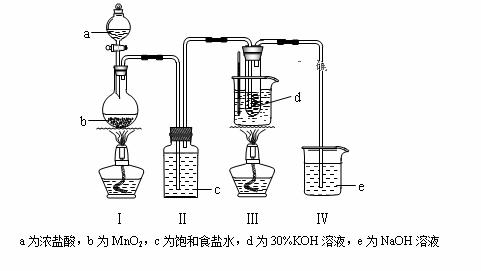
氯气与碱溶液反应,在低温和稀碱溶液中主要产物是ClO—和Cl—,在75℃以上和浓碱溶液中主要产物是ClO3—和Cl—。研究小组用如下实验装置制取氯酸钾(KClO3),并测定其纯度。回答下列问题:
(1)检查装置气密性后,添加药品,待装置Ⅲ水温升至75℃开始反应。 ①写出装置Ⅰ中反应的化学方程式为_____ ___。 ②若取消装置Ⅱ,对本实验的影响是______ __。 ③实验结束,拆解装置Ⅰ前为了防止大量氯气逸出,可采取的措施是_______。 (2)已知碱性条件下,ClO—有强氧化性,而ClO3—氧化性很弱。设计实验证明:碱性条件下,H2O2能被ClO—氧化,而不能被ClO3—氧化。____ ____。 (3)为测定产品KClO3的纯度,进行如下实验: 步骤1:取2.45g样品溶于水配成250mL溶液。 步骤2:取25.00mL溶液于锥形瓶中,调至pH=10,滴加足量H2O2溶液充分振荡,然后煮沸溶液1~2分钟,冷却。 步骤3:加入过量KI溶液,再逐滴加入足量稀硫酸。(ClO3—+6I—+6H+=Cl—+3I2+3H2O) 步骤4:加入指示剂,用0.5000 mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00mL。(2S2O32—+I2=S4O62—+2I—) ①步骤2的目的是________。写出煮沸时反应的化学方程式________。 ②样品中KClO3的质量分数为________。(KClO3相对分子质量:122.5)
|
|
| 9. | 详细信息 |
|
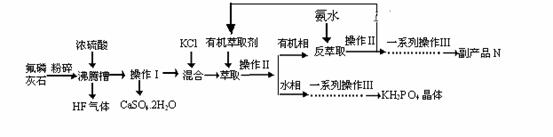
据报道,磷酸二氢钾(KH2PO4)大晶体已应用于我国研制的巨型激光器“神光二号”中。利用氟磷灰石(化学式为Ca5P3FO12)制备磷酸二氢钾的工艺流程如下图所示(部分流程步骤已省略):
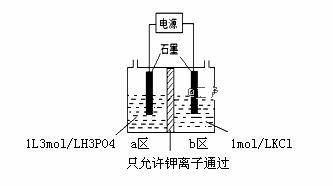
已知萃取的主要反应原理:KCl+H3PO4 (1)流程中将氟磷灰石粉碎的目的是__________________________________。 (2)不能使用二氧化硅陶瓷材质的沸腾槽的主要原因是____________(用化学方程式表示)。 (3)副产品N的化学式是____________;在得到KH2PO4晶体的一系列操作Ⅲ,其主要包括______________________________、过滤、洗涤、干燥等。 (4)若用1000kg质量分数为50.4%的氟磷灰石(化学式为Ca5P3FO12,摩尔质量为504g/mol)来制取磷酸二氢钾晶体,其产率为80%,则理论上可生产KH2PO4(摩尔质量为136g/mol)的质量为_______kg。 (5)电解法制备KH2PO4的装置如图所示.该电解装置中,a 区属于_______区(填“阳极”或“阴极”),阴极区的电极反应式是________________。
(6)工业上还可以用氟磷灰石与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,同时逸出SiF4和CO,该反应的化学方程式为________________________________________。
|
|
| 10. | 详细信息 | |||||||||||||||||||||||||
|
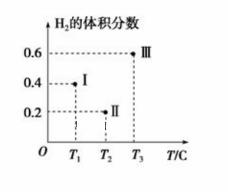
(1)2017年中科院某研究团队通过设计一种新型Na-Fe3O4/HZSM-5多功能复合催化剂,成功实现了CO2直接加氢制取辛烷值汽油,该研究成果被评价为“CO2催化转化领域的突破性进展”。 已知:H2(g)+1/2O2(g)=H2O(l) ΔH1 = -aKJ/mol C8H18(1)+25/2O2(g)=8CO2(g)+9H2O(1) ΔH2= -bKJ/mol 试写出25℃、101kPa条件下,CO2与H2反应生成汽油(以C8H18表示)的热化学方程式 _ _。 (2)利用CO2及H2为原料,在合适的催化剂(如Cu/ZnO催化剂)作用下,也可合成CH3OH,涉及的反应有: 甲:CO2(g)+3H2(g) 乙:CO2(g)+H2(g) ①CO(g)+2H2(g) ②提高CO2转化为CH3OH平衡转化率的措施有___________(填写两项)。 ③催化剂和反应体系的关系就像锁和钥匙的关系一样,具有高度的选择性。下列四组实验,控制CO2和H2初始投料比均为1:2.2,经过相同反应时间(t1min)。
由表格中的数据可知,相同温度下不同的催化剂对CO2的转化为CH3OH的选择性有显著影响,根据上表所给数据结合反应原理,所得最优选项为___________(填字母符号)。 (3)以CO、H2为原料合成甲醇的反应为:CO(g)+2H2(g)
①0~5min时间内容器Ⅱ中用CH3OH表示的化学反应速率为_________________。 ②三个容器中一定达到平衡状态的是容器________(填写容器代号)。
|
||||||||||||||||||||||||||
| 11. | 详细信息 |
|
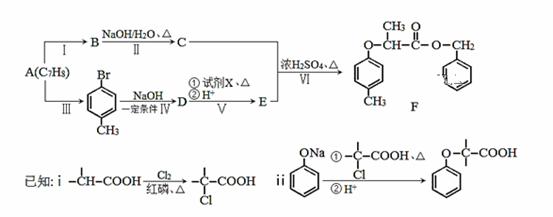
[化学—选修5:有机化学基础](除标注外,其余每空2分,共14分) 有机物F是一种香料,其合成路线如图所示:
(1)D的名称为________________,试剂X的结构简式为____________,步骤Ⅵ的反应类型为___________。 (2)步骤Ⅰ的反应试剂和条件为____________________________。 (3)步骤Ⅱ反应的化学方程式为__________________________________。 (4)满足括号中条件(①苯环上只有两个取代基,②能与FeCl3溶液发生显色反应,③能发生水解反应和银镜反应)的E的同分异构体有____________种,其中核磁共振氢谱峰面积比为6︰2︰2︰1︰1的分子的结构简式为___________________________。 (5)依据题中信息,完成以 合成路线图示例如下:
|
|