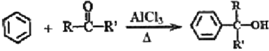2019北京高二上学期人教版(2019)高中化学期中考试
| 1. | 详细信息 |
|
下列各组物种中,属于同系物的是( ) A. CH4、CH2=CH2 B. CH3CH3、CH3CH2CH3 C. CH3CH2OH、CH3CH2OCH3 D. CH3Cl、CHCl3
|
|
| 2. | 详细信息 |
|
下列有机化合物的名称中,正确的是( ) A. 2-乙基丁烷 B. 2,4,5-三氯己烷 C. 2,5-二甲基已烷 D. 2-乙基-2-丁烯
|
|
| 3. | 详细信息 |
|
戊烷(C5H12)的同分异构体共有( )个 A. 2个 B. 3个 C. 4个 D. 5个
|
|
| 4. | 详细信息 |
|
下列化学式只能表示一种物质的是( ) A. C3H8 B. C2H6O C. C4H10 D. C2H4Br2
|
|
| 5. | 详细信息 |
|
下列物质中,包含顺反异构体的是( ) A. C.
|
|
| 6. | 详细信息 |
|
有机物(CH3)2CClCH3与CH3CH2CH2CH2Cl的关系为( ) A. 官能团异构体 B. 碳链异构体 C. (官能团)位置异构体 D. 顺反异构体
|
|
| 7. | 详细信息 |
|
下列物质中,一氯代物的种类最多的是( ) A 正戊烷 B. 异戊烷 C. 邻二甲苯 D. 对二甲苯
|
|
| 8. | 详细信息 |
|
下列四种物质摩尔质量彼此接近。根据它们的结构判断,四种物质中,沸点最高、在水中溶解度最大的是( ) A. 氯乙烷 B. 1-戊烯 C. 正戊烷 D. 1-丁醇
|
|
| 9. | 详细信息 |
|
下列各组物质汇总,最适宜使用红外光谱法进行区分的是( ) A. 2-甲基戊烷、3-甲基戊烷 B. 1-丙醇、1-丁醇 C. 苯、甲苯 D. 1-丁醇、1-溴丁烷
|
|
| 10. | 详细信息 |
|
用乙炔为原料制取CH2Br—CHBrCl,可行的反应途径是( ) A. 先与HCl加成,再与HBr加成 B. 先与H2加成,再与Br2加成 C. 先与Br2加成,再与HCl加成 D. 先与HBr加成,再与Cl2加成
|
|
| 11. | 详细信息 |
|
某醇在发生消去反应时可以得到且仅得到一种单烯烃,则该醇的结构简式可能为( ) A. (CH3)3CC(CH3)2OH B. CH3CH2CH2C(CH3)2CH2OH C. (CH3)2CHC(CH3)2CH2OH D. (CH3)2CHCH(OH)CH2CH2CH3
|
|
| 12. | 详细信息 |
|
下列分子中的碳原子一定不处在同一平面的是( ) A. CH3CH2CH2CH3 B. C.
|
|
| 13. | 详细信息 |
|
下列各反应中,反应类型与其他反应不同的是( ) A 甲烷与氯气混合后光照 B. 以苯为原料制备溴苯 C. 由1,2-二溴乙烷制备1,2-乙二醇 D. 一定条件下甲苯转化为苯甲酸
|
|
| 14. | 详细信息 |
|
2-丁醇发生下列反应时,C-O键会发生断裂的是( ) A. 与金属Na反应 B. 在Cu催化下与O2反应 C. 与HBr在加热条件下反应 D. 与乙酸在适当条件下发生酯化反应
|
|
| 15. | 详细信息 | |||||||||||||||
|
根据以下信息判断,分离乙醇、乙二醇混合物的最佳方法是( )
A. 分液 B. 用水萃取 C. 蒸馏 D. 重结晶
|
||||||||||||||||
| 16. | 详细信息 |
|
下列实验中,不需要使用温度计的是( ) A. 以乙醇为原料制备乙烯 B. 从医用酒精中提取乙醇 C. 以苯为原料制备硝基苯 D. 以苯为原料制备溴苯
|
|
| 17. | 详细信息 |
|
下列各组试剂中,仅使用高锰酸钾酸性溶液就可鉴别的一组是( ) A. 己烷、1-己烯、1-己炔 B. 乙醇、苯、四氯化碳 C. 聚乙烯、聚氯乙烯、聚四氟乙烯 D. 己烷、苯、甲苯
|
|
| 18. | 详细信息 | ||||||||||||||||||||
|
为除去混在目标产物中的杂质,所选试剂及分离方法均正确的是( )
A. A B. B C. C D. D
|
|||||||||||||||||||||
| 19. | 详细信息 |
|
有机物中,两个原子团之间的相互影响会使各原子团本身的化学性质发生改变。化学性质指能否发生某种化学反应,以及发生某种化学反应的难易程度。下列各项事实中不能说明上述观点的是( ) A. 甲烷不能使酸性高锰酸钾溶液褪色,而甲苯能使酸性高锰酸钾溶液褪色 B. 苯与浓硝酸的反应50℃以上才能发生,而甲苯与浓硝酸的反应30℃即可发生 C. 苯在50℃时可以与浓硝酸反应得到一硝基苯,而硝基苯在50℃时不能与浓硝酸反应得到二硝基苯 D. 1-戊醇可以与金属钠反应得到氢气,而戊烷不能与金属钠反应
|
|
| 20. | 详细信息 |
|
一定条件下,萘可以与浓硝酸反应,生成两种二硝酸萘;1,5-二硝基萘、1,8-二硝基萘。两种产物室温下均为固态,均不溶于水、稀酸。1,8-二硝基萘可溶于98%的硫酸,而1,5-二硝基萘不能,利用这一性质可以将两种产物分离。向反应产物中加入适量98%的硫酸,充分搅拌;用耐酸漏斗过滤。欲得到纯净的1,8-二硝基萘,最有效、经济且环保的方法是( ) A. 用水淋洗滤渣数次,干燥 B. 取滤液蒸发结晶 C. 将滤液缓缓倒入水中,过滤,干燥 D. 取滤液加入适量NaOH,过滤,干燥
|
|
| 21. | 详细信息 |
|
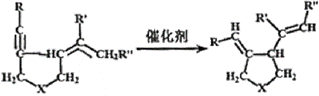
我国著名有机化学家张绪穆于2000年在JACS杂志上公布了著名的“张烯炔异构化反应”及其机理。该反应丰富了人类进行天然有机分子全合成的手段,该反应原理如下: 其中:—R、—R’、—R’’可以为—H、—CH3、—CH2CH3或 现拟合成 A. CH3—C B. CH3—C C. CH3—C D. CH3—C
|
|
| 22. | 详细信息 |
|
某有机物结构简式为 A. 加成反应 B. 消去反应 C. 取代反应 D. 氧化反应
|
|
| 23. | 详细信息 |
|
某芳香烃的分子式为C9H12,其可能的结构有( ) A. 6种 B. 7种 C. 8种 D. 9种
|
|
| 24. | 详细信息 |
|
将溴乙烷与过量的NaOH的某种溶液共热。下列实验方案中,可用于判断共热时所发生反应的反应类型的是( ) A. 取少量溶液于试管中,加入高锰酸钾酸性溶液,观察是否褪色 B. 取少量溶液于试管中,加入溴水,观察是否褪色 C. 取少量溶液于试管中,加入足量硝酸,再加入硝酸银溶液,观察有无沉淀 D. 取少量溶液于试管中,加入足量盐酸,再加入溴水,观察是否褪色
|
|
| 25. | 详细信息 |
|
若有机分子中的两个碳碳双键仅间隔一个碳碳单键,将这两个碳碳双键称为共轭双键。将含有共轭双键的二烯烃称为共轭二烯烃。最简单的共轭二烯烃为1,3-丁二烯。天然橡胶的单体2-甲基-1,3-丁二烯也是共轭二烯烃。现有一种共轭二烯烃A。A与足量H2充分反应后得到烃B。B的结构简式如图所示。不考虑顺反异构体的情况下,A的可能结构有( )
A. 1种 B. 2种 C. 3种 D. 4种
|
|
| 26. | 详细信息 |
|
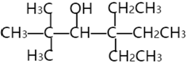
请按要求回答下列问题。 I.请写出下列物质所含官能团的名称: (1)CH3CH2CH2OH;___(2)CH2=CHCH2CH3;___ II.请写出下列物质所含官能团的结构简式: (3)CH3CH2COOH;___(4)CH3CH2CH2Br;___ III.请按照系统命名法为下列物质命名: (5) (6) IV.请按照要求画出相应的同分异构体: (7)分子式为C5H10O的醛共有___种;在这些醛中,醛A的核磁共振氢谱中的信号数量最少(即峰数最少),A的结构简式是___。 (8)不考虑顺反异构的情况下,链状卤代烃C4H7Cl的同分异构体共有___种;若考虑顺反异构,链状卤代烃C4H7Cl的同分异构体共有___种。
|
|
| 27. | 详细信息 |
|
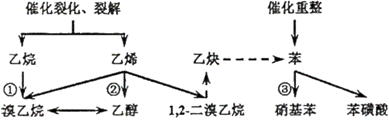
现代化学工业中,有机原料的主要来源为石油的裂化、裂解、重整产物、部分已经学习过的反应如下。
(1)请写出反应①由乙烷制备溴乙烷的化学反应方程式___; (2)请写出反应②由乙烯制备乙醇的化学反应方程式___; (3)请写出反应③由苯制备硝基苯的化学反应方程式___。
|
|
| 28. | 详细信息 |
|
如图为实验室制备乙炔并进行性质验证的装置(夹持仪器己略去)。
(1)实验室制备乙炔的方程式为___; (2)仪器A的名称为___,为防止气体生成的速率过快,由A滴入B的试剂为___; (3)装置C可选用的试剂为___(写出一种即可),其作用为___; (4)反应开始后,D中的现象为___,所发生反应的反应类型为___; (5)D中验证实验结束后。B中反应仍在继续。此时可撤去装置D,在装置C之后连接收集装置,以下装置中最适合用于收集乙炔的是___。
|
|
| 29. | 详细信息 |
|
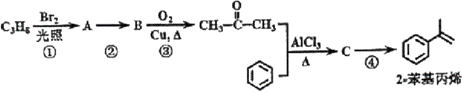
2-苯基丙烯是日化行业常用的化工原料,其合成路线如下(反应②、④的条件未写出)。
已知: 其中,R、R’为H原子或烷基。 (1)C3H8的结构简式为___; (2)反应①的反应类型为___; (3)反应②的化学反应方程式为___; (4)反应③的反应类型为___; (5)反应④的化学反应方程式为___; (6)产物2-苯基丙烯在一定条件下可以发生加聚反应,加聚产物的结构简式为___; (7)请以苯、乙醇及其他必要的无机试剂为原料,合成
|
|
| 30. | 详细信息 | ||||||||
|
某课题组从植物香料中分离出一种罕见的醇(醇A),其结构简式如下。
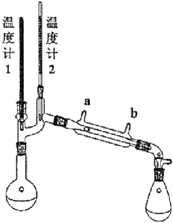
(1)根据课内所学知识,该醇可发生的反应包括:___(填字母序号) A.与金属Na反应 B.与CuO反应 C.与浓盐酸反应 D.消去反应 I.该课题组设计了以醇A为原料制备某物质的合成路线。合成反应的第一步。拟使醇A与浓氢溴酸(质量分数47.6%)在90℃下充分反应,制备中间产物B。实验装置如图所示(夹持及加热仪器略去)。
已知:①HBr溶液受热时,HBr能否蒸发受到体系汇总含水量的影响。具体情况如下表。
②醇A、中间产物B的沸点均超过200℃。 (2)温度计1拟用于监控反应温度,温度计2拟用于监控实验中离开烧瓶的物质的沸点。两个温度计中,水银球位置错误的是___(填“温度计1”或“温度计2”)其水银球应___; (3)实验时,冷凝水应从冷凝管的___(填“a口”或“b口”)流入。 II.将温度计位置调节好后,课题组成员依次进行如下操作: ①检验气密性,装入沸石; ②加入18.6g醇A(0.1mol)、17.0g47.6%氢溴酸(含8.1gHBr、0.1mol); ③开始加热,逐渐升温至反应温度。 (4)反应开始后,当温度计2的示数上升至39℃时,冷凝管末端持续有液体流出。反应结束时,共收集到无色液体7.0g。经检测,该液体为纯净物,标记为产物C。取0.7gC在氧气中充分燃烧,共收集到2.2gCO2、0.9gH2O。另取少量C进行质谱试验,结果如图所示。
根据上述实验结果,C的分子式为___; (5)取少量产物C进行核磁共振氢谱试验,共有三个信号峰。三个信号峰的面积之比为3:6:1。综合上述实验结果,C的结构简式为___; (6)反应结束后,圆底烧瓶内液体分为两层。可用___方法(填实验操作名称)将两液体分离; (7)后续检验证实,两液体均较纯净,其中所含杂质均可忽略。上层液体质量为10.7g。取下层液体进行核磁共振氢谱实验,共有两个信号峰。峰的面积之比为3:2。综合以上信息,本实验的实际总反应方程式为___。
|
|||||||||
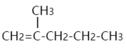 B.
B.