2020湖北高一上学期人教版(2019)高中化学期中考试
| 1. | 详细信息 |
|
|
|
| 2. | 详细信息 |
|
下列关于阿伏加德罗常数的说法正确的是 ( ) A.阿伏加德罗常数是12g碳中所含的碳原子数 B.阿伏加德罗常数是 0.012kg12C中所含的原子数 C.阿伏加德罗常数是6.02×1023 mol-1 D.阿伏加德罗常数的符号为NA,近似值为6.02×1023
|
|
| 3. | 详细信息 |
|
下列有关说法正确的是 ( ) A.蛋白质溶液属于胶体,能透过滤纸. B.在水溶液中或熔融状态下能导电的物质是电解质 C.能电离出氢离子的化合物是酸 D.胶体带电荷,所以会产生电泳现象
|
|
| 4. | 详细信息 |
|
下列类型的化学反应一定是氧化还原反应的是 ( ) A.化合反应 B.分解反应 C.复分解反应 D.置换反应
|
|
| 5. | 详细信息 |
|
下列物质属于非电解质的是 ( ) ①NaOH ②CaCO3 ③Cu ④C2H5OH ⑤SO2 ⑥H2S ⑦氨水 A.④⑤ B.④⑤⑦ C.③④⑤⑦ D.④⑤⑥⑦
|
|
| 6. | 详细信息 |
|
下列各组离子在强酸性溶液中能大量共存的是 ( ) A.Na+、Cl—、K+、HCO3— B. Cl—、NO3—、K+、Ag+ C.Ba2+、Mg2+、Cl-、SO42- D.Al3+、Na+、SO42-、Cl-
|
|
| 7. | 详细信息 |
|
在一定温度和压强下,1体积的A2气体和3体积的B2气体化合成2体积的C气体,则C的化学式为 ( ) A.AB3 B.AB C.A3B D.A2B
|
|
| 8. | 详细信息 |
|
鉴别胶体和溶液的方法是 ( ) A.渗析 B.电泳 C.丁达尔效应 D.布朗运动
|
|
| 9. | 详细信息 |
|
下列说法正确的是 ( ) A.NaOH的摩尔质量为40g。 B.22.4 L气体所含分子数一定大于11.2 L气体所含的分子数。 C.标准状况下,1 mol任何物质的体积都约为22.4 L。 D.标准状况下,1 mol 由O2和N2按任意比组成的混合气体的体积约为22.4 L。
|
|
| 10. | 详细信息 |
|
必须加入还原剂才能实现的反应是 ( ) A.KCIO3 →O2 B.Fe2+→ Fe3+ C.SO2 →S D.CO32— →CO2
|
|
| 11. | 详细信息 |
|
下列液体不能用于从碘水中萃取碘的是 ( ) A.酒精 B. 汽油 C.四氯化碳 D.苯
|
|
| 12. | 详细信息 |
|
氧化还原反应的实质是 ( ) A.氧元素的得与失 B.电子的得失或共用电子对的偏移 C.化合价的升降 D.分子中的原子重新组合
|
|
| 13. | 详细信息 |
|
下列反应的离子方程式书写正确的是 ( ) A.氢氧化钡溶液与硫酸的反应: OH-+H+ = H2O B.铜片插入硝酸银溶液中: Cu + Ag+ = Cu2+ + Ag C.碳酸钙溶于稀盐酸中: CaCO3+2H+ = Ca2++H2O+CO2 D.铁与稀硫酸反应:2Fe +6H+ == 2Fe2+ + 3H2↑
|
|
| 14. | 详细信息 |
|
“纳米材料”是粒子直径为l~100 nm(纳米)的材料,纳米碳就是其中的一种。 若将纳米碳均匀地分散到蒸馏水中,所形成的物质 ( ) ①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过滤纸 ⑥静置后,会析出黑色沉淀 A.①④⑥ B.②③④ C.②③⑤ D.①③④⑥
|
|
| 15. | 详细信息 | ||||||||||||||||||||||||||||||
|
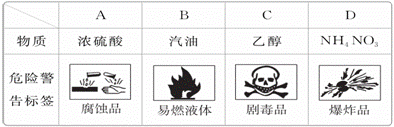
下列物质分类的正确组合是 ( )
|
|||||||||||||||||||||||||||||||
| 16. | 详细信息 |
|
为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列5项操作:①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液。正确的操作顺序可以是 ( ) A.②⑤④①③ B.④①②⑤③ C.⑤②④③① D.①④②⑤③
|
|
| 17. | 详细信息 |
|
将1L0.2mol/L硫酸铝溶液和1L0.2mL/L硫酸钠溶液混合,若混合后溶液的体积等于混合前两溶液的体积之和,则混合后溶液中硫酸根离子浓度为 ( ) A.0.2mol/L B.0.4mol/L C.0.8mol/L D.0.1mol/L
|
|
| 18. | 详细信息 |
|
已知NaCl、MgCl2、AlCl3三种溶液的物质的量浓度之比为1:2: 1,取等体积三种溶液分别与某浓度的AgNO3溶液恰好完全反应,则NaCl、MgCl2、AlCl3三种溶液消耗的AgNO3溶液的体积之比为 ( ) A.12:3:4 B.6:3:4 C.3:4:1 D.1:4:3
|
|
| 19. | 详细信息 |
|
通过电火花使密闭容器中装有的H2、O2、Cl2混合气体恰好完全反应,将容器的温度冷却到室温时可以得到HCl溶液,原容器中H2、O2、Cl2三种气体的体积比可能为 ( ) A、2:1:1 B、7:3:1 C、9:4:3 D、4:2:2
|
|
| 20. | 详细信息 |
|
20℃时,NaCl的溶解度是35.1g,此时NaCl饱和溶液的密度为1.12g/cm3,在此温度下NaCl饱和溶液中NaCl的物质的量浓度为 ( ) A.0.15mol/L B.1.35mol/L C.4.97mol/L D.6.0mol/L
|
|
| 21. | 详细信息 |
|
(1)选择下列实验方法分离物质,将分离方法的序号填在横线上: a、萃取分液法; b、加热分解; c、结晶法; d、分液法; e、蒸馏法; f、过滤法; g、渗析法 ①_____从硝酸钾和氯化钠的混合溶液中获得硝酸钾 ②______分离水和苯的混合物 ③_____除去氢氧化铁胶体中混有的NaCl ④______分离碘和四氯化碳 (2)实验室用4.0 mol/L NaCl溶液配制100mL 0.50 mol/L NaCl溶液。 ①实验需要玻璃棒、胶头滴管、烧杯、量筒外,还需要的玻璃仪器是 。 ②配制上述溶液,需要4.0 mol/L NaCl溶液 mL。 ③配制过程中出现以下情况,使所配溶液浓度偏低 。 A.溶液转移后没有洗涤烧杯和玻璃棒。 B.定容时仰视容量瓶的刻度线。 C. 未冷却即进行转移、定容操作。 D.容量瓶中原有少量蒸馏水 E.如果加水超过了刻度线,取出溶液使液面恰好到刻度线。
|
|
| 22. | 详细信息 |
|
有A、B、C、D 四种化合物,分别由K+ 、Ba2+ 、SO42- 、CO32- 、OH-中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无刺激性气味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。 (1)推断A、B、C、D的化学式: A ;B ;C ;D 。 (2)写出下列反应的离子方程式: C与盐酸反应 B与盐酸反应 过量的E与澄清石灰水反应
|
|
| 23. | 详细信息 |
|
(1)在标准状况下,有物质①44.8LH2,②24gCH4,③1molH2O,④3.01×1023个N2,含分子数最多的是______(填序号,下同),含电子数最多的是________,质量最大的是______,体积最小的是______;密度由小到大的顺序为________________。 (2)0.5mol某固体A的质量是40g,A的摩尔质量为_________。 (3)质量之比为8∶7的两种气体O2、CO,其分子数之比为_______________;氧原子数之比为____________;相同条件下的体积之比为________。 (4) 4.8g碳在一定量的氧气中燃烧,反应后生成CO和CO2的总质量为12.8g。则在同温同压下,生成的CO和CO2的体积比为__________。 (5)由NaHS,MgSO4,NaHSO3组成的混合物中,硫元素的质量分数为a%,则混合物中氧元素的质量分数为_______________。
|
|