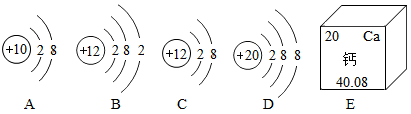2021年辽宁省营口市化学中考试题含详解
| 1. | 详细信息 |
|
下列变化属于化学变化的是 A . 合成新药 B . 铁水铸锅 C . 酒精挥发 D . 矿石粉碎 |
|
| 2. | 详细信息 |
|
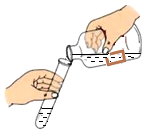
下列图示的 “ 错误操作 ” 与选项中 “ 可能引起的后果 ” 不匹配的是 A . C . |
|
| 3. | 详细信息 |
|
要提高全民的环境意识,保护我们的空气。下列不属于空气污染物的是 A . CO B . O 3 C . CO 2 D . PM 2.5 |
|
| 4. | 详细信息 |
|
下列物质中氯元素的化合价最低的是 A . NaClO 3 B . Cl 2 C . NaCl D . HClO |
|
| 5. | 详细信息 |
|
合成材料的应用,大大方便了人类的生活。下列生活用品由合成材料制成的是 A . 纯棉毛巾 B . 不锈钢餐具 C . 真丝睡衣 D . 塑料水管 |
|
| 6. | 详细信息 |
|
下列灭火方法,主要是利用隔绝氧气原理的是 A . 吹灭蜡烛 B . 用灯帽盖灭酒精灯 C . 关闭炉具阀门 D . 用高压水枪灭火 |
|
| 7. | 详细信息 |
|
下列物质能溶于水形成溶液的是 A . 蔗糖 B . 面粉 C . 植物油 D . 泥沙 |
|
| 8. | 详细信息 |
|
化肥对提高农作物产量具有重要作用。下列属于复合肥料的是 A . K 2 SO 4 B . CO ( NH 2 ) 2 C . ( NH 4 ) 2 HPO 4 D . Ca 3 ( PO 4 ) 2 |
|
| 9. | 详细信息 | ||||||||||
|
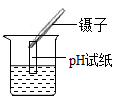
某同学用 pH 试纸测定了生活中一些物质的 pH 如下,其中能使酚酞试液变红的是
A . 食盐水 B . 炉具清洁剂 C . 苹果汁 D . 酱油 |
|||||||||||
| 10. | 详细信息 |
|
防控新冠肺炎期间,很多医院使用来苏水进行杀菌消毒,来苏水的主要成分之一是对甲基苯酚(化学式为: C 7 H 8 O )下列有关对甲基苯酚的叙述正确的是 A . 对甲基苯酚的相对分子质量为 108g B . 对甲基苯酚中碳元素的质量分数最大 C . 对甲基苯酚由 16 个原子构成 D . 对甲基苯酚中碳、氢、氧元素的质量比为 7:8:1 |
|
| 11. | 详细信息 |
|
下列金属不能与 A . |
|
| 12. | 详细信息 |
|
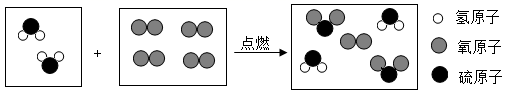
某反应的微观示意图如下,有关说法正确的是 A . 参加反应的两种物质的质量比为 17:24 B . 反应前后各元素的化合价不变 C . 化学方程式为: |
|
| 13. | 详细信息 |
|
下列关于二氧化碳与一氧化碳用途的说法,错误的是 A . CO 2 可用于灭火 B . CO 2 可用作气体肥料 C . CO 可用于人工降雨 D . CO 可用作燃料 |
|
| 14. | 详细信息 | |||||||||||||||
|
除去下列物质中混有的少量杂质(括号内为杂质),所选试剂和操作方法均正确的是
A . A B . B C . C D . D |
||||||||||||||||
| 15. | 详细信息 |
|
只用水这一种试剂不能将下列各组固体物质鉴别出来的是 A . KNO 3 和 NH 4 NO 3 B . CaCO 3 和 Ca ( NO 3 ) 2 C . NaOH 和 NaCl D . K 2 SO 4 和 NaNO 3 |
|
| 16. | 详细信息 |
|
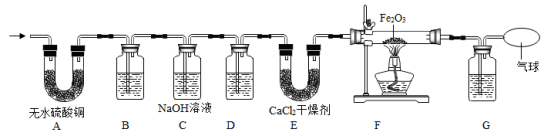
在学习了单质碳的化学性质后,某化学兴趣小组的同学对含碳化合物燃烧后的产物进行了探究。 (提出问题)乙醇燃烧后的产物是什么? (查阅资料) ①无水硫酸铜为白色粉末,遇水会变蓝;②氯化钙有吸水性,可做干燥剂。 (做出猜想) 猜想一:产物中含有 CO 、 H 2 O ; 猜想二:产物中含有 CO 2 、 H 2 O ; 猜想三:产物中含有 _______ 。 (进行实验)同学们设计了如下图的实验:检查装置气密性后,将乙醇燃烧的产物依次通过如图所示的装置进行验证;(部分夹持、固定装置省略; B 、 D 、 G 装置中均为澄清的石灰水)。 ( 1 )装置 B 的作用是 _______ 。 ( 2 ) F 装置中若发生反应,则化学方程式是 ______ 。 (解释与结论)经过实验,同学们认为猜想三成立。 ( 3 )实验中能观察到的现象是 _______ ;装置 C 中发生反应的化学方程式为 _______ 。 (反思与评价)实验结束后,由于小丽同学的操作不当造成了仪器损坏,小组内同学针对这个事故,进行了分析和讨论。 ( 4 )为了避免此事故再次发生,同学们对该装置进行了创新和改进,你认为他们的改进是 ________ (文字说明或画图都可)。 |
|
| 17. | 详细信息 |
|
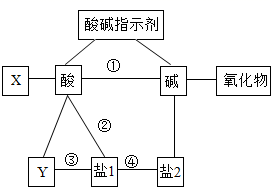
下图为初中化学中关于酸、碱、盐化学性质的知识框架图, X 、 Y 是除酸、碱、盐之外的不同类别的物质,据图回答问题: ( 1 ) X 的物质类别是 ________ 。 ( 2 )若 “盐 1 ”为 ( 3 )反应 ④能够发生应该满足的条件是 _______ 。 ( 4 )在反应 ①②③④中,属于中和反应的是 _______ 。 |
|
| 18. | 详细信息 |
|
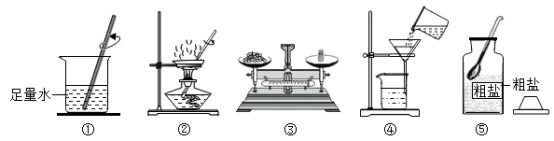
下面为 “去除粗盐中难溶性杂质并计算产率”的实验操作示意图: ( 1 )请将上述操作进行合理排序: ________ (填序号)、计算;请改正操作 ④中的错误 _______ 。 ( 2 )操作 ②中,用玻璃棒不断搅拌的目的是 ________ 。 ( 3 )过滤后,如果滤液仍然浑浊,其原因可能是 ________ 。 ( 4 )通过以上操作只能除去粗盐中难溶性杂质,欲除去可溶性杂质如 MgCl 2 、 CaCl 2 ,得到纯净的 NaCl ,还需依次用到 NaOH 溶液、 Na 2 CO 3 溶液和稀盐酸(三种药品均过量); ①碳酸钠溶液要过量的原因是 _______ ; ②稀盐酸的作用是 _______ 。 |
|
| 19. | 详细信息 |
|
阅读下列材料文字。 材料一:绿色化学的理念是使污染消除在产生的源头,不再使用有毒、有害的物质,不再产生废物,这是从根本上消除污染的对策,过程和终端均为零排放或零污染。世界上很多国家己把 “化学的绿色化”作为新世纪化学发展的主要方向之一。原子经济性和“ 5R ”原则是绿色化学的核心内容。“ 5R ”原则,即 Reduce (减量); Reuse (循环使用); Recycling (回收); Regeneration (再生);: Rejection (拒用)。 材料二:垃圾分类一般是指按一定规定或标准将垃圾分类储存,分类投放和分类搬运,从而变成公共资源的一系列活动的总称。分类的目的是提高垃圾的资源价值和经济价值,力争物尽其用。进行垃圾分类回收可以降低垃圾处理成本,减少土地资源的消耗,具有社会、经济、环保等多方面的好处。垃圾分类从我做起。 绿水青山就是金山银山,保护环境,人人有责。 根据材料内容和所学化学知识,回答下列问题: ( 1 ) “绿色化学”的理念是 _______ 。 ( 2 )今年起国家提倡用纸质吸管代替塑料吸管,你认为这一做法最能体现 “ 5R ”原则中的 _______ ,请简单阐述理由 ______ ; ( 3 )下列属于可回收垃圾的是 ________ 。 A 废旧报纸 B 生锈铁管 C 矿泉水瓶 D 腐烂水果 ( 4 )垃圾分类回收的好处是 _______ 。 |
|
| 20. | 详细信息 |
|
请用化学用语回答 : ( 1 )两个汞原子 ________ 。 ( 2 )天然气的主要成分 ________ 。 ( 3 )亚铁离子 ________ 。 ( 4 )人体胃液中含有的酸 _________ 。 |
|
| 21. | 详细信息 |
|
根据下图所示回答问题: ( 1 ) A 、 B 、 C 、 D 中,表示钙离子结构示意图的是 _________ (填字母,下同),与钙原子化学性质相似的是 ________ ,表示同一种元素的是 _________ 。 ( 2 )具有相对稳定结构的原子是 ________ (填字母)图 E 中 “20” 表示 ________ 。 |
|
| 22. | 详细信息 |
|
化学就在我们身边,人类的生活离不开化学。请回答下列问题: ( 1 )饮用水硬度过大会影响人体健康。生活中降低水硬度常用的方法是 _______ 。 ( 2 )人们每天需要从食物中摄取充足的营养素。下列食物中富含蛋白质的是 ________ 。 A 馒头 B 西红柿 C 牛肉 D 黄花鱼 ( 3 )下列物质可用作食品干燥剂的是 ______ 。 A 生石灰 B 熟石灰 C 火碱 D 纯碱 ( 4 )未经处理的煤燃烧产生的 _______ (写化学式)排放到空气中,会形成酸雨; ( 5 )甲醛( CH 2 O )为室内装修产生的有害物质之一。为去除污染,科学家研制出一种新型的催化剂,在其催化作用下,甲醛与空气中的氧气反应生成两种最常见的氧化物,该反应的化学方程式为 ______ 。 |
|
| 23. | 详细信息 |
|
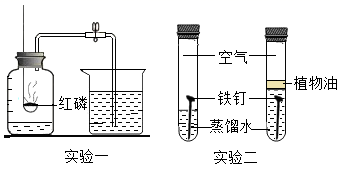
下图所示是初中化学常见的四个实验,请依图回答: ( 1 )实验一:红磷需过量的目的是 ________ 。 ( 2 )实验二:通过对比实验得出结论:铁生锈需要和 ________ 接触; ( 3 )实验三:证明二氧化碳具有的化学性质是 _______ 。 ( 4 )实验四:由于 _______ 不同造成硫燃烧的现象不同。 |
|
| 24. | 详细信息 | |||||||||||||||||||||||||||||
|
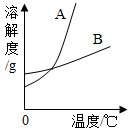
数据处理是对数据进行加工的过程,列表法和作图法是常用的数据处理方法。已知 KNO 3 和 KCl 在不同温度时的溶解度如下表所示,请回答下列问题:
( 1 )依据上表数据,绘制 KNO 3 和 KCl 的溶解度曲线,下图中能表示 KNO 3 溶解度曲线的是 _______ (填 “ A ”或“ B ”); ( 2 )分析表中数据可知, KNO 3 和 KCl 在某一温度时具有相同的溶解度 x ,则 x 取值范围是 _______ 。 ( 3 ) 40 ℃ 时,将 140gKCl 的饱和溶液恒温蒸发 10g 水后,析出 KCl 晶体的质量为 ______ g 。 ( 4 )要使 A 物质的不饱和溶液转化为饱和溶液,方法是 _______ 。 ( 5 )将 60 ℃时 KNO 3 和 KCl 的饱和溶液降温至 20 ℃,析出晶体质量关系为 ________ 。 A KNO 3 > KCl B KNO 3 < KCl C KNO 3 =KCl D 无法确定 |
||||||||||||||||||||||||||||||
| 25. | 详细信息 |
|
实验室制取气体时需要的一些装置如下图所示,请回答下列问题: ( 1 )写出标有序号的仪器名称: ② _______ 。 ( 2 )写出用 A 装置制取氧气的化学方程式 _______ 。 ( 3 )实验室制取 CO 2 时,收集装置通常只选择 E 的原因是 _______ ,若要收集一瓶干燥的二氧化碳,应在 E 之前连接装置 _______ (填字母); ( 4 )实验室常用高锰酸钾固体和浓盐酸在常温下反应制取氯气( C1 2 ),用该方法制取氯气时选用的发生装置是 ______ (填字母);如果用 G 装置收集氯气,气体应从 _______ (填 “ a ”或“ b ”)口进;氯气有毒,可与水反应生成酸,为防止其污染空气,应选择 ______ 性溶液吸收尾气。 |
|
| 26. | 详细信息 |
|
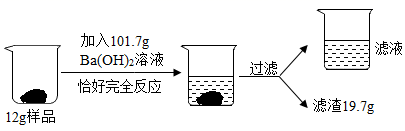
小明用含碳酸钠的氢氧化钠样品进行了如图所示的实验。请回答: ( 1 )此实验中发生反应的化学方程式是 。 ( 2 )过滤后滤液中溶质为 ,其质量分数是 。 |
|