2017жұҹиӢҸд№қе№ҙзә§дёӢеӯҰжңҹиӢҸж•ҷзүҲеҲқдёӯеҢ–еӯҰжңҲиҖғиҜ•еҚ·
| 1. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҸҳеҢ–дёҚеұһдәҺеҢ–еӯҰеҸҳеҢ–зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺ й“қз®”еңЁж°§ж°”дёӯзҮғзғ§В В В BпјҺ й“ңйҰ–иЎЁйқўдә§з”ҹй“ңз»ҝ CпјҺ ж°ҙи’ёеҸ‘В DпјҺ ж·ҖзІүж°ҙи§ЈжҲҗи‘Ўиҗ„зі–
|
|
| 2. | иҜҰз»ҶдҝЎжҒҜ |
|
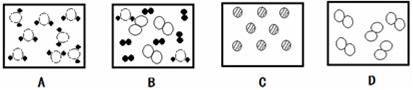
вҖңй—»йҰҷиҜҶиҢ¶вҖқж„ҸжҖқжҳҜйҖҡиҝҮй—»зҡ„ж–№жі•еҲӨж–ӯеҮәиҢ¶зҡ„зұ»еҲ«пјҺдәә们иғҪеӨҹй—»еҲ°иҢ¶йҰҷзҡ„еҺҹеӣ жҳҜпјҲгҖҖгҖҖпјү AпјҺеҲҶеӯҗд№Ӣй—ҙеӯҳеңЁй—ҙйҡ” BпјҺеҲҶеӯҗиҙЁйҮҸе’ҢдҪ“з§ҜеҫҲе°Ҹ CпјҺеҲҶеӯҗеңЁдёҚж–ӯзҡ„иҝҗеҠЁ DпјҺеҲҶеӯҗжҳҜз”ұеҺҹеӯҗжһ„жҲҗзҡ„
|
|
| 3. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еұһдәҺзәҜеҮҖзү©зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺеҮҖеҢ–еҗҺзҡ„з©әж°” BпјҺзҹҝжіүж°ҙВ В CпјҺеҠ зўҳйЈҹзӣҗ DпјҺй«ҳй”°й…ёй’ҫ
|
|
| 4. | иҜҰз»ҶдҝЎжҒҜ |
|
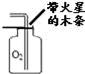
еҰӮеӣҫе®һйӘҢж“ҚдҪңй”ҷиҜҜзҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺ В й—»ж°”дҪ“ж°”е‘і BпјҺ жЈҖжҹҘж°”еҜҶжҖ§В В В CпјҺ В иҜ»еҸ–ж¶ІдҪ“дҪ“з§ҜВ В DпјҺ В зЁҖйҮҠжө“зЎ«й…ё
|
|
| 5. | иҜҰз»ҶдҝЎжҒҜ |
|
жҲ‘еӣҪеҚ—жө·жө·еә•и•ҙи—ҸзқҖдё°еҜҢзҡ„й”°з»“ж ёп№Јп№Јеҗ«жңүй”°гҖҒй“ҒгҖҒй“ңзӯүйҮ‘еұһзҡ„зҹҝзү©пјҺе·ІзҹҘй”°еҺҹеӯҗзҡ„иҙЁеӯҗж•°дёә25пјҢзӣёеҜ№еҺҹеӯҗиҙЁйҮҸдёә55пјҢеҲҷй”°еҺҹеӯҗзҡ„з”өеӯҗж•°дёәпјҲгҖҖгҖҖпјү AпјҺ25В В BпјҺ30В В CпјҺ55В В DпјҺ80
|
|
| 6. | иҜҰз»ҶдҝЎжҒҜ |
|
еҢ–еӯҰж”Ҝ撑科жҠҖпјҢдҝғиҝӣжҲ‘еӣҪиҲӘеӨ©дәӢдёҡиҝ…йҖҹеҸ‘еұ•пјҺеңЁйЈһиҲ№зҡ„зҒ«з®ӯжҺЁиҝӣеҷЁдёӯеёёиЈ…жңүж¶ІжҖҒиӮј[N2H4]е’ҢиҝҮж°§еҢ–ж°ў[H2O2]пјҢе®ғ们混еҗҲж—¶зҡ„еҸҚеә”ж–№зЁӢејҸдёәпјҡ2H2O2+N2H4в•җN2+4XпјҢеҲҷдёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺиҜҘеҢ–еӯҰж–№зЁӢејҸдёӯXзҡ„еҢ–еӯҰејҸдёәH2O BпјҺеҸҚеә”еүҚеҗҺеҺҹеӯҗжҖ»ж•°еҸ‘з”ҹеҸҳеҢ– CпјҺиҜҘеҸҚеә”дёәзҪ®жҚўеҸҚеә” DпјҺж°®жҳҜең°еЈідёӯеҗ«йҮҸжңҖй«ҳзҡ„йқһйҮ‘еұһе…ғзҙ
|
|
| 7. | иҜҰз»ҶдҝЎжҒҜ |
|
еҗ‘зЎқ酸银е’ҢзЎқй…ёй“ңзҡ„ж··еҗҲжә¶ж¶ІдёӯеҠ е…ҘдёҖе®ҡйҮҸзҡ„й”ҢзІүпјҺе……еҲҶеҸҚеә”еҗҺиҝҮж»ӨпјҢеҫҖж»Өж¶Ідёӯж»ҙеҠ зӣҗй…ёпјҢжңүзҷҪиүІжІүж·Җз”ҹжҲҗпјҺдёӢеҲ—иҜҙжі•дёӯжӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺжүҖеҫ—жә¶ж¶ІдёӯеҸҜиғҪеҗ«жңүCu2+ BпјҺжүҖеҫ—ж»ӨжёЈдёӯеҸҜиғҪеҗ«жңүй“ңе’Ңй”Ң CпјҺжүҖеҫ—ж»Өж¶ІдёӯдёҖе®ҡеҗ«жңүAg+гҖҒZn2+гҖҒCu2+ DпјҺжүҖеҫ—ж»ӨжёЈдёӯдёҖе®ҡеҗ«жңү银е’Ңй“ң
|
|
| 8. | иҜҰз»ҶдҝЎжҒҜ |
|
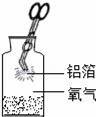
еҢ–еӯҰеӯҰд№ е°Ҹз»„еҒҡе®һйӘҢж—¶и®°еҪ•дәҶдёӢеҲ—е®һйӘҢзҺ°иұЎпјҢе…¶дёӯжӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺеңЁиҝҮж°§еҢ–ж°ўжә¶ж¶ІдёӯеҠ е…Ҙе°‘йҮҸдәҢж°§еҢ–й”°пјҢз«ӢеҚіз”ҹжҲҗдәҶеӨ§йҮҸж°§ж°” BпјҺзЎ«еңЁз©әж°”дёӯзҮғзғ§пјҢеҸ‘еҮәжҳҺдә®зҡ„и“қзҙ«иүІзҒ«з„°пјҢдә§з”ҹеҲәжҝҖжҖ§ж°”е‘ізҡ„ж°”дҪ“ CпјҺеңЁеҗ«жңүй…ҡй…һзҡ„ж°ўж°§еҢ–й’ жә¶ж¶ІдёӯйҖҗж»ҙеҠ е…ҘзЁҖзЎ«й…ёдёӯе’Ңж»ҙе®ҡж—¶пјҢжә¶ж¶ІйўңиүІз”ұзәўиүІйҖҗжёҗеҸҳжҲҗж— иүІ DпјҺжү“ејҖзӣӣжңүжө“зӣҗй…ёзҡ„瓶зӣ–пјҢ瓶еҸЈдә§з”ҹеӨ§йҮҸзҷҪиүІзғҹйӣҫ
|
|
| 9. | иҜҰз»ҶдҝЎжҒҜ |
|
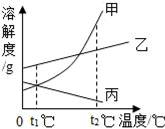
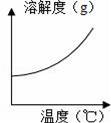
еҰӮеӣҫжҳҜз”ІгҖҒд№ҷгҖҒдёҷдёүз§Қзү©иҙЁпјҲеқҮдёҚеҗ«з»“жҷ¶ж°ҙпјүзҡ„жә¶и§ЈеәҰжӣІзәҝпјҺзҺ°жңүt2в„ғж—¶з”ІгҖҒд№ҷгҖҒдёҷдёүз§Қзү©иҙЁзҡ„йҘұе’Ңжә¶ж¶ІпјҲж— еӣәдҪ“еӯҳеңЁпјүпјҺ дёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү
AпјҺдёүз§Қзү©иҙЁжә¶и§ЈеәҰеӨ§е°Ҹдҫқж¬Ўдёәпјҡд№ҷпјһдёҷпјһз”І BпјҺе°Ҷжё©еәҰз”ұt2в„ғйҷҚеҲ°t1в„ғж—¶пјҢжһҗеҮәз”Ізҡ„иҙЁйҮҸжҜ”д№ҷеӨҡ CпјҺиӢҘз”Ідёӯеҗ«жңүе°‘йҮҸжқӮиҙЁд№ҷпјҢеҸҜйҮҮз”ЁйҷҚжё©з»“жҷ¶зҡ„ж–№жі•иҝӣиЎҢжҸҗзәҜ DпјҺе°Ҷжё©еәҰз”ұt2в„ғйҷҚеҲ°t1в„ғпјҢжүҖеҫ—жә¶ж¶Ідёӯжә¶иҙЁзҡ„иҙЁйҮҸеҲҶж•°з”ұеӨ§еҲ°е°Ҹзҡ„йЎәеәҸдёәпјҡд№ҷпјһдёҷ=з”І
|
|
| 10. | иҜҰз»ҶдҝЎжҒҜ |
|
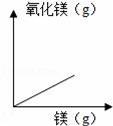
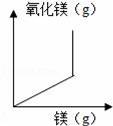
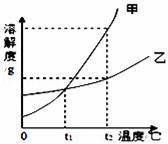
дёӢеҲ—еӣҫиұЎдёҺеҜ№еә”зҡ„е®һйӘҢзҺ°иұЎзӣёз¬Ұзҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺ В В зЁҖйҮҠNaOHжә¶ж¶ІВ В В BпјҺ В й•ҒеңЁз©әж°”дёӯзҮғзғ§ CпјҺ й“ҒеҠ е…ҘзЁҖзӣҗй…ёдёӯВ В В DпјҺ В В В ж°§ж°”зҡ„жә¶и§ЈеәҰ
|
|
| 11. | иҜҰз»ҶдҝЎжҒҜ |
|
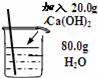
жҢүдёӢеҲ—иЈ…зҪ®е®һйӘҢпјҢдёҚиғҪиҫҫеҲ°еҜ№еә”зӣ®зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺ 收йӣҶH2В В В BпјҺ В В В O2йӘҢж»Ў CпјҺ й…ҚеҲ¶20%зҡ„CaпјҲOHпјү2жә¶ж¶І DпјҺ В В В В йҷӨеҺ»COдёӯзҡ„CO2
|
|
| 12. | иҜҰз»ҶдҝЎжҒҜ |
|
е°Ҹдә®еҗҢеӯҰе®һйӘҢдёӯжөӢеҫ—зҡ„дёӢеҲ—ж•°жҚ®дёӯпјҢдёҚеҗҲзҗҶзҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺз”ЁpHиҜ•зәёжөӢеҫ—жҹҗжә¶ж¶Ізҡ„pHдёә10.3 BпјҺз”Ё10mLйҮҸзӯ’йҮҸеҸ–8.0mLж°ҜеҢ–й’ жә¶ж¶І CпјҺз”ЁжүҳзӣҳеӨ©е№із§°еҫ—жҹҗеӣәдҪ“ж ·е“Ғзҡ„иҙЁйҮҸдёә8.5g DпјҺз”ЁдҪ“жё©и®ЎжөӢеҫ—иҮӘе·ұзҡ„дҪ“жё©дёә37.0в„ғ
|
|
| 13. | иҜҰз»ҶдҝЎжҒҜ |
|
е°ҸзәўеҗҢеӯҰдёәжҺўз©¶XгҖҒYгҖҒZдёүз§ҚйҮ‘еұһпјҲйғҪдёҚжҳҜAgпјүзҡ„жҙ»еҠЁжҖ§йЎәеәҸпјҢеҒҡдәҶеҰӮдёӢе®һйӘҢпјҡ пјҲ1пјүжҠҠXе’ҢYеҲҶеҲ«ж”ҫе…ҘзЁҖH2SO4дёӯпјҢXжә¶и§Је№¶дә§з”ҹH2пјҢYдёҚеҸҚеә” пјҲ2пјүжҠҠYе’ҢZеҲҶеҲ«ж”ҫе…ҘAgNO3жә¶ж¶ІдёӯпјҢеңЁYиЎЁйқўжңүAgжһҗеҮәпјҢиҖҢZжІЎжңүеҸҳеҢ– ж №жҚ®д»ҘдёҠе®һйӘҢдәӢе®һпјҢдёӢеҲ—йҮ‘еұһжҙ»еҠЁжҖ§йЎәеәҸз”ұејәеҲ°ејұжҺ’еҲ—жӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺXпјһYпјһпјҲHпјүпјһZВ В BпјҺXпјһYпјһHпјһZВ В CпјҺXпјһYпјһZпјһAgВ DпјҺXпјһпјҲHпјүпјһYпјһZ
|
|
| 14. | иҜҰз»ҶдҝЎжҒҜ |
|
еңЁдёҚз”ЁжҢҮзӨәеүӮзҡ„жқЎд»¶дёӢпјҢж¬Іе°Ҷеҗ«жңүзӣҗй…ёзҡ„ж°ҜеҢ–й’ҷжә¶ж¶Із”ұй…ёжҖ§иҪ¬еҢ–дёәдёӯжҖ§пјҢдё”дёҚж··е…Ҙе…¶е®ғжқӮиҙЁпјҢеә”йҖүз”Ёзҡ„иҜ•еүӮжҳҜпјҲгҖҖгҖҖпјү AпјҺжҫ„жё…зҹізҒ°ж°ҙВ В BпјҺж°§еҢ–й’ В В CпјҺзҹізҒ°зҹізІүжң«В В DпјҺз”ҹзҹізҒ°зІүжң«
|
|
| 15. | иҜҰз»ҶдҝЎжҒҜ |
|
вҖңдҪҺзўіз”ҹжҙ»вҖқз®ҖиЁҖд№Ӣе°ұжҳҜйҷҚдҪҺдәҢж°§еҢ–зўізҡ„жҺ’ж”ҫпјҢе°ұжҳҜдҪҺиғҪйҮҸгҖҒдҪҺж¶ҲиҖ—гҖҒдҪҺејҖж”Ҝзҡ„з”ҹжҙ»ж–№ејҸпјҺдёӢеҲ—еҒҡжі•дёҚз¬ҰеҗҲдҪҺзўіз”ҹжҙ»ж–№ејҸзҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺйӘ‘иҮӘиЎҢиҪҰдёҠеӯҰ BпјҺеӨҡз”ЁзӣёеҜ№е»үд»·зҡ„з…Ө CпјҺз”Ёж·ҳзұіж°ҙжөҮиҠұ DпјҺеҮҸе°‘дҪҝз”ЁеЎ‘ж–ҷиўӢ
|
|
| 16. | иҜҰз»ҶдҝЎжҒҜ |
|
й“ҒеҲ¶е“Ғй”ҲиҡҖзҡ„иҝҮзЁӢпјҢе®һйҷ…дёҠжҳҜй“ҒдёҺз©әж°”дёӯзҡ„гҖҖгҖҖе’ҢгҖҖгҖҖзӯүеҸ‘з”ҹеҢ–еӯҰеҸҚеә”зҡ„иҝҮзЁӢпјҺжҚ®жңүе…іиө„ж–ҷжҠҘеҜјпјҢдё–з•ҢдёҠжҜҸе№ҙеӣ и…җиҡҖиҖҢжҠҘеәҹзҡ„йҮ‘еұһи®ҫеӨҮжҲ–жқҗж–ҷзӣёеҪ“дәҺе№ҙдә§йҮҸзҡ„20%пҪһ40%пјҺдҝқжҠӨйҮ‘еұһиө„жәҗпјҢдәәдәәжңүиҙЈпјҺиҜ·еҶҷеҮәдёҖжқЎйҳІжӯўй“ҒеҲ¶е“Ғз”ҹй”Ҳзҡ„ж–№жі•гҖҖгҖҖпјҺй“Ғй”Ҳзҡ„дё»иҰҒжҲҗеҲҶжҳҜгҖҖгҖҖпјҢйҖҡеёёеҸҜз”ЁгҖҖгҖҖйҷӨеҺ»й“ҒиЎЁйқўзҡ„й“Ғй”ҲпјҢеҶҷеҮәжңүе…іеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸпјҡгҖҖгҖҖпјҺ
|
|
| 17. | иҜҰз»ҶдҝЎжҒҜ |
|
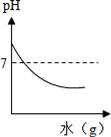
д»Ҡжңүв‘ иӮҘзҡӮж°ҙ в‘ЎйЈҹзӣҗж°ҙ в‘ўжқЁжў…жұҒ в‘ЈзҷҪзі–ж°ҙ в‘Өи’ёйҰҸж°ҙдә”з§Қж¶ІдҪ“пјҢж №жҚ®дҪ зҡ„з”ҹжҙ»з»ҸйӘҢеҲӨж–ӯпјҢе…¶дёӯpHпјң7зҡ„жҳҜгҖҖгҖҖиҜҘжә¶ж¶Ідёӯж»ҙе…Ҙзҙ«иүІзҹіи•Ҡжә¶ж¶ІпјҢзҹіи•Ҡжә¶ж¶ІжҳҫгҖҖгҖҖиүІпјӣpHпјһ7зҡ„жҳҜгҖҖгҖҖ пјҲеЎ«еәҸеҸ·пјүпјҢиҜҘжә¶ж¶Ідёӯж»ҙе…Ҙзҙ«иүІзҹіи•Ҡжә¶ж¶ІпјҢзҹіи•Ҡжә¶ж¶ІжҳҫгҖҖгҖҖиүІпјҺ
|
|
| 18. | иҜҰз»ҶдҝЎжҒҜ |
|
ж°ҙе’Ңжә¶ж¶ІеңЁз”ҹдә§з”ҹжҙ»дёӯйҮҚиҰҒзҡ„дҪңз”ЁпјҺ пјҲ1пјүиҮӘжқҘж°ҙеҺӮеёёз”Ёзҡ„еҮҖж°ҙж–№жі•жңүжІүж·ҖгҖҒгҖҖгҖҖгҖҒеҗёйҷ„гҖҒж¶ҲжҜ’зӯүпјҢеҗёйҷ„иҝҮзЁӢдёӯйңҖиҰҒз”ЁеҲ°зҡ„зү©иҙЁжҳҜгҖҖжҙ»гҖҖпјӣеңЁж—Ҙеёёз”ҹжҙ»дёӯйүҙеҲ«зЎ¬ж°ҙе’ҢиҪҜж°ҙеёёз”ЁгҖҖгҖҖпјҢеёёз”ЁжқҘйҷҚдҪҺж°ҙзҡ„зЎ¬еәҰзҡ„ж–№жі•жҳҜгҖҖгҖҖпјҢж°ҙжҳҜдёҖз§Қе®қиҙөзҡ„иҮӘ然иө„жәҗпјҢжҲ‘们еҝ…йЎ»зҲұжҠӨж°ҙиө„жәҗпјҺйў„йҳІж°ҙжұЎжҹ“зҡ„жҺӘж–ҪжңүгҖҖгҖҖпјҲеҶҷдёҖжқЎеҚіеҸҜпјүпјҺ пјҲ2пјүеҰӮеӣҫжҳҜз”ІгҖҒд№ҷдёӨз§Қзү©иҙЁзҡ„жә¶и§ЈеәҰжӣІзәҝпјҢеӣһзӯ”дёӢеҲ—й—®йўҳпјҡ в‘ t1в„ғж—¶пјҢз”ІгҖҒд№ҷдёӨз§Қжә¶ж¶Ідёӯжә¶иҙЁзҡ„иҙЁйҮҸеҲҶж•°дёҖе®ҡзӣёзӯүгҖҖгҖҖпјҲеЎ«вҖңеҜ№вҖқжҲ–вҖңй”ҷвҖқпјүпјӣ в‘ЎиӢҘеӣәдҪ“з”Ідёӯеҗ«жңүе°‘йҮҸд№ҷж—¶еҸҜз”ЁгҖҖгҖҖж–№жі•жҸҗзәҜз”ІпјҲеЎ«вҖңи’ёеҸ‘з»“жҷ¶вҖқжҲ–вҖңеҶ·еҚҙз»“жҷ¶вҖқпјүпјӣ в‘ўt2в„ғз”ЁзӯүиҙЁйҮҸзҡ„з”ІгҖҒд№ҷдёӨз§Қзү©иҙЁй…ҚеҲ¶з”ІгҖҒд№ҷзҡ„йҘұе’Ңжә¶ж¶ІйңҖиҰҒж°ҙзҡ„иҙЁйҮҸз”ІгҖҖгҖҖд№ҷпјҲеЎ«вҖңпјһвҖқвҖңпјңвҖқжҲ–вҖң=вҖқпјүпјӣ в‘Јй…ҚеҲ¶дёҖе®ҡжә¶иҙЁиҙЁйҮҸеҲҶж•°зҡ„з”Ізү©иҙЁжә¶ж¶ІпјҢд»ҘдёӢж“ҚдҪңдёӯдјҡеҜјиҮҙжүҖй…ҚеҲ¶жә¶ж¶Іжә¶иҙЁиҙЁйҮҸеҲҶж•°еҒҸдҪҺзҡ„жҳҜгҖҖпјҺ AгҖҒйҮҸзӯ’йҮҸеҸ–ж°ҙж—¶д»°и§ҶиҜ»ж•°гҖҖгҖҖгҖҖBгҖҒй…ҚеҲ¶еҘҪзҡ„жә¶ж¶Іеҗ‘з»ҶеҸЈз“¶иҪ¬з§»ж—¶жә…еҮәВ В В В CгҖҒеӣәдҪ“з”Ідёӯеҗ«жңүжқӮиҙЁпјҺ
|
|
| 19. | иҜҰз»ҶдҝЎжҒҜ |
|
зӣҗеҹҺжңәеңәиҲӘз«ҷжҘјдҪҝз”ЁдәҶй’ўжһ¶з»“жһ„ пјҲ1пјүй’ўеұһдәҺгҖҖгҖҖпјҲвҖңзәҜеҮҖзү©вҖқжҲ–вҖңж··еҗҲзү©вҖқпјү пјҲ2пјүеҰӮеӣҫдёӯпјҢеҸҜиЎЁзӨәйҮ‘еұһй“Ғзҡ„жҳҜгҖҖгҖҖпјҺ
|
|
| 20. | иҜҰз»ҶдҝЎжҒҜ |
|
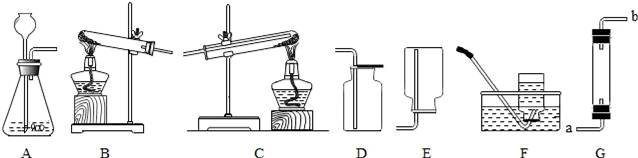
жҹҗеҗҢеӯҰеҜ№ж°”дҪ“зҡ„е®һйӘҢе®ӨеҲ¶жі•дҪңдәҶд»ҘдёӢжҺўз©¶пјҢиҜ·ж №жҚ®еҰӮеӣҫжҢүиҰҒжұӮеӣһзӯ”й—®йўҳпјҡ
пјҲ1пјүиЈ…зҪ®Aдёӯжҹҗз§Қд»ӘеҷЁзҡ„дёӢз«Ҝеҝ…йЎ»дјёе…ҘеҲ°ж¶ІдҪ“йҮҢпјҢиҜҘд»ӘеҷЁзҡ„еҗҚз§°жҳҜгҖҖгҖҖпјҺ пјҲ2пјүе®һйӘҢе®Өз”Ёй«ҳй”°й…ёй’ҫеҲ¶еҸ–O2зҡ„еҸ‘з”ҹиЈ…зҪ®жҳҜгҖҖгҖҖпјҢпјҲжүҖйҖүиЈ…зҪ®з”Ёеӯ—жҜҚиЎЁзӨәпјүжҹҗеҗҢеӯҰз”ЁжҺ’ж°ҙ法收йӣҶж°§ж°”пјҢдёәдәҶйҳІжӯўж°ҙж§ҪеҶ…зҡ„ж°ҙеҸҳжҲҗзәўиүІпјҢе…¶жӯЈзЎ®зҡ„ж“ҚдҪңжҳҜгҖҖгҖҖпјҺ пјҲ3пјүеҶҷеҮәе®һйӘҢе®Өз”ЁAиЈ…зҪ®еҲ¶еҸ–ж°§ж°”зҡ„еҢ–еӯҰж–№зЁӢејҸпјҡгҖҖгҖҖпјҺ пјҲ4пјүе®һйӘҢе®ӨиӢҘеҲ©з”ЁGиЈ…зҪ®ж”¶йӣҶCO2пјҢеҲҷж°”дҪ“еҝ…йЎ»д»ҺгҖҖaгҖҖз«ҜйҖҡе…ҘпјҺпјҲз”Ёеӯ—жҜҚиЎЁзӨәпјү
|
|
| 21. | иҜҰз»ҶдҝЎжҒҜ | ||||||
|
е®һйӘҢе‘ҳе°Ҹе‘ЁеңЁеӯҰжңҹжң«ж•ҙзҗҶе®һйӘҢд»ӘеҷЁж—¶еҸ‘зҺ°жңүдёҖ瓶ж ҮзӯҫжЁЎзіҠзҡ„жә¶ж¶ІпјҢеҰӮдёӢеӣҫпјҺ иҜ·дҪ е’Ңе°Ҹе‘ЁдёҖиө·жҺўз©¶иҜҘжә¶ж¶Ізҡ„жҲҗеҲҶпјҢ并жөӢе®ҡе…¶иҙЁйҮҸеҲҶж•°пјҺ 第дёҖжӯҘпјҡзҢңжғіе№¶йӘҢиҜҒиҜҘжә¶ж¶Ізҡ„жә¶иҙЁжҳҜд»Җд№ҲпјҺ зҢңжғіпјҡж №жҚ®ж ҮзӯҫеҸҜзҹҘпјҢиҝҷ瓶жә¶ж¶ІеҸҜиғҪжҳҜHClгҖҒKClгҖҒNaClзӯү еҗ«жңүж°ҜзҰ»еӯҗзҡ„й…ёжҲ–зӣҗпјҺ йӘҢиҜҒпјҡ
第дәҢжӯҘпјҡжөӢе®ҡиҜҘжә¶ж¶Ізҡ„жә¶иҙЁиҙЁйҮҸеҲҶж•° е®һйӘҢеҺҹзҗҶпјҡпјҲ1пјүз”Ёе·ІзҹҘжө“еәҰзҡ„ж°ўж°§еҢ–й’ жә¶ж¶Іе’Ңзӣҗй…ёеҸҚеә”пјҢеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸдёәпјҡ NaOH+HCl=NaCl+H20 пјҲ2пјүеҪ“зӣҗй…ёе’Ңж°ўж°§еҢ–й’ жҒ°еҘҪе®Ңе…ЁеҸҚеә”ж—¶пјҢеҶҚеўһеҠ дёҖж»ҙж°ўж°§еҢ–й’ жә¶ж¶ІпјҢжә¶ж¶Іе°ұе‘ҲзўұжҖ§пјҲеҸҜд»ҘдҪҝж— иүІй…ҡй…һеҸҳжҲҗзәўиүІпјүпјҢиҖҢдёҖж»ҙж°ўж°§еҢ–й’ жә¶ж¶Ізҡ„дҪ“з§ҜзәҰдёә0.05mLпјҢеҜ№жөӢе®ҡз»“жһңзҡ„еҪұе“ҚеҫҲе°ҸпјҢеҸҜеҝҪз•ҘдёҚи®ЎпјҺ е®һйӘҢжӯҘйӘӨпјҡпјҲ1пјүеҸ–жңӘзҹҘжө“еәҰзҡ„зӣҗй…ё20gеҖ’е…Ҙзғ§жқҜдёӯпјҢеҗ‘е…¶дёӯж»ҙеҠ 2ж»ҙж— иүІй…ҡй…һжә¶ж¶ІпјҺжӯӨж—¶жә¶ж¶Іе‘ҲгҖҖгҖҖиүІпјҺ пјҲ2пјүйҮҸеҸ–иҙЁйҮҸеҲҶж•°1%зҡ„ж°ўж°§еҢ–й’ жә¶ж¶І50mLпјҲеҜҶеәҰиҝ‘дјјдёә1.0g/mLпјүпјҢз”Ёиғ¶еӨҙж»ҙз®ЎйҖҗж»ҙж»ҙеҠ иҜҘж°ўж°§еҢ–й’ жә¶ж¶ІеҲ°зӣҗй…ёдёӯпјҢи§ӮеҜҹеҲ°гҖҖгҖҖпјҢеҒңжӯўж»ҙеҠ пјҢеү©дҪҷж°ўж°§еҢ–й’ жә¶ж¶Ізҡ„10mLпјҺ ж•°жҚ®еӨ„зҗҶпјҡи®Ўз®—иҜҘзӣҗй…ёжә¶ж¶Ізҡ„жә¶иҙЁиҙЁйҮҸеҲҶж•°пјҺ е®һйӘҢеҸҚжҖқпјҡе°Ҹе‘ЁеңЁеҒҡе®һйӘҢзҡ„ж—¶зӣӣж”ҫеҫ…жөӢзӣҗй…ёзҡ„зғ§жқҜпјҲе®һйӘҢжӯҘйӘӨдёӯеҠ зӮ№зҡ„зғ§жқҜпјүеңЁиЈ…е…Ҙзӣҗй…ёеүҚеҶ…еЈҒйҷ„зқҖиҫғеӨҡж°ҙпјҢз”ЁиҜҘзғ§жқҜе®ҢжҲҗдёҠиҝ°е®һйӘҢдјҡеҜјиҮҙз»“жһңгҖҖгҖҖпјҲеЎ«вҖңеҒҸеӨ§вҖқвҖңеҒҸе°ҸвҖқжҲ–вҖңж— еҪұе“ҚвҖқпјүпјҺ
|
|||||||
- 2018еұҠд№қе№ҙзә§дёҠеҚҠжңҹжңҹдёӯиҖғиҜ•еҢ–еӯҰиҖғйўҳеёҰзӯ”жЎҲе’Ңи§ЈжһҗпјҲжұҹиӢҸзңҒиҝһдә‘жёҜеёӮзҒҢеҚ—еҺҝпјү
- 2017еұҠд№қе№ҙзә§дёӢеҚҠе№ҙжңҹдёӯиҖғиҜ•еҢ–еӯҰиҜ•еҚ·пјҲеұұдёңзңҒдёңжҳҢеәңеҢәжўҒж°ҙй•ҮдёӯеҝғдёӯеӯҰпјү
- 2018еұҠд№қе№ҙзә§еӯҰдёҡиҖғиҜ•еҢ–еӯҰиҖғиҜ•пјҲеұұдёңзңҒеҫ·е·һеёӮпјү
- 2018е№ҙдёӯиҖғ еҢ–еӯҰ дёҖиҪ®еҹәзЎҖеӨҚд№ пјҡдё“йўҳдәҢеҚҒ еёёи§Ғзҡ„й…ёе’ҢзўұпјҲеӨҮиҖғпјү
- 2015-2016е№ҙд№қе№ҙзә§еҗҺеҚҠжңҹеҢ–еӯҰдәҢжЁЎиҖғиҜ•иҖғиҜ•пјҲдёҠжө·еёӮй—өиЎҢеҢәпјү
- 2017е№ҙдёӯиҖғжЁЎжӢҹеҢ–еӯҰиҖғиҜ•пјҲйҷ•иҘҝзңҒй“ңе·қеёӮиҖҖе·һеҢәпјү
- 2018еұҠд№қе№ҙзә§12жңҲжңҲиҖғеҢ–еӯҰиҖғиҜ•йўҳпјҲеұұдёңзңҒдёңжҳҢеәңеҢәжўҒж°ҙй•ҮдёӯеҝғдёӯеӯҰпјү
- 2016-2017е№ҙд№қе№ҙзә§еҢ–еӯҰеҲқдёӯжҜ•дёҡзҸӯ第дёҖж¬Ўж•ҷеӯҰиҙЁйҮҸзӣ‘жөӢиҖғиҜ•иҖғиҜ•пјҲе№ҝиҘҝзңҒе№іеҚ—еҺҝпјү