2017山东九年级下学期人教版初中化学学业考试
| 1. | 详细信息 |
|
下列变化属于化学变化的是
A. 天然气燃烧 B. 品红扩散 C. 研碎药品 D. 干冰升华
|
|
| 2. | 详细信息 |
|
下列各组物质的俗称、化学式、用途不一致的是 A. 生石灰—CaO —做干燥剂 B. 纯碱—NaOH —治疗胃酸过多 C. 小苏打— NaHCO3—发酵粉 D. 干冰—CO2—人工降雨
|
|
| 3. | 详细信息 |
|
放入水中不能形成溶液的物质是 A. 白糖 B. 食盐 C. 花生油 D. 白酒
|
|
| 4. | 详细信息 |
|
端午节吃粽子是我国的传统习俗,粽子的主要原料为大米、肉、海蛎干、食盐,主要原料中富含糖类物质的是 A. 肉 B. 大米 C. 食盐 D. 海蛎干
|
|
| 5. | 详细信息 | ||||||||||||
|
一些食物的近似pH如下:
下列说法不正确的是 A. 鸡蛋清显碱性 B. 苹果汁和葡萄汁显酸性 C. 葡萄汁比苹果汁的酸性强 D. 胃酸过多的人适宜吃玉米粥
|
|||||||||||||
| 6. | 详细信息 |
|
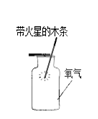
目前,许多烧烤店都改用机制炭作燃料,引燃机制炭可以使用固体酒精,盖灭机制炭可以使用炭灰,下列说法错误的是 A. 酒精的燃烧是为了升高温度 B. 炭灰可以隔绝空气而使机制炭熄灭 C. 酒精的燃烧会升高机制炭的着火点 D. 机制炭做成空心可以增大与空气的接触面积
|
|
| 7. | 详细信息 |
|
硼氢化钠(NaBH4)常用作塑料工业的发泡剂,其中氢元素的化合价为﹣1。硼元素的化合价为 A. ﹣1 B. 0 C. +3 D. +5
|
|
| 8. | 详细信息 |
|
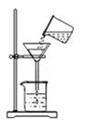
下列实验操作正确的是 A. 测待测溶液pH C. 过滤
|
|
| 9. | 详细信息 |
|
化学是以实验为基础的学科,下列有关实验现象的描述中,正确的是 A. 电解水实验中正极与负极产生的气体体积之比为1∶8 B. 硫粉在氧气中燃烧产生蓝紫色火焰 C. 将铁丝插入硫酸铜溶液中,铁丝上会有红色固体生成,溶液变成无色 D. 在氯化铜溶液中滴加氢氧化钠溶液,有白色沉淀生成
|
|
| 10. | 详细信息 |
|
下列有关化学科学认识正确的是 A. 一定条件下可用石墨制得金刚石 B. “绿色食品”就是绿颜色的食品 C. 氮气不与任何物质反应 D. 纯牛奶中不含任何化学物质
|
|
| 11. | 详细信息 |
|
锡(Sn)是“五金”之一,它的金属活动顺序位于铁和铜之间,则下列反应一定不会发生的是 A. Mg+Sn(NO3)2═Mg(NO3)2+Sn B. Sn+H2SO4═SnSO4+H2↑ C. Sn+Hg(NO3)2═Sn(NO3)2+Hg D. Sn+ZnSO4═SnSO4+Zn
|
|
| 12. | 详细信息 |
|
H7N9型禽流感是一种新型禽流感。据报道,药物扎那米韦(化学式为C12H20N4O7)对人感染H7N9禽流感病毒治疗有效。下列有关扎那米韦的说法不正确的是 A. 扎那米韦属于有机高分子化合物 B. 1个扎那米韦分子由12个碳原子、20个氢原子、4个氮原子和7个氧原子构成 C. 扎那米韦中碳元素、氢元素和氮元素的质量比为36∶5∶14 D. 扎那米韦的相对分子质量为332
|
|
| 13. | 详细信息 |
|
物质的宏观性质与微观组成(或结构)相互联系是化学特有的思维方式,下列对物质性质的微观解释不正确的是 A. 稀有气体的化学性质比较稳定,是因为它们原子的最外层电子数都为8 B. 氧化汞、水都能分解得到氧气,是因为它们的构成中都含有氧原子 C. 金刚石、石墨的物理性质差异较大,是因为碳原子的排列方式不同 D. 氢氧化钾溶液、石灰水都能使石蕊试液变蓝,是因为它们都含有OH﹣
|
|
| 14. | 详细信息 |
|
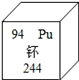
钚(Pu)是原子能工业的一种重要原料,可作为核燃料和核武器的裂变剂。钚元素的有关信息如图,下列说法正确的是
A. 钚原子中有94个中子 B. 钚原子核外有150个电子 C. 钚的相对原子质量是244g D. 钚是金属元素
|
|
| 15. | 详细信息 |
|
推理和归纳是化学学习和研究中常用的思维方法,下列推理正确的是 A. 燃烧一般都伴随着发光、放热现象,所以有发光、放热现象的变化就是燃烧 B. 单质是由一种元素组成的物质,由一种元素组成的物质一定是单质 C. 化学变化中分子种类发生改变,分子种类发生改变的变化一定是化学变化 D. 酸溶液能使紫色试液变红,所以能使紫色石蕊变红的一定是酸的溶液
|
|
| 16. | 详细信息 |
|
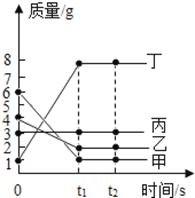
在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量变化情况如图所示,下列说法错误的是
A. 该物质为化合反应 B. 该化学反应中乙、丁的质量变化之比为1∶4 C. 该化学反应中甲、丁的质量变化之比为5∶7 D. 丙可能是该反应的催化剂
|
|
| 17. | 详细信息 |
|
对知识的归纳是学习化学的一种重要方法。下列归纳正确的是 A. 汽油和洗涤剂除油污的原理相同 B. 空气、糖水、高锰酸钾都属于混合物 C. 纯碱、烧碱都属于碱 D. 只有当两种化合物互相交换成分,生成物中有沉淀或气体或水生成时,复分解反应才可以发生
|
|
| 18. | 详细信息 |
|
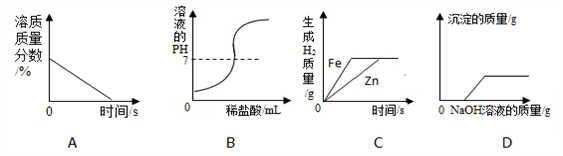
下列图象能正确反映对应变化关系的是
A. 浓硫酸长久露置在空气中 B. 向NaOH溶液中逐滴加入稀盐酸 C. 将一定质量的稀盐酸平均分为两份,分别向其中加入足量的金属Zn和Fe D. 在一定量CuCl2和HCl溶液中逐滴加入NaOH溶液
|
|
| 19. | 详细信息 |
|
在化学实验或日常生活中都应强化安全意识。下列做法符合安全要求的是 A. 氢氧化钠不慎沾到皮肤上,立即用硫酸冲洗 B. 一氧化碳还原氧化铁实验中,将尾气直接排放 C. 使用酒精炉时,直接向燃着的炉内添加酒精 D. 在生产易燃品的厂房,所有的电器设备和照明设备均采用隔离、封闭
|
|
| 20. | 详细信息 | |||||||||||||||
|
除去下列物质中所含的少量杂质(括号内的为杂质),所用试剂及主要实验操作均正确的一组是
A. A B. B C. C D. D
|
||||||||||||||||
| 21. | 详细信息 |
|
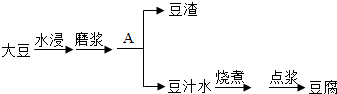
小明喜欢在厨房自己制作点心、饮料等。 (一)他用面粉、鸡蛋、牛奶、白糖、橄榄油等原料制作蛋糕。 (1)上述原料中,富含糖类的是____________。 (2)蛋糕散发出阵阵香味,说明分子具有的性质是_________________________。 (3)用白糖、果汁、小苏打和柠檬酸等制作汽水。从物质溶解的角度看,打开汽水瓶盖,有气泡冒出,说明气体溶解度与______有关;从变化的角度看,配制汽水时,小苏打与柠檬酸(化学式为C6H8O7)发生反应:3NaHCO3+C6H8O7═C6H5O7Na3+3X+3CO2↑,则X的化学式为______。 (二)这几天他想自己制作豆腐。查阅到豆腐制作过程如下:
根据要求回答问题: (4)操作A为 ___________。 (5)豆腐能够预防骨质疏松症,说明豆腐含较丰富的 _____________(填元素符号)。 (6)豆腐的制作过程中需要大量的软水,我们可以用____________ 来区分硬水和软水,生活中常用_________的方法来降低水的硬度。
|
|
| 22. | 详细信息 |
|
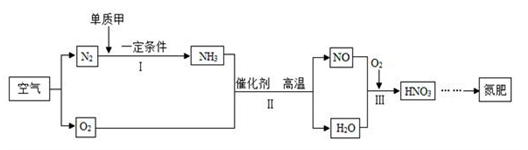
合理利用能源和保护环境是我们关注的问题,请回答: (1)下列保护空气措施合理的是______________(填序号)。 A. 工厂通过加高烟囱直接排放废气 B. 推广使用乙醇汽油代替普通汽油 C. 提倡步行、骑自行车等“低碳”出行方式 (2)利用空气制取氮肥的流程如图所示。
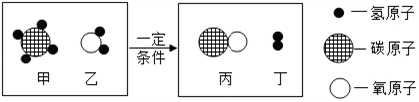
物质所含元素化合价发生变化的反应称为氧化还原反应。 反应Ⅰ--Ⅲ中属于氧化还原反应的共_____ 个。 (3)煤作为燃料给我们带来了益处,但对环境也造成了不良影响。 ①下列关于酸雨的叙述正确的是______(填序号)。 A.腐蚀大理石 B.是由二氧化碳引起的 C.酸化土地 ②为减少污染、治理“雾霾”,新开发一种新能源页岩气,它是指蕴藏于页岩系统中的天然气。工业上用其制备水煤气,其反应的微观示意图如下图所示
写出该反应的化学方程式___________________________________________。但页岩气中常含有剧毒的H2S气体,开采时若发生泄漏,可以喷射氢氧化钠溶液与H2S形成的溶液发生反应,该反应的化学方程式为___________________________________。
|
|
| 23. | 详细信息 |
|
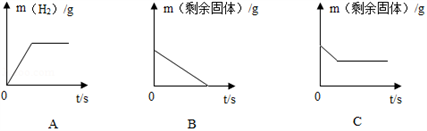
金属材料与人类的生产和生活密切相关。请回答: (1)下列用品中,主要利用金属导电性的是_____(填序号)。 A.铂金饰品 B.铁锅 C.铝导线 (2)生活中的铝合金比纯铝的硬度_____(填“大”或“小”);铁制品锈蚀的过程,实际上是铁跟空气中的氧气和______________发生化学反应的过程。 (3)在氯化铜和氯化亚铁的混合溶液中加入一定质量的镁粉,充分反应后过滤,得到滤渣和滤液。 ①滤液中一定含有的溶质是_____(填化学式)。 ②向滤渣中滴加稀盐酸,有气泡产生,则滤渣中一定含有的物质是_____(填化学式)。 (4)将足量的稀盐酸加入一定量的铁、铜混合物中,下图是实验过程生成气体或剩余固体的质量随反应时间的变化关系,其中表示正确的是_____(填序号)。
(5)某同学将铁片放入CuSO4溶液中,发现铁片表面有红色物质析出,同时还有少量无色无味气泡产生。对于产生气泡的“异常现象”,下列猜想不合理的是____(填序号)。 A.产生的气体可能是H2 B.产生的气体可能是CO2 C.CuSO4溶液中可能含有少量的某种酸 D.CuSO4溶液的pH 小于7
|
|
| 24. | 详细信息 |
|
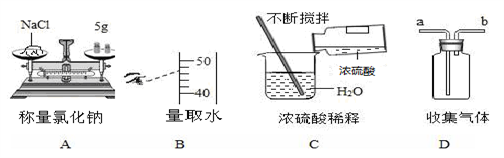
根据如图所示的实验操作回答问题。
(1)图A、B是某同学配制50g质量分数为6%的氯化钠溶液时,在称量和量取两个操作步骤中出现的情况。 ①如图A所示:在称量氯化钠的操作过程中,发现指针偏右,则继续进行的操作是______,至天平平衡。 ②如图B所示,量取水时,仰视读数,所得溶液中溶质的质量分数会________(填“偏大”、“偏小”或“不变”)。 (2)实验室配制50g质量分数为6%的氯化钠溶液时,用到的玻璃仪器除试剂瓶、量筒、烧杯外,还需要_________________________________________。 (3)上图C操作中如果将浓硫酸和水的顺序颠倒,将会出现的后果_________。 (4)若用D收集下列气体,从a通入气体可以收集_____________(填序号)。 A. NH3 B. CO2 C.CH4 D.SO2
|
|
| 25. | 详细信息 |
|
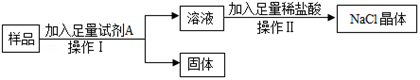
海洋是巨大的资源宝库,蕴藏着非常丰富的海洋资源,开发前景远大。 (1)海盐是人类最早从海洋中获取的矿物质之一。从海水中提取食盐的方法主要为盐田法,所得到的母液是当时温度下氯化钠的____________溶液(填“饱和”或“不饱和”)。 (2)某氯化钠溶液中含有较多CaCl2,按下图方案提纯得到氯化钠晶体。
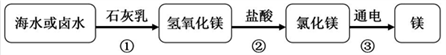
①试剂A的化学式为______________________。 ②加入足量稀盐酸的目的是__________________________________。 ③操作Ⅰ、Ⅱ的名称分别是__________________、_________________________。 ④操作Ⅰ、Ⅱ中都要用到一种玻璃仪器,该仪器在操作Ⅱ中的作用是_________________。 (3)金属镁广泛应用于生活、生产和国防工业,从卤水中提取镁的过程如图所示。
在上述转化过程中,所发生的化学反应属于分解反应的是___________(填反应序号)。
|
|
| 26. | 详细信息 | ||||||
|
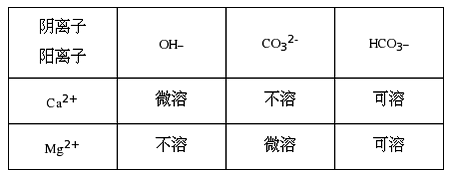
化学小组对热水壶底部水垢的主要成分进行了如下探究,请回答问题。 【查阅资料】天然水中含有Ca2+、Mg2+、HCO3-等离子,在加热条件下,这些离子趋于生成溶解度更小的物质——水垢(主要成分为碳酸盐和碱)。有关物质的溶解性见下表。
【提出猜想】水垢的主要成分中一定含有______和_________(填化学式),可能含有Ca(OH)2和MgCO3。 【设计方案】 实验1:确定水垢中是否含Ca(OH)2和CaCO3
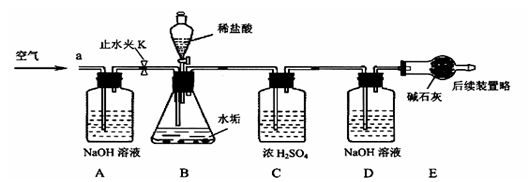
实验2:确定水垢中是否含MgCO3 利用下列实验装置,完成实验2探究。其主要实验步骤如下:
称量D、E装置总质量为600.00g,按上图组装后,将2.50g水垢试样放入锥形瓶中,加入足量稀盐酸溶液,待锥形瓶中不再产生气泡时,打开止水夹K,从导管a处缓缓鼓入空气,一段时间后称量装置D、E的总质量为601.25g(碱石灰主要成分为CaO和NaOH,不考虑装置内空气对实验的影响)。 【实验讨论】(1)加入样品前应_______________________________。 (2)反应结束后打开止水夹K,缓缓鼓入空气的目的是_______________________,装置A的作用是________________________________ 。 (3)A、B装置之间_____设置干燥装置(填:“要”或“不要”),理由是_____________。 (4)装置B中生成CO2的质量为______g。通过计算说明水垢中_____含MgCO3(填字母)。 A. 一定 B. 一定不 C. 可能 D. 无法确定 实验3:确定水垢中是否含有Mg(OH)2 (5)另取质量为2.50g的水垢,加入3.65%的稀盐酸与之反应,测得消耗稀盐酸w g。结合以上实验结论,判断w的值满足________________条件时,水垢中一定含有Mg(OH)2。
|
|||||||
| 27. | 详细信息 | ||||||||||||||||||||
|
某同学为探究铜铁合金中铁的质量分数,先后进行了四次实验,实验数据如下:
根据该同学的实验,回答以下问题: (1)上表第四次实验中合金里的铁恰好与稀硫酸完全反应,则其中m=_____, n=______。 (2)该铜铁合金中铁的质量分数是多少?
|
|||||||||||||||||||||

 B.
B. 
 D.
D.