江西省赣州市十六县(市)十九校2021-2022学年高一下学期期中联考化学试题
江西省赣州市十六县(市)十九校2021-2022学年高一下学期期中联考化学试题
教材版本:化学
试卷分类:化学高一下学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高一下学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
在10 L密闭容器中,1 mol A和3 mol B在一定条件下反应:A(g)+xB(g)=2C(g),2 min后反应达到平衡时,测得混合气体共3.4 mol,生成0.4 mol C,则下列计算结果正确的是( )
A . 平衡时,容器内的压强是起始时的
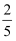 B . x值等于3
C . A的转化率为20%
D . B的平均反应速率为0.4 mol·L-1·min-l
B . x值等于3
C . A的转化率为20%
D . B的平均反应速率为0.4 mol·L-1·min-l
|
|
| 2. 单选题 | |
|
《厉害了,我的国》展示了中国探索太空。开发深海,建设世界第一流的高铁、桥梁、码头。5G技术联通世界等取得的举世瞩目的成就。它们与化学有着密切联系。下列说法正确的是( )
A . 为打造生态文明建设,我国大力发展核电、光电、风电、水电,电能属于不可再生能源
B . “神舟十一号”宇宙飞船返回舱外表面使用的高温结构陶瓷的主要成分是硅酸盐
C . 我国提出网络强国战略,光缆线路总长超过三千万公里。光缆的主要成分是晶体硅
D . C919大型客机使用了大量先进复合材料、铝锂合金等,铝锂合金可减轻机身自重
|
|
| 3. 单选题 | |
|
用
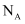 表示阿伏加德罗常数的值,下列说法正确的是( ) 表示阿伏加德罗常数的值,下列说法正确的是( )
A .
 的 的 溶液中的氮原子数为 溶液中的氮原子数为 B . 常温常压下,
B . 常温常压下, 和 和 的混合物共 的混合物共 , 所含氧原子数目一定为 , 所含氧原子数目一定为 C . 标准状况下
C . 标准状况下 与 与 充分反应后气体的分子数为 充分反应后气体的分子数为 D .
D .  与足量的 与足量的 充分反应,反应中转移的电子数为 充分反应,反应中转移的电子数为
|
|
| 4. 单选题 | |
|
一定温度下,将 2 mol SO2 和 1 mol O2 充入2L密闭容器中,在催化剂存在下进行下列反应: 2SO2+ O2
 2SO3 , 下列说法中正确的是( ) 2SO3 , 下列说法中正确的是( )
A . 达到反应限度时,生成2molSO3
B . 达到反应限度时SO2的消耗速率必定等于O2的生成速率
C . 达到反应限度时SO2、O2、SO3的分子数之比一定为2∶1∶2
D . SO2和SO3物质的量之和一定为 2mol
|
|
| 5. 单选题 | |
|
800℃时,A、B、C三种气体在密闭容器中反应时浓度的变化如图所示。则以下说法错误的是( )
A . 发生的反应可表示为
 B . 前
B . 前 , A的分解速率为 , A的分解速率为 C .
C .  时,A,B,C的浓度之比为2∶3∶1
D . 通过调控反应条件,可以提高该反应进行的程度 时,A,B,C的浓度之比为2∶3∶1
D . 通过调控反应条件,可以提高该反应进行的程度
|
|
| 6. 单选题 | |
|
推理是一种重要的能力,打开分液漏斗活塞,进行如图所示的探究实验,对实验现象的预测及分析错误的是( )
A . 锥形瓶中
 与70%硫酸发生氧化还原反应
B . 试管内 与70%硫酸发生氧化还原反应
B . 试管内 层溶液褪色,说明 层溶液褪色,说明 具有氧化性
C . 试管中的红色花瓣褪色,说明 具有氧化性
C . 试管中的红色花瓣褪色,说明 具有漂白性
D . 一段时间后试管内有白色沉淀,说明有 具有漂白性
D . 一段时间后试管内有白色沉淀,说明有 生成 生成
|
|
| 7. 单选题 | |
|
铁粉具有平肝镇心、消痈解毒之功效,主治惊痫、癫狂、脚气冲心、贫血等。某兴趣小组探究用氢气和碳酸亚铁制取铁粉并检验反应产物,实验装置如图。下列说法错误的是 ( )
A . 在锌粒中加入几粒硫酸铜晶体可能加快H2的生成
B . 装置②、③中的药品分别是无水硫酸铜、氯化钙
C . 装置①、④中药品为浓H2SO4
D . 加热装置Y前,应先让X反应一段时间,排除装置中的空气
|
|
| 8. 单选题 | |
|
电化学法处理
 是目前研究的热点。利用双氧水氧化吸收 是目前研究的热点。利用双氧水氧化吸收 可消除 可消除 污染,并制备硫酸。设计装置如图所示(已知电极为石墨电极只起导电作用,质子交换膜只允许 污染,并制备硫酸。设计装置如图所示(已知电极为石墨电极只起导电作用,质子交换膜只允许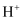 通过)。下列叙述中错误的是( ) 通过)。下列叙述中错误的是( )
A .
 通入的一极为电池负极
B . 导线上箭头方向表示电流方向
C . B池中的反应为 通入的一极为电池负极
B . 导线上箭头方向表示电流方向
C . B池中的反应为 D . 若
D . 若 (标准状况) (标准状况)  参与反应,则A池中增加 参与反应,则A池中增加
|
|
| 9. 单选题 | |
|
已知2Fe3++2I-→2Fe2++I2 , 为了探究FeCl3溶液和KI溶液的反应是否存在一定的限度,取5mL0.5mol•L-1KI溶液,向其中加主0.1mol•L-1的FeCl31mL,充分反应,下列实验操作能检验该反应是否存在限度的是( )
A . 再滴加AgNO3溶液,观察是否有黄色沉淀产生
B . 再加入CCl4振荡后,观察下层液体颜色是否变为紫红色
C . 再加入CCl4振荡后,取上层清液,滴加AgNO3溶液,观察是否有白色沉淀产生
D . 再加入CCl4振荡后,取上层清液,滴加KSCN溶液,观察溶液是否变成红色
|
|
| 10. 单选题 | |||||||||||||||||||||||||||
|
利用如图所示装置进行下列实验,能得出相应实验结论的是( )
A . A
B . B
C . C
D . D
|
|||||||||||||||||||||||||||
高中化学 试卷推荐
- 高中化学人教版(2019)必修第一册第二章实验活动配制一定物质的量浓度的溶液
- 2015-2016学年江苏省淮安市淮阴区高一下学期期中化学试卷2015-2016学年江苏省淮安市淮阴区高一下学期期中化学试卷
- 2015-2016学年福建省福州市五校联考高二下学期期中化学试卷
- 2016年高考理综真题试卷(化学部分)(新课标Ⅲ卷)
- 四川省雅安市2017-2018学年高二下学期化学期末考试试卷
- 人教版高中化学选修五 第三章第四节:有机合成
- 湖南省常德市2017-2018学年高考理综-化学一模考试试卷
- 2015-2016学年湖北省宜昌市部分示范高中高一上学期期末化学试卷
- 2015-2016学年四川省成都市彭州市五校联考高一下学期期中化学试卷
- 2016-2017学年福建省宁德市柘荣一中等五校联考高一上学期期中化学试卷
- 2014年海南省高考化学试卷
- 2019年高考化学真题分类汇编专题11:有机化学
最近更新








