广西梧州市2021年高考理综-化学3月模拟试卷
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
化学与生产、生活密切相关,下列叙述错误的是( )
A . 添加碱性蛋白酶能提高洗衣粉的去污能力,使用时水温越高洗涤效果越好
B . 84消毒液和医用酒精杀灭新冠肺炎病毒的原理不同
C . 用超临界液态CO2代替有机溶剂萃取大豆油,有利于环保
D . 侯氏制碱法利用了物质溶解度的差异
|
|
| 2. 单选题 | |
|
有机物W在工业上常用作溶剂和香料,其合成方法如图:
下列说法正确的是( )
A . M的一氯代物有3种
B . N、W组成上相差一个CH2原子团,所以互为同系物
C . M、N、W均能发生加成反应和取代反应
D .
 最多可与 最多可与  发生反应 发生反应
|
|
| 3. 单选题 | |
|
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A . 标准状况下,33.6L氟化氢中含有氟原子的数目为1.5NA
B . 常温常压下,7.0g乙烯与丙烯的混合物中含有氢原子的数目为NA
C . 50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA
D . 某密闭容器盛有0.1molN2和0.3molH2 , 在一定条件下充分反应,转移电子的数目为0.6NA
|
|
| 4. 单选题 | |
|
短周期主族元素W、X、Y、Z的原子序数依次增大,W的最高价氧化物固态时可用作人工降雨剂或用于冷藏食品,X、Y的最外层电子数之和与W的最外层电子数相等,W的简单氢化物与Z的单质混合光照可生成Z的氢化物和油状混合物。下列说法正确的是( )
A . 原子半径:W>X>Y>Z
B . X、Y的简单离子的电子层结构相同
C . W的简单氢化物的稳定性比Z的强
D . Z分别与W、X形成的化合物中所含化学键类型相同
|
|
| 5. 单选题 | |||||||||||||||||||||
|
下列实验现象和结论相对应且正确的是( )
A . A
B . B
C . C
D . D
|
|||||||||||||||||||||
| 6. 单选题 | |
|
焦亚硫酸钠(Na2S2O5)可用作食品加工的防腐剂,制备示意图如下。已知:2NaHSO3=Na2S2O5+H2O。下列说法错误的是( )
A . 采用的是阳离子交换膜
B . 阳极的电极反应式为2H2O-4e-= 4H+ + O2↑
C . 当阴极生成0.2 g气体时,a室溶液质量减少1.6 g
D . 电解后将b室溶液进行结晶、脱水,可得到Na2S2O5
|
|
| 7. 多选题 | |
|
下列指定反应的离子方程式书写正确的是( )
A . 四氧化三铁溶于足量稀硝酸:3Fe3O4+28H++
 =9Fe3++NO↑+14H2O
B . 工业上生产漂白粉的原理:Cl2+2OH-=Cl-+ClO-+H2O
C . 向硫酸铵溶液中滴入少量氢氧化钠溶液: =9Fe3++NO↑+14H2O
B . 工业上生产漂白粉的原理:Cl2+2OH-=Cl-+ClO-+H2O
C . 向硫酸铵溶液中滴入少量氢氧化钠溶液:  +OH-=NH3·H2O
D . 向酸性高锰酸钾溶液中滴入少量H2O2溶液:2 +OH-=NH3·H2O
D . 向酸性高锰酸钾溶液中滴入少量H2O2溶液:2  +6H++7H2O2=2Mn2++6O2↑+10H2O +6H++7H2O2=2Mn2++6O2↑+10H2O
|
|
| 8. 实验探究题 | |||||||||||||||||
|
无水四氯化锡(
 )用于制作FTO导电玻璃,FTO玻璃广泛用于液晶显示屏、光催化、薄膜太阳能电池基底等,可用下图装置制备四氯化锡。 )用于制作FTO导电玻璃,FTO玻璃广泛用于液晶显示屏、光催化、薄膜太阳能电池基底等,可用下图装置制备四氯化锡。
有关信息如下表:
|
|||||||||||||||||
| 9. 综合题 | |||||||||||||||||||||||||||||||
|
随着新能源汽车销量的猛增,动力电池退役高峰将至,磷酸铁锂(LFP)是目前使用最多的动力电池材料,因此回收磷酸铁锂具有重要意义。一种从废旧磷酸铁锂正极片( LiFePO4、导电石墨、铝箔)中回收锂的工艺流程如图:
已知:Li2CO3在水中的溶解度随温度升高而降低,但煮沸时发生水解。回答下列问题:
|
|||||||||||||||||||||||||||||||
| 10. 综合题 | |||||||||||||||||||
|
汽车尾气和燃煤尾气是造成雾霾的主要原因之一、
|
|||||||||||||||||||

 ,不含
,不含 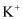
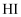 溶液加入
溶液加入  溶液中,充分反应后再加入
溶液中,充分反应后再加入  混合振荡,静置
混合振荡,静置



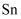
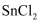

 、
、 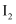 等氧化为
等氧化为  和
和 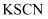 溶液的
溶液的  溶液 d.双氧水
溶液 d.双氧水 产品于锥形瓶中,用蒸馏水溶解,淀粉溶液做指示剂,用
产品于锥形瓶中,用蒸馏水溶解,淀粉溶液做指示剂,用 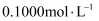 碘标准溶液滴定,滴入最后一滴,出现现象时达到滴定终点,此时消耗碘标准溶液
碘标准溶液滴定,滴入最后一滴,出现现象时达到滴定终点,此时消耗碘标准溶液  ,则产品中
,则产品中 
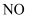 ,可减少氮氧化物的排放。
,可减少氮氧化物的排放。 

 还原为
还原为  的热化学方程式为。
的热化学方程式为。 。向恒温恒容密闭容器中充入
。向恒温恒容密闭容器中充入  ,用传感器测得的数据如下表所示:
,用传感器测得的数据如下表所示: 

 。
。 和氮的氧化物气体(
和氮的氧化物气体( 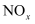 ),可得到
),可得到  、
、  、
、  、
、 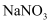 等溶液。(已知:常温下,
等溶液。(已知:常温下, 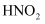 的电离常数为
的电离常数为  ,
, 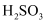 的电离常数为
的电离常数为  、
、  ,
,  )。
)。  )常见有
)常见有  、
、 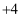 两种价态。
两种价态。  的溶液吸收,生成
的溶液吸收,生成  ,
,  (二者物质的量之比为1∶1)。可采用电解法将上述吸收液中的
(二者物质的量之比为1∶1)。可采用电解法将上述吸收液中的 



