天津市西青区2021--2022学年高三上学期期末考试化学试题
天津市西青区2021--2022学年高三上学期期末考试化学试题
教材版本:化学
试卷分类:化学高三上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高三上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图1所示。下列说法正确的是( )
A . 元素X与元素Z的最高正化合价之和的数值等于8
B . 原子半径的大小顺序为:rX>rY>:rZ>rW>rQ
C . 离子Y2-和Z 3+的核外电子数和电子层数都不相同
D . 元素W的最高价氧化物对应的水化物的酸性比Q的强
|
|
| 2. 单选题 | |
 为正盐,能将溶液中的 为正盐,能将溶液中的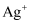 还原为 还原为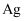 , 可用于化学镀银。利用 , 可用于化学镀银。利用 进行化学镀银反应中,若氧化剂与还原剂的物质的量之比为 进行化学镀银反应中,若氧化剂与还原剂的物质的量之比为 。下列说法正确的是( ) 。下列说法正确的是( )
A . 上述反应中,氧化产物是
 B .
B .  是三元酸,与 是三元酸,与 反应可生成三种盐
C . 反应可生成三种盐
C .  中含有离子键、极性共价键和非极性共价键
D . 该反应的离子方程式为 中含有离子键、极性共价键和非极性共价键
D . 该反应的离子方程式为
|
|
| 3. 单选题 | |
|
下列事实不能用有机物分子内基团间的相互影响解释的是( )
A . 苯酚能跟浓溴水反应而苯不能
B . 乙炔能跟溴水反应而乙烷不能
C . 苯酚显弱酸性而乙醇不显弱酸性
D . 甲苯易被酸性高锰酸钾氧化而甲烷不能
|
|
| 4. 单选题 | |
|
在元素周期表中,有一种元素
 , 它作为玻璃添加剂,能吸收紫外线与红外线,还可降低车内温度,从而节约空调用电,现已被大量应用于汽车玻璃行业。下列对其元素说法正确的是( ) , 它作为玻璃添加剂,能吸收紫外线与红外线,还可降低车内温度,从而节约空调用电,现已被大量应用于汽车玻璃行业。下列对其元素说法正确的是( )
A . 所含的质子数为140
B . 所含的质量数是58
C . 所含的中子数是82
D . 核外电子数是140
|
|
| 5. 单选题 | |
|
某学习小组用“间接碘量法”测定某CuCl2晶体试样的纯度,试样不含其他能与I-发生反应的氧化性杂质,已知:2Cu2++4I-=2CuI↓+I2 , I2+2S2O
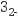 =S4O =S4O +2I-。取m g试样溶于水,加入过量KI固体,充分反应,用0.100 0 mol·L-1 Na2S2O3标准溶液滴定,部分实验仪器和读数如图所示。下列说法正确的是( ) +2I-。取m g试样溶于水,加入过量KI固体,充分反应,用0.100 0 mol·L-1 Na2S2O3标准溶液滴定,部分实验仪器和读数如图所示。下列说法正确的是( )
A . 试样在容量瓶中溶解,滴定管选乙
B . 选用淀粉作指示剂,当甲中溶液由无色变为蓝色时,即达到滴定终点
C . 丁图中,滴定前滴定管的读数为a-1.00 mL
D . 对装有待测液的滴定管读数时,滴定前后读数方式如丁图所示,则测得的结果偏大
|
|
| 6. 单选题 | |
|
O2F2可以发生反应:H2S+4O2F2=SF6+2HF+4O2 , 下列说法正确的是( )
A . 若生成2.24 L HF,则转移0.4 mol电子
B . HF是氧化产物
C . O2F2既是氧化剂又是还原剂
D . 还原剂与氧化剂的物质的量之比为1:4
|
|
| 7. 单选题 | |
|
H3PO4的电离是分步进行的,常温下
 , ,  , ,  。下列说法正确的是( ) 。下列说法正确的是( )
A . 浓度均为0.1 mol/L的NaOH溶液和H3PO4溶液按照体积比2∶1混合,混合液的pH<7
B . Na2HPO4溶液中,
 C . 向0.1 mol/L的H3PO4溶液中通入HCl气体(忽略溶液体积的变化),溶液pH=1时,溶液中大约有7.1%的H3PO4电离
D . 在H3PO4溶液中加入NaOH溶液,随着NaOH的加入,溶液的pH增大,当溶液的pH=11时,
C . 向0.1 mol/L的H3PO4溶液中通入HCl气体(忽略溶液体积的变化),溶液pH=1时,溶液中大约有7.1%的H3PO4电离
D . 在H3PO4溶液中加入NaOH溶液,随着NaOH的加入,溶液的pH增大,当溶液的pH=11时,
|
|
| 8. 单选题 | |
|
铬(Ⅵ) 的化合物有较大毒性,如不回收利用,会对环境造成污染。某混合浆液含Al(OH)3、MnO2和少量Na2CrO4。某研究小组设计了如下电解分离装置,可以使浆液较完全地分离成固体混合物和含铬元素溶液,并回收利用。下列说法不正确的是( )
A . 通电后CrO42-将通过阴离子膜进入阳极室
B . 阴极室最终只能得到Na2SO4和H2
C . 阳极的电极反应式为:4OH--4e-=O2↑+2H2O
D . 分离后所得含铬元素的粒子有CrO42-和Cr2O72-
|
|
| 9. 单选题 | |
|
下列化学用语的书写正确的是( )
A . O2-的离子结构示意图:
 B . 质子数为27、中子数为60的Co原子:
B . 质子数为27、中子数为60的Co原子: Co
C . H2O的电子式: Co
C . H2O的电子式: D . 用电子式表示氢溴酸的形成过程为:
D . 用电子式表示氢溴酸的形成过程为:
|
|
| 10. 单选题 | |
|
科学家设想用结构相似的C60与Si60合成一种类似工艺品“套球”(如图示)的球型碳硅化合物Si60C60 , 外层球壳原子与里层球壳原子通过共价键结合。下列说法一定正确的是( )
A . 该物质与碳化硅(SiC)互为同素异形体
B . 该物质形成的晶体是分子晶体
C . 该物质结构中,外层球壳为C60 , 内层球壳为Si60
D . 该物质的熔点高、硬度大
|
|
高中化学 试卷推荐
- 山东省潍坊市2019-2020学年高一下学期化学期末考试试卷
- 山东省烟台市2019-2020学年高二下学期化学期末考试试卷
- 2015-2016学年山东省德州市跃华学校高一下学期期中化学试卷
- 2015-2016学年山东省淄博市淄川一中高二下学期第一次月考化学试卷
- 人教版化学高二选修1第二章第一节合理选择饮食同步练习
- 黑龙江省大庆市三校联考2018-2019学年高二下学期化学期末考试试卷
- 上海市普陀区2016-2017学年高考化学二模考试试卷
- 2015-2016学年广西柳州市铁路一中高一上学期段考化学试卷
- 2015-2016学年山东省临沂市蒙阴一中高二下学期期中化学试卷
- 江苏省盐城市2018-2019学年高一下学期化学期末考试试卷
- 浙江省百校联盟2019-2020学年高三上学期化学10月月考试卷
- 高中化学人教版必修1 第一章第一节 化学实验基本方法
最近更新







