吉林省松原市六校2021-2022学年度高一上学期月考联考试卷化学试卷
吉林省松原市六校2021-2022学年度高一上学期月考联考试卷化学试卷
教材版本:化学
试卷分类:化学高一上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高一上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A . 1 mol Na2O2固体中离子总数为4NA
B . 标准状况下,22.4 L水中所含分子数为NA
C . 常温常压下,16 g氧气中所含原子数为NA
D . 等物质的量的N2和CO所含有原子数均为2NA
|
|
| 2. 单选题 | |
|
国防科大航天科学与工程学院新型陶瓷纤维及其复合材料重点实验室成功研制出一种具有超强吸附能力的新型超轻纳米材料(基本微粒直径为1~100nm)。这种材料结构上由一维氮化硼纳米管和二维氮化硼纳米晶片复合而成,整个材料内部充满气孔。这种材料耐高温,且用它吸附完有机物后,可以通过点燃的方式实现重复使用。下列关于该材料的说法不正确的是( )
A . 将该材料分散到液体分散剂中,所得混合物可能具有丁达尔效应
B . 该材料的基本微粒不能透过滤纸
C . 该材料在高温下,还可以保持结构完整,可正常使用
D . 该材料比表面积大,吸附能力强
|
|
| 3. 单选题 | |
|
下列叙述正确的是( )
A . Cu易导电,属于电解质
B . SO2溶于水能导电,所以SO2是电解质
C . 固体NaCl不导电,但NaCl是电解质
D . BaSO4的水溶液不导电,所以BaSO4是非电解质
|
|
| 4. 单选题 | |
|
25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
A . pH=1的溶液中:Na+、K+、
|
|
| 5. 单选题 | |
|
下列离子方程式书写正确的是( )
A . MgCl2溶液与氨水反应:Mg2++2OH- = Mg(OH)2↓
B . 氯气跟水反应:Cl2 + H2O = 2H+ + Cl- + ClO-
C . 大理石与醋酸反应:CaCO3 + 2CH3COOH = Ca2+ + 2CH3COO- + CO2↑ + H2O
D . 硫酸铜溶液跟氢氧化钡溶液反应:Ba2+ + SO
|
|
| 6. 单选题 | |
|
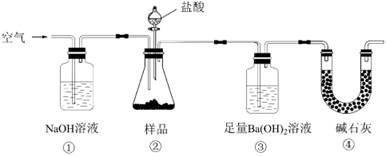
实验室按如下装置测定纯碱(含少量NaCl)的纯度。下列说法不正确的是( )
A . 必须在装置②、③间添加盛有饱和NaHCO3溶液的洗气瓶
B . 装置①、④的作用是防止空气中的CO2进入装置③
C . 滴入盐酸前,应将装置中含有CO2的空气排尽
D . 反应结束时,应再通入空气将装置②中CO2转移到装置③中
|
|
| 7. 单选题 | |
|
下列叙述中正确的是( )
①标准状况下,6.02×1023个分子所占体积约是22.4L ②标准状况下,1gH2和14gN2的体积相同 ③28gCO的体积为22.4L ④两种物质的物质的量相同时,它们在标准状况下的体积也相同 ⑤同温同体积时,气体的物质的量越大,则压强越大 ⑥同温同压下,气体的密度与气体的相对分子质量成正比 ⑦标准状况下,1LHCl和1LH2O的物质的量相同
A . ①④⑤
B . ①⑤⑥
C . ②⑥⑦
D . ②⑤⑥
|
|
| 8. 单选题 | |
|
如图所示,
A . 浓
|
|
| 9. 单选题 | |
|
为预防“H1N1”甲型流感,可用“84”消毒液(NaClO溶液)消毒,下列说法中正确的是( )
A . “84”消毒液与“洁厕灵”(盐酸)共同使用,可达到既清洁又消毒的双重效果
B . 1 mol Cl2与足量NaOH溶液反应转移2 mol电子
C . “84”消毒液可以敞口保存
D . “84”消毒液是以NaClO为有效成分的消毒液
|
|
| 10. 单选题 | |
|
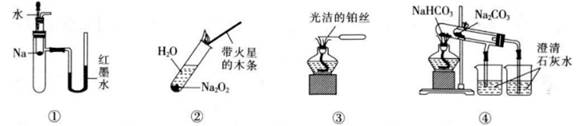
下列实验装置不能达到实验目的的是( )
A . 利用装置①验证Na和水反应为放热反应
B . 利用装置②检验Na2O2与H2O反应有O2生成
C . 利用装置③观察纯碱的焰色试验的现象
D . 利用装置④比较Na2CO3和NaHCO3的热稳定性
|
|
高中化学 试卷推荐
- 福建省龙岩市2022届高中毕业班第三次教学质量检测化学试题
- 重庆市九校联盟2021-2022学年高二上学期12月联考化学试题
- 天津市南开区2020-2021学年高三上学期化学期中考试试卷
- 河南省洛阳市2021年高考化学3月试卷
- 四川省绵阳市2022届高三第三次诊断性考试理综化学试题
- 陕西省汉中市镇巴县2021-2022学年高一下学期期中考试化学试题
- 辽宁省辽阳市2022届高三一模化学试题
- 广东省深圳市第七高级中学2020-2021学年高二上学期化学第一次月考试卷
- 广东省广州市荔湾区2020-2021学年高二上学期化学期末考试试卷
- 陕西省洛南中学2020-2021学年高三上学期化学第一次模拟考试
- 山西省怀仁市2021-2022学年期末调研高一上学期期末调研化学试题
- 安徽省江南十校2021年高考化学一模试卷
最近更新