化学选修4第三章 水溶液中的离子平衡
化学选修4第三章 水溶液中的离子平衡
教材版本:化学
试卷分类:化学高二上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高二上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
已知下面三个数据:7.2×10-4、4.6×10-4、4.9×10-10分别是三种酸的电离平衡常数,若已知这些酸可发生如下反应:①NaCN+HNO2=HCN+NaNO2 , ②NaCN+HF=HCN+NaF,③NaNO2+HF=HNO2+NaF。由此可判断下列叙述中,不正确的是( )
A . HF的电离平衡常数为7.2×10-4
B . HNO2的电离平衡常数为4.9×10-10
C . 根据①③两个反应即可知三种酸的相对强弱
D . HNO2的电离平衡常数比HCN大,比HF小
|
|
| 2. 单选题 | |
|
下表中物质的分类组合完全正确的是( )
A . A
B . B
C . C
D . D
|
|
| 3. 单选题 | |
|
下列溶液中,因为电离产生的离子发生水解而显酸性的是( )
A . NaHCO3
B . NaHSO3
C . CuSO4
D . Ca(NO3)2
|
|
| 4. 单选题 | |
|
在水溶液中下列电离方程式书写正确的是( )
A . Ca(OH)2
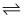 Ca2++2OH-
B . NaHCO3=Na++H++CO32-
C . H2CO3 Ca2++2OH-
B . NaHCO3=Na++H++CO32-
C . H2CO3 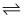 2H++CO32-
D . Na2SO4=2Na++SO42- 2H++CO32-
D . Na2SO4=2Na++SO42-
|
|
| 5. 单选题 | |
|
醋酸溶液中存在电离平衡:CH3COOH
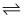 H++CH3COO- , 下列叙述不正确的是( ) H++CH3COO- , 下列叙述不正确的是( )
A . 升高温度,平衡正向移动,醋酸的电离常数Ka增大
B . 0.10 mol·L-1的CH3COOH溶液加水稀释,溶液中c(OH-)增大
C . CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动
D . 25 ℃时,欲使醋酸溶液的pH、电离常数Ka和电离程度都减小,可加入少量冰醋酸
|
|
| 6. 单选题 | |
|
已知氢氟酸在水溶液中建立如下电离平衡:HF
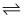 H++ F- , 若只改变一个条件,一定可以使c(HF)/c(H+)减小的是( ) H++ F- , 若只改变一个条件,一定可以使c(HF)/c(H+)减小的是( )
A . 通氯化氢气体
B . 加入少量氟化钾固体
C . 加入少量氢氧化钠固体
D . 通入少量氟化氢气体
|
|
| 7. 单选题 | |
|
已知室温时,0.1 mol·L-1某一元酸HA的电离平衡常数约为1×10-7 , 下列叙述错误的是( )
A . 该溶液的pH=4
B . 此溶液中,HA约有0.1%发生电离
C . 加水稀释,HA的电离平衡向右移动,HA的电离平衡常数增大
D . 由HA电离出的c(H+)约为水电离出的c(H+)的106倍
|
|
| 8. 单选题 | |
|
下列关于盐酸与醋酸两种稀溶液的说法正确的是( )
A . 相同浓度的两溶液中c(H+)相同
B . 100 mL 0.1 mol·L-1的两溶液能中和等物质的量的氢氧化钠
C . c(H+)=10-3mol·L-1的两溶液稀释100倍,c(H+)都为10-5mol·L-1
D . 两溶液中分别加入少量对应的钠盐,c(H+)均明显减小
|
|
| 9. 单选题 | |
|
准确移取20.00 mL某待测HCl溶液于锥形瓶中,用0.100 0 mol·L-1NaOH溶液滴定。下列说法正确的是( )
A . 滴定管用蒸馏水洗涤后,装入NaOH溶液进行滴定
B . 随着NaOH溶液滴入,锥形瓶中溶液pH由小变大
C . 用酚酞作指示剂,当锥形瓶中溶液由红色变无色时停止滴定
D . 滴定达终点时,发现滴定管尖嘴部分有悬滴,则测定结果偏小
|
|
| 10. 单选题 | |
|
今有室温下四种溶液,下列有关叙述不正确的是( )
A . ③和④中分别加入适量的醋酸钠晶体后,两溶液的pH均增大
B . ②和③两溶液等体积混合,所得溶液中c(H+)>c(OH-)
C . 分别加水稀释10倍,四种溶液的pH:①>②>④>③
D . V1L ④与V2L ①溶液混合后,若混合后溶液pH=7,则V1<V2
|
|
高中化学 试卷推荐
- 广西三新学术联盟2021-2022学年高一上学期期末联考化学试题
- 江西省名校2021-2022学年高二上学期化学第一次月考试卷
- 河北省2021-2022学年高三上学期化学开学考试试卷
- 云南省昆明市嵩明县2021-2022学年高二下学期期中考试化学试题
- 山东省滨州市无棣县2020-2021学年高二下学期化学期中考试试卷
- 四川省南充市2020-2021学年高二上期期末考试化学试题
- 安徽省皖西南联盟2020-2021学年高一上学期期末考试化学试题
- 浙江省绍兴市2021-2022学年高一上学期期末调测化学试题
- 浙江省嘉兴市南湖片区2021-2022学年高一上学期期中检测化学试题
- 山西省晋城市高平市2020-2021学年高一上学期化学期中考试试卷
- 浙江省绍兴市2022届高三选考科目适应性考试(二模)化学试题
- 浙江省温州市环大罗山联盟2021-2022学年高一下学期期中联考化学试题
最近更新





