2018-2019学年人教版(五·四学制)化学九年级全一册第三单元课题2 酸和碱的中和反应 同步训练
2018-2019学年人教版(五·四学制)化学九年级全一册第三单元课题2 酸和碱的中和反应 同步训练
教材版本:化学
试卷分类:化学九年级上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学九年级上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 填空题 | |
|
某试剂瓶上的标签已破损,残余部分如图.
①请猜测瓶中的试剂可能是. ②取瓶中的试剂少许溶于水,发现放出大量的热,如何用pH试纸测所得溶液的pH值(写出具体操作方法). ③用该稀溶液与氧化铜反应的方程式是. ④若少量该试剂沾到皮肤上,应迅速用较多水冲洗,再涂上3%﹣5%溶液(填“碳酸氢钠”或“氢氧化钠”),最后再用清水清洗. |
|
| 2. 综合题 | |
|
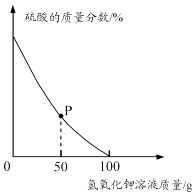
实验室常会产生含硫酸的废水,需经处理至中性.某兴趣小组同学配制一定质量分数的氢氧化钾溶液来处理酸性废水.
|
|
| 3. 单选题 | |
|
学会用化学解决实际问题是学习化学的一项重要任务.下列方案合理的是( )
A . 通过点燃的方法除去CO2中的CO
B . 加入过量的NaOH处理硫酸厂的废水
C . 加入过量的Ca(OH)2除去CaCl2中的HCl
D . 用水鉴别生石灰和熟石灰
|
|
| 4. 单选题 | |
|
推理是化学学习中常用的思维方法,下列推理正确的是( )
A . 人的血液呈碱性,则人的体液都呈碱性
B . NaCl溶液能够导电,则所有液体都能导电
C . KNO3溶液无色透明,则无色透明的液体都是溶液
D . 酸性溶液能使石蕊变红,能使石蕊变红的溶液都是酸性溶液
|
|
| 5. 填空题 | |
|
实验室有A、B 两种溶液,A 能使紫色石蕊溶液变红色,B能使无色酚酞溶液变红色,则A、B两种溶液的pH大小关系是AB (填“大于”或“小于”),显酸性的是溶液,该溶液是酸(填一定、不一定 ).要测定A、B 溶液的pH,其做法是。
|
|
| 6. 单选题 | |
|
向某稀盐酸中逐渐加入试剂X后溶液的pH变化如图。试剂X可能是下列物质中的( )
A . H2O
B . H2SO4
C . NaOH
D . CaCO3
|
|
| 7. 单选题 | |
|
下列说法正确的是( )
A . 除去二氧化碳中混有的氯化氢气体,可通过氢氧化钠溶液洗气
B . 测定溶液的pH时,需预先用蒸馏水将pH试纸润湿
C . 比较铁、铜的活动性强弱,可分别将这两种金属投入稀盐酸中观察现象
D . 若厨房天然气泄漏,应立即打开脱排油烟机进行排气
|
|
| 8. 综合题 | |
|
化学基础与常识
|
|
| 9. 单选题 | |
|
下列图像能正确反映其对应关系的是( )
A . ①表示向NaOH溶液中不断加水稀释
B . ②表示水电解生成氢气与氧气的质量关系
C . ③表示用等质量、等质量分数的过氧化氢溶液制取氧气
D . ④表示分别向等质量、等质量分数的稀硫酸中加入足量的镁、铝
|
|
| 10. 综合题 | |
|
铝是地壳中含量最多的金属元素,铝的化合物种类繁多,氧化铝的熔点(2050℃)高于铝的熔点(660℃)。硬铝(含铝、铜、镁、硅)是用途广发的铝合金。结合课本知识回答下列问题。
|
|
初中化学 试卷推荐
- 广东省广州市从化区2021-2022学年九年级上学期期末化学试题
- 陕西省咸阳市秦都区电建学校2021-2022学年九年级上学期化学第一次月考试卷
- 山东省烟台市龙口市2021-2022学年九年级上学期期中化学试题
- 吉林省通化市集安市2020-2021学年九年级上学期化学期末考试试卷
- 2021年广西南宁市武鸣区中考一模化学试题
- 广东省梅州市梅县区2020-2021学年九年级上学期化学期中考试试卷
- 河北省秦皇岛市海港区2021年中考一模化学试题
- 河南省焦作市沁阳市2020-2021学年九年级下学期化学第二次月考试卷
- 河北省承德市2021年中考化学一模试卷
- 山东省济宁市嘉祥县2022年中考一模化学试题
- 四川省凉山州2021年中考化学试卷
- 北京市东城区2020-2021学年九年级上学期化学期末考试试卷
最近更新