高中化学人教版(2019)选择性必修1第一章第一节反应热
高中化学人教版(2019)选择性必修1第一章第一节反应热
教材版本:化学
试卷分类:化学高二上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高二上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
丙烷的一溴代反应产物有两种:
 和 和 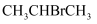 ,部分反应过程的能量变化如图所示( ,部分反应过程的能量变化如图所示( 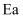 表示活化能)。下列叙述错误的是( ) 表示活化能)。下列叙述错误的是( )
A .
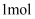 丙烷中有 丙烷中有 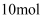 共价键
B . 共价键
B .  与 与  的反应涉及极性键和非极性键的断裂
C . 的反应涉及极性键和非极性键的断裂
C .  D . 比较
D . 比较 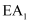 和 和  推测生成速率: 推测生成速率: 
|
|
| 2. 填空题 | |
|
化合物AX3和单质X2在一定条件下反应可生成化合物AX5。已知AX3的熔点和沸点分别为-93.6 ℃和76 ℃,AX5的熔点为167 ℃。室温时AX3与气体X2反应生成1 mol AX5 , 放出热量123.8 kJ。该反应的热化学方程式为。
|
|
| 3. 多选题 | |
|
下列关于热化学反应的描述中正确的是( )
A . HCl和NaOH反应的中和热△H=-57.3 kJ/mol
B . 甲烷的标准燃烧热△H=- 890.3 kJ/mol,则CH4(g) +2O2(g) =CO2(g)+2H2O(g) △H<-890.3 kJ/mol
C . 500℃、30 MPa下,N2(g)+3H2(g)
 2NH3(g) △H = -92.4kJ/mo1, 将1.5 mol H2和过量的N2在此条件下充分反应,放出热量46.2 kJ
D . CO(g)的燃烧热是283.0 kJ/mol,则2CO2(g)=2CO(g)+O2(g)的△H=+566.0 kJ/mol 2NH3(g) △H = -92.4kJ/mo1, 将1.5 mol H2和过量的N2在此条件下充分反应,放出热量46.2 kJ
D . CO(g)的燃烧热是283.0 kJ/mol,则2CO2(g)=2CO(g)+O2(g)的△H=+566.0 kJ/mol
|
|
| 4. 单选题 | |
|
某温度下,在容积为2 L的密闭容器中进行如下反应:N2(g)+3H2(g)
 2NH3(g) △H=-92.60 kJ/mol。图1表示N2的物质的量随时间的变化曲线,图2表示其他条件不变的情况下,改变起始物H2的物质的量对反应平衡的影响.下列说法正确的是( ) 2NH3(g) △H=-92.60 kJ/mol。图1表示N2的物质的量随时间的变化曲线,图2表示其他条件不变的情况下,改变起始物H2的物质的量对反应平衡的影响.下列说法正确的是( )
A . 加入适当催化剂后,该反应的△H<-92.60 kJ/mol
B . 11 min时其他条件不变压缩容器体积,N2物质的量变化曲线为c
C .
 内,该反应的平均反应速率v(H2)=0.045 mol/(L·min)
D . 在A,B,C三点所表示的平衡中,B点表示的N2的转化率最高 内,该反应的平均反应速率v(H2)=0.045 mol/(L·min)
D . 在A,B,C三点所表示的平衡中,B点表示的N2的转化率最高
|
|
| 5. 单选题 | |
|
我国科学家使用双功能催化剂(能吸附不同粒子)催化水煤气变换反应:CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH<0,在低温下获得高转化率与高反应速率。反应过程示意图如下: CO2(g)+H2(g) ΔH<0,在低温下获得高转化率与高反应速率。反应过程示意图如下: 下列说法正确的是( )
A . 过程Ⅰ、过程Ⅱ均为放热过程
B . 使用催化剂降低了水煤气变换反应的ΔH
C . 该催化过程中:有极性键的断裂,极性键和非极性键的形成
D . 图示显示:起始时的2个H2O在反应过程中并未都参与了反应
|
|
| 6. 实验探究题 | |||||||||||||||||||||||||||||
|
中和热的测定实验中取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:
|
|||||||||||||||||||||||||||||
| 7. 多选题 | |
|
在一定温度下,H2(g)+I2(g)
 2HI(g)反应达到了化学平衡,其反应过程对应的能量变化如图所示。下列说法正确的是( ) 2HI(g)反应达到了化学平衡,其反应过程对应的能量变化如图所示。下列说法正确的是( )
A . 该反应为放热反应
B . 该反应的△H=Ea'-Ea
C . 该反应中加入催化剂,可增大反应速率,同时改变焓变
D . 温度升高,单位体积的活化分子百分数增加,反应速率加快,且平衡逆向移动
|
|
| 8. 实验探究题 | |
|
用50mL 0.50mol/L盐酸与50mL 0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
|
|
| 9. 填空题 | |
|
化学反应过程中发生物质变化的同时,常常伴有能量的变化。这种能量的变化常以热量的形式表现出来,叫做反应热。由于反应的情况不同,反应热可以分为许多种,如燃烧热和中和热等。 下列△H 表示物质燃烧热的是(填字母编号)。
A. 2H2(g)+O2(g)═2H2O(l)△H1 B. C(s)+  O2(g)═CO(g)△H2 O2(g)═CO(g)△H2C. 2H2(g)+O2(g)═2H2O(l)△H1 D. C(s)+  O2(g)═CO(g)△H2 O2(g)═CO(g)△H2E. C6H12O6(s)+6O2(g)═6CO2(g)+6H2O(l)△H5 F. NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H6 G. CH3COO(aq)+NaOH(aq)═CH3COONa(aq)+H2O(l)△H7 |
|
| 10. 填空题 | |
|
中学化学实验中的中和热的测定所需的玻璃仪器除了大、小烧杯外还有。在大、小烧杯间填满碎泡沫(或纸条)的作用是。结合日常生活实际,该实验改在中进行效果会更好。
|
|
高中化学 试卷推荐
- 2015-2016学年江苏省南通市如皋市高一下学期期中化学试卷
- 人教版高中化学选修五 第一章第三节:有机化合物的命名
- 2016-2017学年四川省绵阳市丰谷中学高二上学期开学化学试卷
- 2019年初中化学中考难点专练 16 无机化工流程
- 福建省三明市2019-2020学年高一下学期化学期末考试试卷
- 2019年高考化学真题分类汇编专题07:化学平衡
- 江苏省南京师范大学附属中学2020年高考化学6月模拟试卷
- 浙江省嘉兴市2019-2020学年高二下学期化学期末考试试卷
- 北京市朝阳区2017-2018学年高一上学期化学期末考试试卷
- 2016年江西省上饶市余干县高考化学四模试卷
- 江苏省泰州市2020年高考化学二模试卷
- 备考2019年高考化学二轮专题 07 电化学及其应用
最近更新