吉林省吉林市蛟河市第一中学2019-2020学年高二上学期化学期中考试试卷
吉林省吉林市蛟河市第一中学2019-2020学年高二上学期化学期中考试试卷
教材版本:化学
试卷分类:化学高二上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高二上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
常温下,将CO2通入2LpH=12的KOH溶液中,溶液中水电离出的OHˉ离子浓度(c)与通入的CO2的体积(V)的关系如图所示.下列叙述错误的是( )
A . a点溶液中:水电离出的c(H+)=1×10-12 mol/L
B . b点溶液中:c(H+)=1×10-7mol/L
C . c点溶液中:c(K+)=2[c(CO32-)+c(HCO3ˉ)+c(H2CO3)]
D . d点溶液中:c(K+)=2c(CO32-)+c(HCO3ˉ)
|
|
| 2. 单选题 | |
|
我国科学家研发了一种室温下“可呼吸”的Na-CO2二次电池,将NaClO4溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO2+4Na
 2Na2CO3+C,下列说法错误的是() 2Na2CO3+C,下列说法错误的是()

A . 放电时,ClO4-向负极移动
B . 充电时释放CO2 , 放电时吸收CO2
C . 放电时,正极反应为:3CO2+4e-=2CO32-+C
D . 充电时,正极反应为:Na+ + e- =Na
|
|
| 3. 单选题 | |
|
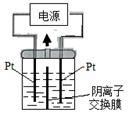
电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开。在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。
已知:3I2+6OH-=IO3-+5I-+3H2O 下列说法错误的是( )
A . 右侧发生的电极方程式:2H2O+2e-=H2↑+2OH-
B . 电解结束时,右侧溶液中含有IO3-
C . 电解槽内发生反应的总化学方程式KI+3H2O=KIO3+3H2↑
D . 如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学方程式不变
|
|
| 4. 单选题 | |
|
甲、乙两杯醋酸稀溶液,甲的pH=a,乙的pH=a+1,对下列叙述的判断正确的是( )
A . 甲中水电离出来的H+的物质的量浓度是乙中水电离出来H+的物质的量浓度的10倍
B . 中和等物质的量的NaOH溶液需甲、乙两杯醋酸溶液的体积,10V(甲)>V(乙)
C . 物质的量浓度c(甲)>10c(乙)
D . 甲中的c(OH-)为乙中的c(OH-)的10倍
|
|
| 5. 单选题 | |
|
用碱性氢氧燃料电池为电源进行电解的实验装置示意图如图所示。下列说法中正确的是( )
A . 燃料电池工作时负极反应为:H2=2H++2e-
B . 若要实现铁上镀铜,则a极是铁,b极是铜
C . 若要实现电解精炼粗铜,则a极发生氧化反应,b极上有铜析出
D . a、b两极均是石墨时,在相同条件下,当电池中消耗H222.4L(标准状况)时,a极析出铜64g
|
|
| 6. 单选题 | |
|
下列指定化学用语正确的是( )
A . NaHCO3水解的离子方程式:HCO3-+H2O=CO32-+H3O+
B . Ba(OH)2的电离方程式:Ba(OH)2
|
|
| 7. 单选题 | |||||||||
|
下表是几种弱酸常温下的电离平衡常数:
则下列说法中错误的是( )
A . 碳酸的酸性强于氢硫酸
B . 多元弱酸的酸性主要由第一步电离决定
C . 常温下,加水稀释醋酸,
 增大
D . 向弱酸溶液中加少量NaOH溶液,电离常数不变 增大
D . 向弱酸溶液中加少量NaOH溶液,电离常数不变
|
|||||||||
| 8. 单选题 | |
|
用标准浓度氢氧化钠的溶液来滴定未知浓度的盐酸,下列操作中会使盐酸测定的浓度偏大的是( )
①碱式滴定管用蒸馏水洗净后未用标准溶液润洗 ②锥形瓶中盛有少量蒸馏水,再加待测液 ③酸式滴定用蒸馏水洗净后,未用盐酸润洗 ④滴定前碱式滴定管尖端气泡未排除,滴定后气泡消失 ⑤滴定后观察碱式滴定管读数时,俯视刻度线
A . ①④
B . ①③
C . ②③
D . ④⑤
|
|
| 9. 单选题 | |
|
下列说法正确的是( )
A . 常温下,pH=4的CH3COOH溶液中,由水电离的c(H+)=10-10 mol/L
B . 将pH=2的HCl溶液和pH=4的H2SO4溶液等体积混合,所得溶液pH=3
C . 0.1mol/L氨水和0.1mol/LNH4Cl溶液等体积混合后所得溶液pH>7,则c(NH4+)<c(NH3·H2O)
D . 向0.1mol/L、pH=1的NaHA溶液中加入NaOH溶液反应的离子方程式为:HA-+OH-=H2O+A2-
|
|
| 10. 单选题 | |
|
下列事实:
①NaHSO4溶液呈酸性;②长期使用化肥(NH4)2SO4会使土壤酸性增大,发生板结;③配制CuCl2溶液,用稀盐酸溶解CuCl2固体;④NaHS溶液中c(H2S)>c(S2-);⑤氯化铵溶液可去除金属制品表面的锈斑;⑥加热FeCl3·6H2O晶体,往往得不到FeCl3固体。 其中与盐类的水解有关的叙述有( )
A . 6项
B . 5项
C . 3项
D . 4项
|
|
高中化学 试卷推荐
- 重庆市缙云教育联盟2022届高三第三次诊断性检测化学试题
- 四川省成都市2021年高考理综-化学一模试卷
- 浙江省普通高中强基联盟2022届高三上学期12月统测化学试题
- 江苏省常州市教育学会2021-2022学年高一下学期期中学业水平监测化学试题
- 广东省广州市天河区2021年高考化学三模试卷
- 河南省郑州市2021年高考化学一模试卷
- 浙江省精诚联盟2020-2021学年高一下学期化学3月月考试卷
- 北京市朝阳区2020-2021学年高一上学期期末考试化学试题
- 山东省青岛市即墨区2020-2021学年高二上学期化学期中考试试卷
- 四川省成都市蓉城名校联盟2021-2022学年高二下学期联考化学试题
- 吉林省榆树市第一高级中学2020-2021学年高二上学期化学期中考试试卷
- 山西省大同市2022届高三上学期学情调研测试化学试题
最近更新