浙江省杭州市长征中学2020-2021学年高二下学期化学第一次月考试卷
浙江省杭州市长征中学2020-2021学年高二下学期化学第一次月考试卷
教材版本:化学
试卷分类:化学高二下学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高二下学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 计算题 | |
|
将铜与Fe2O3的混合物共ag加入20.0mL4.00mol·L-1的过量稀硫酸中,充分反应后剩余固体的质量为bg。请计算:
|
|
| 2. 综合题 | |
|
NH3是重要的化工原料,经一系列反应可得到HNO3、CO(NH2)2、HCN等产品。
|
|
| 3. 综合题 | |
|
某研究小组拟合成抗抑郁药西酞普兰中间体 5-腈基苯酞。
已知:① 请回答:
|
|
| 4. 单选题 | |
|
下列表示错误的是( )
A . 羟基的电子式:
|
|
| 5. 单选题 | |
|
设[aX+bY]为a个X微粒和b个Y微粒组成的一个微粒集合体,NA为阿伏加德罗常数的值。下列说法错误的是( )
A . H2(g)+
 O2(g)=H2O(l) ΔH=-286 kJ·mol−1 , 则每1 mol [H2(g)+ O2(g)=H2O(l) ΔH=-286 kJ·mol−1 , 则每1 mol [H2(g)+  O2(g)]生成1 mol [H2O(l)]放热286 kJ
B . Cr2O72-+ne−+14H+=2Cr3++7H2O,则每生成1 mol Cr3+转移电子数为3NA
C . Al3++4OH−=[Al(OH)4]− , 说明1 mol Al(OH)3电离出H+数为NA
D . 1 mol CO2与NaOH溶液完全反应,则n(CO32-)+n(HCO3-)+n(H2CO3)=1 mol O2(g)]生成1 mol [H2O(l)]放热286 kJ
B . Cr2O72-+ne−+14H+=2Cr3++7H2O,则每生成1 mol Cr3+转移电子数为3NA
C . Al3++4OH−=[Al(OH)4]− , 说明1 mol Al(OH)3电离出H+数为NA
D . 1 mol CO2与NaOH溶液完全反应,则n(CO32-)+n(HCO3-)+n(H2CO3)=1 mol
|
|
| 6. 单选题 | |
|
下列说法错误的是( )
A .
 的溶液不一定呈碱性
B . 中和pH和体积均相等的氨水、 的溶液不一定呈碱性
B . 中和pH和体积均相等的氨水、  溶液,所需 溶液,所需 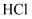 的物质的量相同
C . 相同温度下,pH相等的盐酸、 的物质的量相同
C . 相同温度下,pH相等的盐酸、  溶液中, 溶液中,  相等
D . 氨水和盐酸反应后的溶液,若溶液呈中性,则 相等
D . 氨水和盐酸反应后的溶液,若溶液呈中性,则 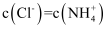
|
|
| 7. 单选题 | |
|
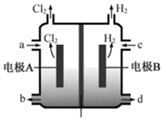
在氯碱工业中,离子交换膜法电解饱和食盐水示意图如下,下列说法错误的是( )
离子交换膜
A . 电极A为阳极,发生氧化反应生成氯气
B . 离子交换膜为阳离子交换膜
C . 饱和NaCl从a处进,NaOH溶液从d处出
D . OH-迁移的数量等于导线上通过电子的数量
|
|
| 8. 单选题 | |
|
在干燥的HCl气流中加热MgCl2·6H2O,能得到无水MgCl2。下列说法错误的是( )
A . MgCl2·nH2O(s)=MgCl2·(n-1)H2O(s)+H2O(g) ΔH>0
B . MgCl2·2H2O(s)=Mg(OH)2(s)+2HCl(g),HCl气流可抑制反应进行
C . MgCl2·H2O(s)=Mg(OH)Cl(s)+HCl(g),升高温度,反应更易发生
D . MgCl2·4H2O(s)=MgCl2·2H2O(s)+2H2O(g),HCl气流可抑制反应进行
|
|
| 9. 单选题 | |||||||||||||||||||||
|
一定温度下,在2 L的恒容密闭容器中发生反应
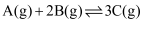 。反应过程中的部分数据如下表所示: 。反应过程中的部分数据如下表所示:
下列说法正确的是( )
A . 0~5 min用A表示的平均反应速率为
 B . 该反应在10 min后才达到平衡
C . 平衡状态时,
B . 该反应在10 min后才达到平衡
C . 平衡状态时,  D . 物质B的平衡转化率为20%
D . 物质B的平衡转化率为20%
|
|||||||||||||||||||||
| 10. 单选题 | |
|
在一定温度下,某反应达到了化学平衡,其反应过程对应的能量变化如图。
下列说法正确的是( )
A . Ea为逆反应活化能,Ea′为正反应活化能
B . 温度升高,逆反应速率加快幅度大于正反应加快幅度,使平衡逆移
C . 所有活化分子的平均能量高于或等于所有分子的平均能量
D . 该反应为放热反应,ΔH=Ea′-Ea
|
|
高中化学 试卷推荐
- 人教版化学高二选修5第二章第一节脂肪烃同步练习
- 浙江省宁波十校2019-2020学年高三下学期化学3月月考试卷
- 湖北省黄冈市2016-2017学年高一上学期化学期末考试试卷
- 2015-2016学年湖南省常德市汇文中学高二下学期期中化学试卷
- 广东省茂名市2020年高考理综-化学一模试卷
- 广西钦州市2015-2016学年高一下学期化学期末考试试卷
- 2015-2016学年山东省德州市武城二中高一下学期期中化学试卷
- 江苏省扬州市宝应县安宜高级中学2016-2017学年高二上学期化学期中考试试卷(选修)
- 2016年江西省宜春三中高考化学三模试卷
- 备考2018年高考化学一轮基础复习:专题4 氧化还原反应
- 2015-2016学年江西省吉安市高一上学期期末化学试卷
- 2017年宁夏中卫市高考化学一模试卷
最近更新
 NH2COONH4(l) Δ H1 = a kJ·mol-1
NH2COONH4(l) Δ H1 = a kJ·mol-1 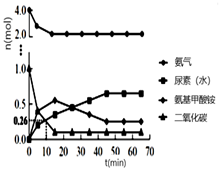
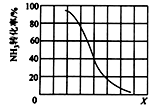
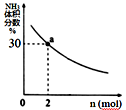

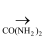
 ②
②