人教版高中化学选修四化学反应原理综合
人教版高中化学选修四化学反应原理综合
教材版本:化学
试卷分类:化学高二上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高二上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
“生物质能”主要是指树木、庄稼、草类等植物直接或间接提供的能量;古老的柴火做饭、烧炭取暖等粗放用能方式正被现代科学技术所改变,下面说法错误的是( )
A . 生物质能的缺点是严重污染环境
B . 生物质能源是可再生的能源
C . 利用生物质能就是间接利用太阳能
D . 使用沼气这种生物质能是对化学能的充分利用
|
|
| 2. 单选题 | |
|
在25 ℃时,水的离子积Kw=1.0×10-14 , 在35 ℃时,水的离子积Kw=2.1×10-14 , 则下列叙述正确的是( )
A . c(H+)随着温度的升高而降低
B . 35 ℃时,c(H+)<c(OH-)
C . 35 ℃时的水比25 ℃时的水电离程度小
D . 水的电离是吸热的
|
|
| 3. 单选题 | |
|
某种溶质的溶液的pH=2,向该溶液中加水到体积变为原来溶液体积的10倍,所得溶液的pH在2~3之间,则溶液中的溶质可能是( )
A . 强酸
B . 弱酸
C . 强碱
D . 弱碱
|
|
| 4. 单选题 | |
|
下图是甲醇燃料电池的结构示意图,甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为2CH3OH+3O2=2CO2+4H2O。下列说法不正确的是( )
A . 左电极为电池的负极,a处通入的物质是甲醇
B . 正极反应式为O2+2H2O+4e-=4OH-
C . 负极反应式为CH3OH+H2O-6e-=CO2+6H+
D . 该电池提供1 mol e- , 消耗氧气0.25 mol
|
|
| 5. 单选题 | |
|
某温度下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是( )
A . Ksp[Fe(OH)3]<Ksp[Cu(OH)2]
B . 加适量NH4Cl固体可使溶液由a点变到b点
C . c、d两点代表的溶液中c(H+)与c(OH-)乘积相等
D . Fe(OH)3、Cu(OH)2分别在b、c两点代表的溶液达到饱和
|
|
| 6. 单选题 | |
|
下图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加几滴石蕊溶液。下列实验现象描述正确的是( )
A . 逸出气体的体积,a电极的小于b电极的
B . 一电极逸出无味气体,另一电极逸出刺激性气体
C . a电极附近呈红色,b电极附近呈蓝色
D . a电极附近呈蓝色,b电极附近呈红色
|
|
| 7. 单选题 | |
|
下列电离方程式错误的是( )
A . (NH4)2SO4溶于水:(NH4)2SO4=2
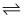 2H++SO42-
C . HF溶于水:HF 2H++SO42-
C . HF溶于水:HF 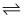 H++F
D . NaHCO3溶于水:NaHCO3=Na++HCO3-、HCO3- H++F
D . NaHCO3溶于水:NaHCO3=Na++HCO3-、HCO3- 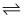 H++CO32- H++CO32-
|
|
| 8. 单选题 | |
|
在较稀FeCl3溶液中,存在如下水解平衡:Fe3++3H2O
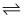 Fe(OH)3+3H+ , 在此溶液中滴入饱和的FeCl3溶液,下列说法正确的是( ) Fe(OH)3+3H+ , 在此溶液中滴入饱和的FeCl3溶液,下列说法正确的是( )
A . 水解平衡不移动
B . 水解平衡向逆反应方向移动
C . 溶液中H+浓度增大
D . Fe3+的水解程度增大
|
|
| 9. 单选题 | |
|
现有常温时pH=1的某强酸溶液10 mL,下列操作能使溶液的pH变成2的是
A . 加水稀释成100 mL
B . 加入10 mL的水进行稀释
C . 加入10 mL 0.01 mol·L-1的NaOH溶液
D . 加入10 mL 0.01 mol·L-1的HCl溶液
|
|
| 10. 单选题 | |
|
已知:H2(g)+
 O2(g)=H2O(l) ΔH=-285.83 kJ·mol-1 O2(g)=H2O(l) ΔH=-285.83 kJ·mol-1CO(g)+ 若氢气与一氧化碳的混合气体完全燃烧可生成5.4 g H2O(l),并放出114.04 kJ热量,则混合气体中CO的物质的量为( )
A . 0.22 mol
B . 0.15 mol
C . 0.1 mol
D . 0.05 mol
|
|
最近更新






