山西省沁源县第一中学2020-2021学年高二下学期化学开学考试试卷
山西省沁源县第一中学2020-2021学年高二下学期化学开学考试试卷
教材版本:化学
试卷分类:化学高二下学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高二下学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
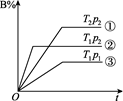
已知某可逆反应m A(g)+n B(g)
 p C(g)在密闭容器中进行,下图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数B%的关系曲线,由曲线分析,下列判断正确的是( ) p C(g)在密闭容器中进行,下图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数B%的关系曲线,由曲线分析,下列判断正确的是( )
A . T1<T2 p1>p2 m+n>p 放热反应
B . T1>T2 p1<p2 m+n>p 吸热反应
C . T1<T2 p1>p2 m+n<p 放热反应
D . T1>T2 p1<p2 m+n<p 吸热反应
|
|
| 2. 单选题 | |
|
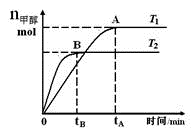
在恒容密闭容器中,由CO合成甲醇:CO(g) + 2H2(g)
 CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是( ) CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是( )
A . 平衡常数K=
 B . 该反应在T1时的平衡常数比T2时的小
C . CO合成甲醇的反应为吸热反应
D . 处于A点的反应体系从T1变到T2 , 达到平衡时
B . 该反应在T1时的平衡常数比T2时的小
C . CO合成甲醇的反应为吸热反应
D . 处于A点的反应体系从T1变到T2 , 达到平衡时  增大 增大
|
|
| 3. 单选题 | |
|
已知H2(g)+Cl2(g)=2HCl(g)△H=-184.6kJ/mol,则反应HCl(g)=
 H2(g)+ H2(g)+  Cl2(g)的△H为( ) Cl2(g)的△H为( )
A . +184.6kJ/mol
B . -92.3kJ/mol
C . -369.2kJ/mol
D . +92.3kJ/mol
|
|
| 4. 单选题 | |||||||||
|
根据下表的数据,H2(g)+Cl2(g)=2HCl(g)的反应热应为( )
部分物质的键能
A . +183.0 kJ·mol-1
B . -366.0 kJ·mol-1
C . -183.0 kJ·mol-1
D . +211.0 kJ·mol-1
|
|||||||||
| 5. 单选题 | |
|
在一个密闭容器中盛有N2和H2 , 它们的起始浓度分别是1.8 mol /L和5.4 mol /L,在一定的条件下它们反应生成NH3 , 10 min后测得N2的浓度是0.8 mol /L,则在这10 min内用NH3来表示的平均反应速率是( )
A . 0.1 mol /(L·min)
B . 0.2 mol /(L·min)
C . 0.3 mol /(L·min)
D . 0.6 mol /(L·min)
|
|
| 6. 单选题 | |
|
在密闭容器中进行反应:X2(g)+Y2(g)⇌2Z(g),已知X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.3mol·L-1、0.2mol·L-1 , 在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )。
A . Z为0.3 mol·L-1
B . Y2为0.4 mol·L-1
C . X2为0.2 mol·L-1
D . Z为0.4 mol·L-1
|
|
| 7. 单选题 | |
|
现有0.1mol·L-1氨水10mL,加蒸馏水稀释到1L后,下列变化中正确的是( )
①电离程度增大②[NH3·H2O]增大③
A . ①②③
B . ①③⑤
C . ①③⑥
D . ②④⑥
|
|
| 8. 单选题 | |
|
有四种物质的量浓度相等且都由一价阳离子A+和B+及一价阴离子X-和Y-组成的盐溶液。据测定常温下AX和BY溶液的pH=7,AY溶液的pH>7,BX溶液的pH<7,由此判断不水解的盐是( )
A . BX
B . AY
C . AX
D . BY
|
|
| 9. 单选题 | |
|
下列是某同学做铜锌原电池实验后得出的结论和认识,其中正确的是( )
A . 构成原电池正极和负极的材料必须是两种金属
B . 由铜、锌做电极与硫酸铜溶液组成的原电池中铜是负极
C . 电子沿导线由锌流向铜,通过硫酸溶液被氢离子得到而放出氢气
D . 铜锌原电池工作时,若有13g 锌被溶解,电路中就有0.4 mol电子通过
|
|
| 10. 单选题 | |
|
锂电池是新一代高能电池,目前已研发出多种锂电池。某种锂电池的总反应式为Li + MnO2 =LiMnO2 , 下列说法中正确的是( )
A . Li是正极,MnO2 是负极
B . 放电时负极的应应:Li - e- =Li+
C . 放电时正极发生氧化反应
D . 电池放电时,产生高锰酸根离子
|
|
高中化学 试卷推荐
- 人教版化学高二选修6第一单元实验1-3污水处理电浮选凝聚法同步练习
- 吉林省榆树一中五校联考2018-2019学年高二上学期化学期末考试试卷
- 2015-2016学年陕西省宝鸡市金台区高二下学期期中化学试卷
- 2015年河南河北山西三省高考化学考前模拟试卷(二)
- 河南省周口市2017-2018学年高二下学期化学期末考试试卷
- 山东省泰安市2019-2020学年高二下学期化学期末考试试卷
- 人教版化学高二选修1第一章第三节生命的基础——蛋白质同步练习
- 山东省淄博六中2016-2017学年高二上学期化学期中考试试卷
- 北京市东城区2017-2018学年高二下学期化学期末考试试卷
- 上海市宝山区2018-2019学年高考化学一模考试试卷
- 陕西省渭南市临渭区2019-2020学年高二下学期化学期末考试试卷
- 2017年高考化学备考复习专题十四:烃的衍生物
最近更新
 数目增多④[OH-]增大⑤导电性增强⑥
数目增多④[OH-]增大⑤导电性增强⑥  增大⑦
增大⑦  减小
减小


