北京市门头沟区2022届高三一模化学试题
北京市门头沟区2022届高三一模化学试题
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |||||||||||||
|
第24届冬季奥林匹克运动会在北京市和张家口市成功举办。下列不属于化学变化的是( )
A . A
B . B
C . C
D . D
|
|||||||||||||
| 2. 单选题 | |
|
下列化学用语或表示不正确的是( )
A . 甲基的电子式:
 C . 中子数为18的氯原子:
C . 中子数为18的氯原子: Cl
D . 基态Cr的电子排布式:1s22s22p63s23p63d44s2 Cl
D . 基态Cr的电子排布式:1s22s22p63s23p63d44s2
|
|
| 3. 单选题 | |
|
下列表述不正确的是( )
A . 原子轨道能量:1s<2s<3s<4s
B . M电子层存在3个能级、9个原子轨道
C . 4s电子能量较高,总是在比3s电子离核更远的地方运动
D . 同一周期,碱金属元素的第一电离能最小,最容易失电子
|
|
| 4. 单选题 | |
|
将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。下列叙述不正确的是( )
A . H2S和空气通过上述循环的目的是降低活化能,提高总反应速率
B . 在转化过程中能循环利用的物质是FeCl3和CuCl2
C . 该过程的总反应式为:2H2S+O2
 2H2O+2S↓
D . 若有1molH2S发生图示转化的同时消耗O2为0.4mol,则混合液中Fe3+浓度增大 2H2O+2S↓
D . 若有1molH2S发生图示转化的同时消耗O2为0.4mol,则混合液中Fe3+浓度增大
|
|
| 5. 单选题 | |||||||||||||
|
下列装置能达到相应实验目的的是( )
A . A
B . B
C . C
D . D
|
|||||||||||||
| 6. 单选题 | |
|
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A . 1L0.2mol·L-1NH4Cl溶液中,NH
 的数目为0.2NA
B . 标准状况下,11.2LCCl4含共用电子对数为2NA
C . 24g正丁烷和5g异丁烷的混合物中含共价键数目为6.5NA
D . 等质量的O2和O3中,所含电子数之比为2∶3 的数目为0.2NA
B . 标准状况下,11.2LCCl4含共用电子对数为2NA
C . 24g正丁烷和5g异丁烷的混合物中含共价键数目为6.5NA
D . 等质量的O2和O3中,所含电子数之比为2∶3
|
|
| 7. 单选题 | |
|
近期,我国研究人员报道了温和条件下实现固氮的一类三元NiFeV催化剂,如图为其电催化固氮的机理示意图。以下关于该电催化机理过程的描述不正确的是( )
A . 反应在酸性条件下进行
B . 反应过程涉及N2的氧化反应
C . 1个N2分子反应生成2个NH3分子
D . 反应分多步进行,中间产物为几种不同的氮氢化物
|
|
| 8. 单选题 | |
|
下列用于解释实验事实的离子方程式不正确的是( )
A . 酚酞滴入碳酸钠溶液中,溶液变红色:CO
 +2H2O +2H2O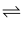 H2CO3+2OH-
B . 向NaHCO3溶液中加入少量澄清石灰水,有白色沉淀生成:2HCO H2CO3+2OH-
B . 向NaHCO3溶液中加入少量澄清石灰水,有白色沉淀生成:2HCO +Ca2++2OH-=CaCO3↓+CO +Ca2++2OH-=CaCO3↓+CO +2H2O
C . FeSO4溶液滴入溴水中,溴水颜色变浅:2Fe2++Br2=2Fe3++2Br-
D . 苯酚钠溶液中通入少量CO2气体,溶液变浑浊:C6H5O-+CO2+H2O=C6H5OH+HCO +2H2O
C . FeSO4溶液滴入溴水中,溴水颜色变浅:2Fe2++Br2=2Fe3++2Br-
D . 苯酚钠溶液中通入少量CO2气体,溶液变浑浊:C6H5O-+CO2+H2O=C6H5OH+HCO
|
|
| 9. 单选题 | |||||||||||||
|
已知[Co(H2O)6]2+呈粉红色、[CoCl4]2—呈蓝色、[ZnCl4]2—为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:[Co(H2O)6]2++4Cl—
 [CoCl4]2—+6H2O △H,将该溶液分为三份做实验,溶液的颜色变化如表: [CoCl4]2—+6H2O △H,将该溶液分为三份做实验,溶液的颜色变化如表:
以下结论和解释正确的是( )
A . 等物质的量的[Co(H2O)6]2+和[CoCl4]2—中σ键数之比为3:2
B . 由实验①可知:△H<0,由实验②可推知加水稀释,浓度熵Q<K,平衡逆向移动
C . 由实验③可知:Zn2+络合Cl—能力比Co2+络合Cl—能力弱
D . 实验①②③可知:配合物的形成与温度、配体的浓度及配体的种类等有关
|
|||||||||||||
| 10. 单选题 | |
|
工业上可通过甲醇羰基化法制取甲酸甲酯:CH3OH(g)+CO(g)
 HCOOCH3(g),在容积固定的密闭容器中,投入等物质的量CH3OH和CO,测得相同时间内CO的转化率随温度变化如图所示,下列说法正确的是( ) HCOOCH3(g),在容积固定的密闭容器中,投入等物质的量CH3OH和CO,测得相同时间内CO的转化率随温度变化如图所示,下列说法正确的是( )
A . 反应速率vb>vd
B . 由图可知生产时反应温度控制在80~85℃为宜
C . 向该容器中充入N2 , CH3OH的转化率增大
D . d→e,CO的转化率随温度的升高而减小,是因为该反应是吸热反应,升高温度反应正向移动
|
|
高中化学 试卷推荐
- 北京市大兴区2021-2022学年高二上学期期中考试化学试题
- 福建省福州市八县(市)协作校2021-2022学年高二上学期期中联考化学试题
- 福建省三明市教研联盟校2021-2022学年高二上学期期中联考化学试题
- 江苏省常熟市2021-2022学年高二上学期期中考试化学试题
- 江苏省淮安市高中校协作体2021-2022学年高二上学期期中考试化学(选修)试题
- 江苏省宿迁市沭阳县2021-2022学年高二上学期期中调研测试化学试题
- 江苏省徐州市2021-2022学年高二上学期期中考试化学试题
- 辽宁省六校2021-2022学年高二上学期期中考试化学试题
- 山西省怀仁市2021-2022学年高二上学期期中化学试题
- 山西省太原市2021-2022学年高二上学期期中考试化学试题
- 福建省福州市福清市高中联合体2021-2022学年高一上学期期中考试化学试题
- 江苏省常熟市2021-2022学年高一上学期期中化学试题
最近更新















