2015-2016学年江西省赣州市于都三中高二下学期第一次月考化学试卷
2015-2016学年江西省赣州市于都三中高二下学期第一次月考化学试卷
教材版本:化学
试卷分类:化学高二下学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高二下学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
已知:①C(s)+O2(g)=CO2(g);△H=﹣393.5kJ/mol.
②H2(g)+ 现有0.2mol的炭粉和氢气组成的悬浮气在氧气中完全燃烧,共放出55.945kJ热量,则混合物中C(s)与H2的物质的量之比为( )
A . 1:1
B . 1:2
C . 1:3
D . 1:4
|
|
| 2. 单选题 | |
|
燃料电池能有效提高能源利用率,具有广泛的应用前景.下列物质均可用作燃料电池的燃料,其中最环保的是( )
A . 甲醇
B . 天然气
C . 液化石油气
D . 氢气
|
|
| 3. 单选题 | |
|
下列变化过程,属于放热反应的是( )
①生石灰与水反应 ②酸碱中和反应 ③浓H2SO4稀释 ④固体氢氧化钠溶于水 ⑤H2在Cl2中燃烧 ⑥醋酸电离 ⑦NH4Cl晶体与Ba(OH)2•8H2O混合搅拌
A . ①②⑤
B . ①②③④⑤
C . ①③④
D . ⑥⑦
|
|
| 4. 单选题 | |
|
下列说法或表示方法正确的是( )
A . 生成物总能量高于反应物总能量,该反应不能发生
B . 需要加热的反应一定是吸热反应
C . 由石墨比金刚石稳定,可知C(石墨)(s)═C(金刚石)(s);△H>0
D . 稀盐酸和氨水发生中和反应的热化学方程式可表示为:H+(aq)+OH﹣(aq)═H2O(l);△H=﹣57.3 kJ•mol﹣1
|
|
| 5. 单选题 | |
|
下列说法正确的是( )
A . 灼热的木炭与CO2的反应既属于氧化还原反应,又是放热反应
B . 决定化学反应速率快慢的主要因素是温度
C . 物质发生化学反应都伴随着能量变化
D .
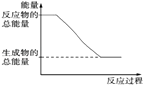 能量变化如图所示的化学反应是吸热反应 能量变化如图所示的化学反应是吸热反应
|
|
| 6. 单选题 | |
|
25℃、101kPa下,碳、氢气、甲烷和一氧化碳的燃烧热依次是﹣393.5kJ/mol、﹣285.8kJ/mol、﹣890.3kJ/mol、﹣283kJ/mol,则下列热化学方程式正确的是( )
A . C(s)+
 O2(g)=CO(g);△H=﹣393.5kJ/mol
B . H2(g)+ O2(g)=CO(g);△H=﹣393.5kJ/mol
B . H2(g)+  O2(g)=H2O(l);△H=+285.8kJ/mol
C . CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=﹣890.3kJ/mol
D . 2CO(g)+O2(g)=2CO2(g);△H=﹣566kJ/mol O2(g)=H2O(l);△H=+285.8kJ/mol
C . CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=﹣890.3kJ/mol
D . 2CO(g)+O2(g)=2CO2(g);△H=﹣566kJ/mol
|
|
| 7. 单选题 | |
|
已知下列反应的热化学方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)═2C3H5(ONO2)3(l)△H1 2H2(g)+O2(g)═2H2O(g)△H2 C(s)+O2(g)═CO2(g)△H3 则反应4C3H5(ONO2)3(l)═12CO2(g)+10H2O(g)+O2(g)+6N2(g)的△H为( )
A . 12△H3+5△H2﹣2△H1
B . 2△H1﹣5△H2﹣12△H3
C . 12△H3﹣5△H2﹣2△H1
D . △H1﹣5△H2﹣12△H3
|
|
| 8. 单选题 | |
|
已知:CO(g)+
 O2(g)=CO2(g);△H=﹣283kJ/mol O2(g)=CO2(g);△H=﹣283kJ/mol Na2O2(s)+CO2(g)═Na2CO3(s)+ 根据以上热化学方程式判断,下列说法正确的是( )
A . CO的燃烧热为283kJ
B .
 如图可表示由CO生成CO2的反应过程和能量关系
C . Na2O2(s)+CO(g)=Na2CO3(s);△H=﹣509kJ/mol
D . Na2O2(s)与CO2(g)反应放出226kJ热量时,电子转移数为2NA 如图可表示由CO生成CO2的反应过程和能量关系
C . Na2O2(s)+CO(g)=Na2CO3(s);△H=﹣509kJ/mol
D . Na2O2(s)与CO2(g)反应放出226kJ热量时,电子转移数为2NA
|
|
| 9. 单选题 | |
|
CO(g)+H2O(g)⇌H2(g)+CO2(g)△H<0,在其他条件不变的情况下( )
A . 加入催化剂,改变了反应的途径,反应的△H也随之改变
B . 改变压强,平衡不发生移动,反应放出的热量不变
C . 升高温度,反应速率加快,反应放出的热量不变
D . 若在原电池中进行,反应放出的热量不变
|
|
| 10. 单选题 | |
|
下列条件一定能使反应速率加快的是( )
①增加反应物的物质的量 ②升高温度 ③缩小反应容器的体积 ④加入生成物 ⑤加入MnO2 .
A . 全部
B . ①②⑤
C . ②
D . ②③
|
|
高中化学 试卷推荐
- 北京市石景山区2021届高三上学期期末考试化学试题
- 浙江省百校2021-2022学年高三下学期开学模拟检测化学试题
- 四川省德阳市2022届高三下学期第二次诊断考试(二模)理科综合化学试题
- 浙江省“七彩阳光”新高考研究联盟2021-2022学年高二上学期期中联考化学试题
- 浙江省衢州五校联盟2020-2021学年高一上学期化学期末考试试卷
- 广东省广州市三校联考2020-2021学年高二上学期化学期末考试试卷
- 云南省玉溪市2021-2022学年高二上学期期末教学质量检测化学试题
- 浙江金华十校2021-2022学年高一上学期期末调研考试化学试题
- 北京市门头沟区2021年高考化学一模试卷
- 浙江省金丽衢十二校2021年高考化学二模试卷
- 山东省潍坊市2020-2021学年高二下学期化学期中考试试卷
- 山东省临沂市2020-2021学年高三上学期化学期中考试试卷
最近更新
 O2(g)=H2O(g);△H=﹣241.8kJ/mol.
O2(g)=H2O(g);△H=﹣241.8kJ/mol.


