物质的量浓度及其相关计算-2022高考化学一轮复习
物质的量浓度及其相关计算-2022高考化学一轮复习
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
将V L浓度为0.3mol/L的盐酸浓度扩大一倍,采取的措施合理的是( )
A . 将溶液加热浓缩至原来体积的一半
B . 通入标准状况下的HCl气体6.72L
C . 加入3mol/L的盐酸0.2V L,再稀释至1.5V L
D . 加入等体积0.9mol/L的盐酸,混合均匀
|
|
| 2. 单选题 | |
 为阿伏加德罗常数,下列说法正确的是( ) 为阿伏加德罗常数,下列说法正确的是( )
A . 标准状况下,22.4L的
 的物质的量为1mol
B . 现有乙烯、丙烯的混合气体共14g,其原子数为3 的物质的量为1mol
B . 现有乙烯、丙烯的混合气体共14g,其原子数为3  C . 28g乙烯所含共用电子对数目为5
C . 28g乙烯所含共用电子对数目为5  D . 1mol羟基所含电子数为10
D . 1mol羟基所含电子数为10 
|
|
| 3. 单选题 | |
|
NA代表阿伏加德罗常数的数值。下列有关NA的叙述中,正确的是( )
A . 标准状况下,11.2 LCCl4所含的分子数为0.5NA
B . 14 g氮气所含的氮原子数为NA
C . 1 mol/L H2SO4 的阴、阳离子总数为3NA
D . 12 mol/L的浓硫酸 50 mL与足量的Cu加热反应,得到SO2为0.3NA
|
|
| 4. 单选题 | |
|
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A . 1mol/LFe(NO3)2溶液中,NO
 的数目是2NA
B . 反应4FeS2+11O2 的数目是2NA
B . 反应4FeS2+11O2  2Fe2O3+8SO2 , 每生成1molFe2O3转移电子数目22NA
C . 标准状况下,2.24LNO2溶于足量水中充分反应,转移电子数0.1NA
D . 密闭容器中,2molSO2与2molO2充分反应,容器中分子总数为3NA 2Fe2O3+8SO2 , 每生成1molFe2O3转移电子数目22NA
C . 标准状况下,2.24LNO2溶于足量水中充分反应,转移电子数0.1NA
D . 密闭容器中,2molSO2与2molO2充分反应,容器中分子总数为3NA
|
|
| 5. 单选题 | |
|
亚硝酸
 是一种弱酸,一定条件下在水溶液中部分电离出 是一种弱酸,一定条件下在水溶液中部分电离出 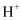 和 和  。 。 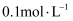 的亚硝酸溶液,当其达到电离平衡时,溶液中 的亚硝酸溶液,当其达到电离平衡时,溶液中  的浓度c为( ) 的浓度c为( )
A .
 B .
B .  C .
C .  D .
D . 
|
|
| 6. 单选题 | |
|
设
 为阿伏加德罗常数的值,下列说法正确的是( ) 为阿伏加德罗常数的值,下列说法正确的是( )
A .
 中,生成0.6molS,转移电子数为0.8 中,生成0.6molS,转移电子数为0.8  B . 3.0g
B . 3.0g  含有的共用电子对数为0.6 含有的共用电子对数为0.6  C . 质量分数为a%的硝酸稀溶液的物质的量浓度为bmol/L,则溶液密度为
C . 质量分数为a%的硝酸稀溶液的物质的量浓度为bmol/L,则溶液密度为  D . 质量相等,密度不等的
D . 质量相等,密度不等的  和CO,含有的分子数不相等 和CO,含有的分子数不相等
|
|
| 7. 单选题 | |
|
已知NA为阿伏加德罗常数的值。下列说法正确的是( )
A . 1molNH4F晶体中含有共价键数目为4NA
B . 1L0.1mol/L磷酸钠溶液含有的
 数目与0.1L1mol/L磷酸钠溶液含有的 数目与0.1L1mol/L磷酸钠溶液含有的  数目相等
C . 标况下,3.36LHF中含有的质子数为1.5NA
D . 60gSiO2晶体中含有的Si-O键数目为2NA 数目相等
C . 标况下,3.36LHF中含有的质子数为1.5NA
D . 60gSiO2晶体中含有的Si-O键数目为2NA
|
|
| 8. 单选题 | |
|
设
 为阿伏加德罗常数,下列说法正确的是( ) 为阿伏加德罗常数,下列说法正确的是( )
A . 常温常压下
 和 和  完全燃烧生成 完全燃烧生成  的 的  B .
B .  晶体中含有离子数为4 晶体中含有离子数为4  C .
C .  通入足量的NaOH溶液中充分反应,转移的电子数0.2 通入足量的NaOH溶液中充分反应,转移的电子数0.2  D . 将含
D . 将含  的溶液滴入沸水所制得的 的溶液滴入沸水所制得的 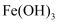 胶体粒子数目为 胶体粒子数目为 
|
|
| 9. 综合题 | |
|
为确定某碱式碳酸镁
 的组成,某同学取23.3g样品置于硬质玻璃管中充分灼烧至恒重,残留固体质量为10.0g,将产生的气体先通过足量98%的浓硫酸( 的组成,某同学取23.3g样品置于硬质玻璃管中充分灼烧至恒重,残留固体质量为10.0g,将产生的气体先通过足量98%的浓硫酸( 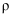 为 为  ),再通过足量的碱石灰,碱石灰质量增加8.8g。请计算: ),再通过足量的碱石灰,碱石灰质量增加8.8g。请计算:
|
|
| 10. 综合题 | |
|
|
最近更新



