2016年江西省宜春市靖安县高考化学二模试卷
2016年江西省宜春市靖安县高考化学二模试卷
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
下列说法正确的是( )
A . 因为SO2具有漂白性,所以它能使品红溶液、溴水、KMnO4(H+)、石蕊溶液褪色
B . 能使品红溶液褪色的不一定是SO2
C . SO2、漂白粉、活性炭、Na2O2都能使红墨水褪色,其原理相同
D . SO2和Cl2等物质的量混合后同时通入装有湿润的有色布条的集气瓶中,漂白效果更好
|
|
| 2. 单选题 | |
|
下列排列顺序不正确的是( )
A . 热稳定性:H2O>NH3>PH3
B . 原子半径:Si>Na>O
C . 碱性:CsOH>KOH>NaOH
D . 失电子能力:K>Na>Mg
|
|
| 3. 单选题 | |
|
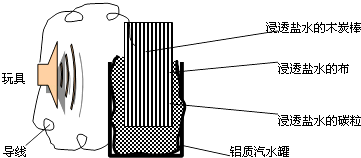
利用生活中常见的材料可以进行很多科学实验,甚至制作出一些有实际应用价值的装置来,如图就是一个用废旧材料制作的可用于驱动玩具的电池的示意图.上述电池工作时,有关说法正确的是( )
A . 铝罐将逐渐被腐蚀
B . 碳粒和炭棒上发生的反应为:O2+4e﹣=2O2﹣
C . 炭棒应与玩具电机的负极相连
D . 该电池工作一段时间后炭棒和炭粒的质量会减轻
|
|
| 4. 单选题 | |
|
下列离子方程式书写正确的是( )
A . 向碳酸钠溶液中滴加与其溶质的物质的量相等的盐酸:CO
 +2H+═CO2↑+H2O
B . 向苯酚钠溶液中通入少量的CO2: +2H+═CO2↑+H2O
B . 向苯酚钠溶液中通入少量的CO2:  C . 足量铁粉与稀硝酸反应:Fe+4H++NO
C . 足量铁粉与稀硝酸反应:Fe+4H++NO  ═Fe3++2H2O+NO↑
D . 向漂白粉溶液中通入少量二氧化硫:Ca2++2ClO﹣+SO2+H2O=CaSO3↓+2HClO ═Fe3++2H2O+NO↑
D . 向漂白粉溶液中通入少量二氧化硫:Ca2++2ClO﹣+SO2+H2O=CaSO3↓+2HClO
|
|
| 5. 单选题 | |
|
烷烃分子可以看作由以下基团组合而成:
A . 6
B . 7
C . 8
D . 10
|
|
| 6. 单选题 | |
|
4molA和2molB放入2L密闭容器中发生反应2A(g)+B(g)⇌2C(g),△H<0.4s后反应达到平衡状态,此时测得C的浓度为0.6mol/L.下列说法正确的是( )
A . 4s内,v(B)=0.075mol/(L•s)
B . 当c(A):c(B):c(C)=2:1:2时,该反应即达到平衡状态
C . 达到平衡状态后,若只升高温度,则C的物质的量浓度增大
D . 达到平衡状态后,若温度不变,缩小容器的体积,则A的转化率降低
|
|
| 7. 单选题 | |
|
实验室中,要使AlCl3溶液中的Al3+离子全部沉淀出来,适宜用的试剂是( )
A . NaOH溶液
B . Ba(OH)2溶液
C . 盐酸
D . 氨水
|
|
| 8. 单选题 | |
|
下列事实不能用金属活动性解释的是( )
A . 生活中可用铝制的水壶烧水
B . 镀锌铁制品破损后,镀层仍能保护铁制品
C . 工业上常用热还原法冶炼铁,用电解法冶炼钠
D . 电解法精炼铜时,其含有的Ag、Au杂质沉积在电解槽的底部
|
|
| 9. 推断题 | |
|
常见的六种盐A、B、C、D、E、F,它们的阳离子可能是Na+、NH4+、Cu2+、Ba2+、Al3+、Ag+ , 阴离子可能是Cl﹣、NO
 、SO 、SO  、CO 、CO  、SO 、SO  ,(阴、阳离子可能重复)已知: ,(阴、阳离子可能重复)已知: ①六种盐均溶于水,水溶液均为无色. ②A的溶液呈中性,B、C、E的溶液呈酸性,D、F的溶液呈碱性. ③D、F的焰色反应呈黄色,向F溶液加入少量FeCl3溶液,得到浅绿色溶液. ④若在这六种盐的溶液中,分别加入氨水,E和C的溶液中生成沉淀,继续加氨水,C中沉淀消失. ⑤若在这六种盐的溶液中分别加入Ba(NO3)2溶液,只有A、C的溶液不产生沉淀. ⑥把A的溶液分别加入到B、C、E的溶液中,均能生成不溶于稀硝酸的沉淀. 请回答下列问题:
|
|
| 10. 综合题 | |||||||||||||||||||||||||||||||||||||
|
下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题;(回答问题时,均需使用元素的真实元素符号,不得使用数字编号)
|
|||||||||||||||||||||||||||||||||||||
高中化学 试卷推荐
- 云南省昆明市2017-2018学年高考理综-化学3月模拟考试试卷
- 广东省云浮市2019-2020学年高一下学期化学期末考试试卷
- 人教版化学高一必修一第四章第一节无机非金属材料的主角--硅同步练习
- 人教版化学高二选修1第三章第四节塑料、纤维和橡胶同步练习
- 2016-2017学年天津市芦台一中等六校联考高二上学期期中化学试卷
- 天津市武清区2018-2019学年高三上学期化学期中考试试卷
- 人教版化学高二选修5第四章第一节油脂同步练习
- 四川省达州市2016-2017学年高二上学期化学期末考试试卷
- 安徽省天长市铜城中学2018-2019学年高一下学期化学期末考试试卷
- 专题10:硫及其化合物
- 人教版化学高二选修2第一单元课题2人工固氮技术——合成氨同步练习
- 山东省潍坊市2020年高考化学一模试卷
最近更新