2019年高考化学真题分类汇编专题06:无机物的转化、鉴别、除杂0
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | |
|
硼酸(H3BO3)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含Mg2B2O5·H2O、SiO2及少量Fe2O3、Al2O3)为原料生产硼酸及轻质氧化镁的工艺流程如下:
回答下列问题:
|
|
| 2. 综合题 | |
|
硫酸铁铵[NH4Fe(SO4)2·xH2O]是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:
回答下列问题:
|
|
| 3. 单选题 | |
|
下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是( )
A . A
B . B
C . C
D . D
|
|
| 4. 综合题 | |
|
化学小组实验探究
 与 与 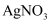 溶液的反应。 溶液的反应。
|
|
| 5. 实验探究题 | |
|
立德粉ZnS·BaSO4(也称锌钡白),是一种常用白色颜料。回答下列问题:
|
|
| 6. 单选题 | ||||||||||||||||
|
下列实验不能达到目的的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 7. 实验探究题 | |||||||||||||||||||||||||
|
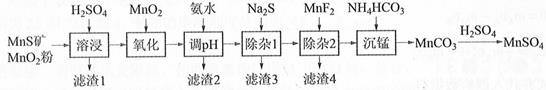
高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:
相关金属离子[c0(Mn+)=0.1 mol·L−1]形成氢氧化物沉淀的pH范围如下:
|
|||||||||||||||||||||||||
| 8. 单选题 | |
|
在给定条件下,下列选项所示的物质间转化均能实现的是( )
A . NaCl(aq)
 Cl2(g) Cl2(g)  FeCl2(s)
B . MgCl2(aq) FeCl2(s)
B . MgCl2(aq)  Mg(OH)2(s) Mg(OH)2(s)  MgO (s)
C . S(s) MgO (s)
C . S(s)  SO3(g) SO3(g)  H2SO4(aq)
D . N2(g) H2SO4(aq)
D . N2(g)  NH3(g) NH3(g)  Na2CO3(s) Na2CO3(s)
|
|
| 9. 单选题 | ||||||||||||||||
|
室温下进行下列实验,根据实验操作和现象所得到的结论正确的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 10. 实验探究题 | |
|
实验室以工业废渣(主要含CaSO4·2H2O,还含少量SiO2、Al2O3、Fe2O3)为原料制取轻质CaCO3和(NH4)2SO4晶体,其实验流程如下:
|
|
- 江苏省扬州市2020-2021学年高三下学期化学开学考试试卷
- 山西省吕梁市2020-2021学年高二下学期期末考试化学试题
- 山东省青岛胶州市2020-2021学年高一下学期化学期中考试试卷
- 河南省洛阳市2020-2021学年高三上学期化学期中考试试卷
- 四川省宜宾市2022届普通高中高考适应性考试理科综合化学试题
- 陕西省渭南市大荔县2020-2021学年高一上学期期末考试化学试题
- 湖北省石首市2021-2022学年高二下学期期中考试化学试题
- 山东省潍坊市2020-2021学年高一上学期化学期末考试试卷
- 陕西省宝鸡市2021年高考化学5月模拟试卷
- 浙江省名校新高考研究联盟(Z20联盟)2020-2021学年高三上学期化学第二次月考试卷
- 广东省汕头市潮阳区2020-2021学年高二上学期化学期末考试试卷
- 备考2021年高考化学二轮专题 第2讲 非金属元素及其化合物

 H++B(OH)−4 , Ka=5.81×10−10 , 可判断H3BO3是酸;在“过滤2”前,将溶液pH调节至3.5,目的是。
H++B(OH)−4 , Ka=5.81×10−10 , 可判断H3BO3是酸;在“过滤2”前,将溶液pH调节至3.5,目的是。




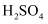 与Cu反应的化学方程式是
与Cu反应的化学方程式是 、
、  或二者混合物。
或二者混合物。 
 ,进而推断B中含有
,进而推断B中含有  的产生有两个途径:
的产生有两个途径: 被氧化为
被氧化为  进入D。
进入D。 溶液,未出现白色沉淀,可判断B中不含
溶液,未出现白色沉淀,可判断B中不含 
 =2I−+
=2I−+  。测定时消耗Na2S2O3溶液体积V mL。终点颜色变化为,样品中S2−的含量为(写出表达式)。
。测定时消耗Na2S2O3溶液体积V mL。终点颜色变化为,样品中S2−的含量为(写出表达式)。
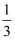 时,z=。
时,z=。

 (aq)
(aq)  (aq)达到平衡,则溶液中
(aq)达到平衡,则溶液中  =[Ksp(CaSO4)=4.8×10−5 , Ksp(CaCO3)=3×10−9]。
=[Ksp(CaSO4)=4.8×10−5 , Ksp(CaCO3)=3×10−9]。




