第3节 原子结构的模型 知识点题库
加碘食盐中的“碘”是指( )
A . 分子
B . 原子
C . 元素
D . 单质
与铵根离子(NH  )具有相同的质子数和电子数的微粒是( )
)具有相同的质子数和电子数的微粒是( )
 )具有相同的质子数和电子数的微粒是( )
)具有相同的质子数和电子数的微粒是( )
A . Na+
B . OH-
C . H2O
D . LiF
济阳仁风镇是“中国西瓜之乡”,生产的富硒西瓜色泽好、糖分高、口感佳,被农业部认证为国家级“无公害产品”和“绿色食品”.
-
(1)
西瓜适合在弱酸性土壤中生长,某校化学课外小组的同学,为了考查某地土壤是否适合种植西瓜,对其土壤进行了实验分析,具体实验步骤如下:
①将在该地多点选取的土壤混合,并研成粉末装.
②称量一定质量的土壤粉末置于烧杯中,加入适量水,搅拌.
③将充分溶解后的混合液进行过滤,所使用的装置如图所示,请指出图中的一项错误:

④用pH试纸测定过滤后所得土壤溶液的pH,测定的具体方法是
-
(2) 经测定,该土壤溶液的pH为8,为了适合西瓜种植,需对该土壤的酸碱性进行调节,则下列各项中,可采用的是(填选项序号)
①施以氢氧化钙粉末 ②施以碳酸钙粉末 ③用氨水进行喷灌 ④适量施用酸性肥料
-
(3) 硒(Se)是人体所需要的重要矿物质营养素,有“抗癌之王”的美称,硒的原子序数为34,其相对原子质量为79,硒原子最外电子层上有6个电子,则下列说法中,不正确的是(填选项序号)
①硒为非金属元素
②一个硒原子的原子核内有34个质子
③硒原子很容易失去电子
④富硒西瓜中的硒元素以化合物形态存在.
下列互为同位素的是( )
A .  、
、 、
、 B . 白磷、红磷
C . 重水、水
D . 金刚石、石墨
B . 白磷、红磷
C . 重水、水
D . 金刚石、石墨
 、
、 、
、 B . 白磷、红磷
C . 重水、水
D . 金刚石、石墨
B . 白磷、红磷
C . 重水、水
D . 金刚石、石墨
填写下列各组物质之间的关系(填编号字母):
A.同种物质 B.同位素 C.同系物 D.同素异形体 E.同分异构体
-
(1) 正丁烷和异丁烷,
-
(2) 红磷和白磷,
-
(3) 甲烷和乙烷,
-
(4) 氕、氘、氚.
小科利用12种元素制作了一张如图所示的“元素钟面”。

-
(1) 钟面上的这些元素之间最根本的区别是不同。
-
(2) 小科根据钟面上提供的元素,写出了下列三种物质的化学作式:O2、MgO和NaNO3 , 其中属于氧化物的是 。
-
(3) 此刻钟面上的时针、分针和秒针分别指向三种不同元素,请写出由这三种元素组成的化合物(用化学式表示)。
经实验测得某一溶液由Na+、Mg2+、Cl-、 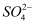 四种离子组成,其中含有4.6克Na+、14.4克
四种离子组成,其中含有4.6克Na+、14.4克 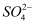 、14.2克Cl- , 则Mg2+质量为( )
、14.2克Cl- , 则Mg2+质量为( )
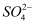 四种离子组成,其中含有4.6克Na+、14.4克
四种离子组成,其中含有4.6克Na+、14.4克 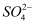 、14.2克Cl- , 则Mg2+质量为( )
、14.2克Cl- , 则Mg2+质量为( )
A . 2.4克
B . 5克
C . 6克
D . 4.8克
核电站使用铀作燃料发电,铀的相对原子质量为238,质子数为92,则铀原子的核外电子数为( )
A . 238
B . 146
C . 136
D . 92
下表是小明收集的一些微粒的资料,请根据表格数据,回答下列问题。
|
粒子名称 |
质子数 |
中子数 |
电子数 |
|
A |
14 |
14 |
14 |
|
B |
26 |
30 |
24 |
|
C |
14 |
14 |
18 |
|
D |
14 |
18 |
14 |
-
(1) B微粒所带的电性为。(填“不带电”、“带正电”或“带负电”)
-
(2) 与A互为同位素原子的是。
在原子中,核电荷数==。原子核和核外电子所带的电量大小相等,电性相反,因而原子呈电。
美国科学家合成了含有N5+的盐类,含有该离子的盐是高能爆炸物质,该离子的结构呈V 形,如图所示。下列有关说法中正确的是( )

A . 每个N5+中含有35个质子和36个电子
B . N5+是一种单质
C . 含有N5+的盐类是纯净物
D . 每个N5+带一个单位负电荷
了解物理规律的发现过程,学会像科学家那样观察和思考,往往比掌握知识本身更重要。下列描述与事实不相符的是( )
A . 汤姆生发现了比原子小的多的电子
B . 法拉第发现了电流周围存在磁场
C . 卢瑟福提出原子核式结构模型
D . 拉瓦锡通过实验测定了空气中氧气的大致含量
与碳元素一样,氢元素也有三种不同的原子,依次称为氕[piē]、氘[dāo]、氚[chuān],分别用符号 H、D、T 表示,其原子核内质子数均为 1,中子数依次为 0、1、2.下列有关说法不正确的是( )
A . 氕、氘、氚三种原子核外均只有一个电子
B . 一个氘原子的质量约为一个氕原子质量的 2 倍
C . 氕、氘、氚三种原子的化学性质几乎完全相同
D . 化学式为 HD 的物质属于化合物
模型常常可以帮助人们认识和理解一些不能直接观察到的或复杂的事物。下列模型的建构中,说法错误的是( )

A . 图甲能表明钠在氯气中燃烧的电子得失
B . 在图乙实验的基础上,卢瑟福提出了原子的核式结构模型
C . 图丙是氢的3种同位素,其核内的质子数和中子数都相同
D . 图丁可以表示地壳中所含各种元素的分布情况
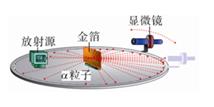
探究原子结构的奥秘。
收集证据:绝大多数α粒子(带+电)穿过金箔后仍沿原来的方向前进,但是有少数α粒子却发生了较大的偏转,并且有极少数α粒子的偏转超过90°,有的甚至几乎达到180°,像是被金箔弹了回来。猜想与假设:α粒子遇到电子后,就像飞行的子弹碰到灰尘一样运动方向不会发生明显的改变,而结果却出乎意料,除非原子的大部分质量集中到了一个很小的结构上,否则大角度的散射是不可能的。解释与结论:
-
(1) 若原子质量、正电荷在原子内均匀分布,则α粒子就(填“会”或“不会”)发生大角度散射。卢瑟福所说的“除非原子的大部分质量集中到了一个很小的结构上”中的“很小的结构”指的是。
-
(2) 1微米金箔包含了3000层金原子,绝大多数α粒子穿过后方向不变,说明 。A . 原子的质量是均匀分布的 B . 原子内部绝大部分空间是空的
-
(3) 1919年,卢瑟福用加速了的高能α粒子轰击氮原子,结果有种微粒从氮原子被打出,而α粒子留在了氮原子中,使氮原子变成了氧原子,从现代观点看,被打出的微粒一定是。
氧气分子和水分子中都含有氧原子,它们统称为氧元素。这是因为不管在氧气分子中,还是在水分子中,这些氧原子都具有相同的( )
A . 核外电子数
B . 核内质子数
C . 核内中子数
D . 相对原子质量
下列说法中的先后顺序,不符合科学史实的是( )
A . 对细胞的认识:先提出动植物都是由细胞构成的,后提出一切细胞来自于细胞
B . 对电磁现象的认识:先有电流磁效应的发现,后有电磁铁的应用
C . 对原子结构的认识:先发现原子中有原子核,后发现原子中有电子
D . 对海陆变迁的认识:先提出大陆漂移学说,后建立板块构造学说
科学研究中。人们通过一定的科学方法,建立一个适当的模型来代替和反映客观对象,并通过的这个级型来揭示客观对象的形态、特征和本质。下列分析正确的是( )


A . ①揭示单侧光对生长素分布的影响,向光侧生长素多,生长快
B . ②用磁感线描述条形磁体周围的磁场分布,越密表示磁场越弱
C . ③是原子结构模型,中央是原子核,核外是绕核高速运动的电子
D . ④描述地球绕日公转,地轴始终是倾斜状态,箭头表示公转方向
“加碘食盐”、“高钙牛奶”、“补铁酱油”中的“碘”“钙”“铁”指的是( )
A . 元素
B . 原子
C . 离子
D . 分子
HCl气体通人水中可得到盐酸,室温下,将HCl气体通入盛有NaOH溶液的试管中,直至溶液的pH=7。回答问题:

-
(1)
 和
和 的中子个数相差个。
的中子个数相差个。
-
(2) HCl气体通人NaOH溶液前后,试管中溶液的离子种类如图所示,其中能使无色酚酞试液变红的是(选填“①”“②”或“③”)
最近更新



