第2节 金属矿物 铁的冶炼 知识点题库
-
(1) 下列汽车组件中,由有机合成材料制成的是 (填序号)A . 钢铁车架 B . 真皮座套 C . 玻璃车窗 D . 橡胶轮胎
-
(2) 钢铁车壳表面喷漆不仅美观,而且可有效防止与空气中的(填两种物质名称)接触而生锈.
-
(3) 汽车制造需要钢铁,工业上的用赤铁矿(主要成分为氧化铁)与一氧化碳来炼铁的化学方程式为,该反应中(填化学式)发生了还原反应.
(1)证明碳具有还原性的实验现象是 , .
(2)CuO发生 反应(填“氧化”或“还原”).
(3)酒精灯加上网罩的作用是 .

-
(1) 写出工业上以赤铁矿为原料炼铁的原理:;
-
(2) 我国在金属的冶炼方面有着悠久的历史,早在南北朝就能冶铸黄铜.铜冶铸成黄铜,其熔点比纯铜;黄铜是由铜和锌组成的,如果根据化学方法除去黄铜中的锌,有关的化学方程式.
-
(3) 农药波尔多液的成分之一是硫酸铜,不能用铁桶盛放波尔多液的原因是.(用化学方程式表示)
-
(4) 铝比铁具有抗腐蚀性的原因是.
-
(1) 写出下列物质的化学式:氢氧化铜,氧化亚铜
-
(2) 高温时,氧化铜可被木炭还原为铜,反应的化学方程式是
-
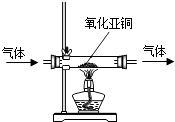
(3) 氧化亚铜是一种红色粉末.加热时,氧化亚铜能与氧气发生化合反应,反应的化学方程式是;利用这一性质可检验氮气中是否含有氧气(装置如图所示),判断氮中含有氧气的现象是.

请回答下列问题:
-
(1) 上述实验过程中发生反应的化学方程式为;
-
(2) 样品中单质铁的质量分数为;
-
(3) 根据已知条件列出求解加入的稀硫酸中溶质质量(x)的比例式为;
-
(4) 最终所得到的不饱和溶液中溶质的质量分数为;
-
(5) 若用含氧化铁80%的赤铁矿炼出上述实验中所需要的铁合金160t,则理论上需要赤铁矿的质量为.
-
(1) 【提出猜想】根据反应物和生成物性质猜想黑色固体成分
甲同学猜想:氧化铜;乙同学猜想:碳;丙同学猜想:。
-
(2) 甲同学猜想的理由是:。
-
(3) 【查阅资料】氧化铜在空气中不燃烧
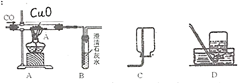
【设计实验】乙同学为了验证自己的猜想,设计实验如图所示,取黑色固体放入试管中加强热,若观察到澄清石灰水变白色浑浊,即可以得出自己猜想的正确的结论。请你对乙同学的结论做出评价。
-
(4) 【进行实验】丙同学按照乙同学的实验设计进行了实验,观察到的现象是。证明自己的猜想正确,写出黑色固体发生反应的化学方程式。
-
(5) 【反思与总结】根据上述实验探究内容,我们可以总结出在根据实验产生的现象验证物质成分时,需要注意,才能准确得出结论。
-
(1) 为避免一氧化碳污染空气并回收利用一氧化碳,B装置应连接C、D哪个装置?
-
(2) 实验进行一段时间后,玻璃管A中出现的现象有什么?写出该反应化学方程式
-
(3) 在这个反应里,如何体现还原反应的概念?请说明
-
(1) 利用如图装置可进行气体性质的探究实验(导管a处用火柴点燃)

Ⅰ.探究CO与CuO的反应:通入气体一氧化碳,M处为氧化铜,加热前先通一氧化碳的目的是;M处反应的化学方程式为;澄清石灰水的作用是。
Ⅱ.探究CO2与C的反应(改为酒精喷灯):通入气体二氧化碳,M处为木炭,观察到玻璃管中的现象是,M处反应的化学方程式为。导管a处点燃的目的是。
-
(2) 化学小组取一定量碳酸钙固体高温煅烧一段时间,冷却后,对剩余固体成分进行如下探究。
(提出问题)剩余固体成分是什么?
(猜想与假设)
猜想一:。
猜想二:是氧化钙与碳酸钙的混合物。
(实验探究)
实验步骤
实验现象
步骤1
取一定量的剩余固体于试管中,加入一定量的水,振荡、静置。取上层清液,滴加无色酚酞试液。
步骤2
另取一定量的剩余固体于试管中,加入足量。
有气泡产生
(探究结论)通过探究,猜想二成立。

-
(1) 根据上述资料,可以推理得出钨金属的性质是_____(填编号);A . 硬度大 B . 熔点高 C . 常温下不易与氧气反应 D . 能与硫酸亚铁溶液发生置换反应
-
(2) H2WO4的名称是,它是一种不溶于水的黄色固体;
-
(3) 上图所示金属钨的生产过程涉及的主要化学反应如下:
步骤①:

步骤②:把Na2WO4 溶液(无色)加入热的浓盐酸中,发生了复分解反应,则反应的化学方程式是,该反应中可能观察到的现象是;
步骤③:
 ;
;步骤④:该反应的化学方程式是;
-
(4) 若工厂在生产过程中消耗了168吨含钨酸亚铁75%的黑钨矿石,则理论上需要消耗氢气的质量为吨(保留一位小数)。
-
(1) 电解水过程加入硫酸钠或氢氧化钠的目的;
-
(2) 在CO还原氧化铜这个实验中,实验结束时,先停止加热再停止通入CO的目的;
-
(3) 生活中降低水硬度的方法:。
-
(1) 认识铁:从宏观看,铁由组成:从微观看,铁由构成。
-
(2) 生活中:如图是常用的铁锅。把铁制成铁锅利用了铁的延展性和性,防止铁制品锈蚀,可采用的一种防锈方法是。
-
(3) 实验室:细铁丝在氧气中燃烧的现象是:火星四射、放热、,该反应的化学方程式是。
-
(4) 工业上:用一氧化碳和赤铁矿(主要成分是Fe2O3)炼铁的化学方程式是;过高炉炼得的铁是(填“纯铁”或“生铁”)。

-
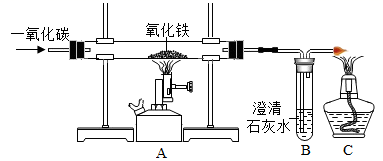
(1) A处可观察到, 说明CO气体具有。
-
(2) B处石灰水变浑浊说明有生成。
-
(3) C处可观察到。说明CO气体具有。
-
(4) 写出A、C处化学变化的化学表达式:A处:;C处:。

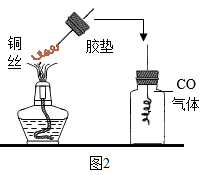
请回答以下有关问题
-
(1) 实验开始时,先通入CO一段时间,然后再加热,其原因是。
-
(2) 该实验中,能证明CO具有还原性的实验现象。
-
(3) 装置B的试管中,发生反应的化学反应方程式为。
-
(4) 经过思考,小明同学改进了实验(如图2所示)。请参与完成下列实验探究:
步骤
实验操作
实验现象
结论或解释
①
将插入胶塞的一根光亮的红色铜丝绕成螺旋状,在酒精灯的火焰上灼烧一段时间。
铜丝表面变成黑色
发生反应的化学方程式为:。
②
再次灼烧铜丝至红热,趁热将铜丝迅速伸入盛有CO气体的集气瓶中,塞紧胶塞。
铜丝表面由黑色变为。
发生反应的化学方程式为:。
-
(5) 对比原实验,改进后的实验具有的优点是。
-
(1) 下列生活用品,属于金属材料制品的是(填字母)。
A 塑料水杯 B 大理石砖 C 不锈钢盆
-
(2) 工业上用赤铁矿(主要成分Fe2O3)冶炼生铁的化学方程式为。
-
(3) 防止铁制栏杆生锈的方法之一是。
-
(4) 路边的太阳能路灯灯柱为铝合金材质,因为铝合金的比纯铝大。
图1  图2
图2 
①两个实验中都可观察到黑色固体变红,澄清石灰水变浑浊;
②两个实验都可以根石灰水不冒气泡的现象判断反应已经结束
③两个实验均应防止石灰水倒吸
④两个实验发生的反应中,C、CO都得到氧,发生还原反应;
⑤两个实验的相关反应中,C、Cu、O三种元素的化合价都发生改变;
⑥两个实验中固体减少的质量均为产生气体的质量
⑦两个实验中铜元素在固体中的质量分数逐渐变大;
⑧图1中,若取氧化铜样品质量为m,充分反应后,玻璃管内的固体质量减少了n,则样品中氧化铜的质量分数为  ×100%(杂质不参加反应),澄清石灰水增加的质量为
×100%(杂质不参加反应),澄清石灰水增加的质量为  。
。
-
(1) 从宏观看,铁由组成:从微观看,铁由构成。
-
(2) 硫酸铜溶液不能用铁制容器盛放的原因是(用化学方程式表示)。
-
(3) 工业上用一氧化碳和赤铁矿(主要成分是Fe2O3)炼铁的化学方程式是,该反应利用了一氧化碳的哪种化学性质:。某钢铁厂每天需消耗4800t含Fe2O3 76%的赤铁矿石,该厂理论上可日产含Fe 96%的生铁的质量是t。
-
(4) 实验室探究铁、铜的金属活动性顺序,除铁、铜外,还需要的一种试剂可以是____。A . 稀盐酸 B . FeSO4溶液 C . CuSO4溶液 D . Al2(SO4)2溶液
-
(5) 某化学兴趣小组进行铁锈蚀条件的探究实验。实验中通过对比(填序号)。试管中的现象,证明铁生锈需要氧气。为了防止钢铁锈蚀,通常采用的方法是在其表面涂刷矿物油或镀上其它金属形成覆盖保护膜,这些方法能防止锈蚀的原理是:。


-
(1) 一氧化碳与氧化铁反应的化学方程式为。
-
(2) 实验时需进行尾气处理的原因是。



