第六单元 常用的金属和盐 知识点题库
某化学反应的微观示意图如下。下列说法正确的是( )

A . 该反应属于复分解反应
B . 生成物都是氧化物
C . 参加反应的甲和乙的分子个数比为1:1
D . 该变化体现了无机物到有机物的转化
下列操作可以达到实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 检验甲烷中是否含有氢气 | 将气体点燃 |
| B | 鉴别碳粉、铁粉和氧化铜粉末 | 取样后,分别加入稀盐酸 |
| C | 除去氯化锌溶液中少量的氯化铜 | 加入足量铁粉 |
| D | 分离KClO3和KCl | 溶解、过滤、洗涤固体并烘干 |
A . A
B . B
C . C
D . D
向一定质量的CuSO4溶液中滴加KOH溶液一段时间后,改为滴加稀盐酸,所得沉淀质量随加入试剂总体积的变化趋势如图所示。下列有关说法错误的是( )

A . 加入试剂总体积为V1时,溶液中不存在KOH
B . b点时所加试剂一定是稀盐酸
C . c点时溶液中的溶质都是盐
D . a点时溶液中一定不存在Cu2+
-
(1) 观察下图中氮元素的化合价与其所组成的物质类别的关系,回答下列问题:

①甲在空气中的体积分数为,乙的化学式;丙的化学式为HNO3 , 该物质的名称是。
②若丁是工业用盐NaNO2 , 能区别NaNO2溶液与食盐溶液的一种试剂是。(友情提示:NaNO2有毒,有咸味,外形与食盐相似,其水溶液呈碱性。)
③氮元素的化合价也可以为-3价,写出
 形成一种化肥的化学式。
形成一种化肥的化学式。 -
(2) 将炉甘石(ZnCO3)、赤铜(Cu2O)和木炭粉混合加热到约800℃,可得到铜锌合金,其中发生的置换反应有个。该合金外观酷似黄金,下列试剂中,能鉴别该合金和黄金的是填字母序号)。
A、NaCl溶液
B、AgNO3溶液
C、稀盐酸
下列生活中的说法和做法错误的是( )
| | | | |
| A.用涂油的方法防止自行车链条锈蚀 | B.农业上用一定浓度的氯化钠溶液选种 | C.养鱼池将水喷向空中,可增加鱼池水中氧气的溶解度 | D.炒菜时油锅中油不慎着火,可用锅盖盖灭 |
A . A
B . B
C . C
D . D
推理是化学学习中常用的思维方法。下列推理正确的是( )
A . 点燃可燃性气体前要验纯,所以点燃H2前一定要验纯
B . 离子是带电的粒子,所以带电的粒子一定是离子
C . H2O和H2O2的元素组成相同,所以它们的化学性质相同
D . 置换反应有单质生成,所以有单质生成的反应一定是置换反应
取硫酸铜和硫酸钠混合物8.9g,向其中加入100g溶质质量分数为4%的氢氧化钠溶液,恰好完全反应。计算:
-
(1) 样品中硫酸铜的质量;
-
(2) 反应中生成的沉淀的质量;
-
(3) 反应后溶液中溶质的质量分数(计算结果精确至0.1%)。
如图中大写字母分别代表初中化学常见的几种物质。

-
(1) 物质D的化学式为,反应③是高炉炼铁的原理之一,写出反应③的化学方程式,该反应说明物质 E具有性,实验室在进行此操作时,要对尾气进行处理,以免污染空气。
-
(2) 化学反应④在反应前后溶液的质量(填"增加"或"减少")。
某小组利用如图装置进行创新实验。实验时,先加热炭粉,一段时间后将酒精灯移至CuO处加热。下列说法错误的是( )

A . 酒精灯加网罩是为了提高火焰温度
B . 气球可以收集尾气,防止污染空气
C . 反应过程中,黑色氧化铜变为红色固体
D . 装置中发生反应: 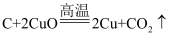
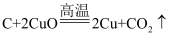
厨房中使用的食用碱(主要成分为碳酸钠)中往往含有少量的氯化钠,某化学兴趣小组同学通过实验来测定某品牌食用碱样品中碳酸钠的含量。实验过程和数据如下图所示:

请计算:
-
(1) 6g该食用碱样品中碳酸钠的质量是多少?
-
(2) 所得滤液中溶质的质量分数是多少?
-
(1) 写出下列符号或示意图中数字“2”的含义
2H: ;Mg2+
-
(2) 地壳中含量最高的金属与空气中含量排第二位的物质反应的生成物化学式为,苏打(碳酸钠)的化学式为
-
(3) 硝酸(HNO3)是高中化学将要学习的一种常见物质,硝酸中氮元素的化合价为价,浓硝酸见光会发生分解反应,生成红棕色的NO2气体和一种常见液体以及能供给呼吸的气体,写出该反应的化学方程式
-
(4) 甲、乙、丙是初中化学常见的三种物质,其相互转化关系如图,通常甲为固态单质,乙、丙为两种气体,且所含元素种类相同,乙易与血液中的血红蛋白结合。

写出③、④转化的化学方程式:③;④
-
(5) 在天平(灵敏度极高)两边的烧杯中分别盛有等质量的足量的稀硫酸,天平平衡,再向两烧杯中分别加入相同质量的镁(左盘)和铁(右盘),充分反应后,天平,(填平衡或不平衡)。如果不平衡,指针偏向(填左或右)。
实验室里区分下列物质的两个实验设计方案都合理的是( )
| 选项 | A | B | C | D |
| 区分的物质 | 空气和人呼出气体 | 食盐水和水 | 铁丝和铜丝 | 白酒和白醋 |
| 第一方案 | 取样,观察颜色 | 取样,蒸干 | 观察颜色 | 观察颜色 |
| 第二方案 | 将带火星的木条,分别伸入待测气体中,观察现象. | 取样,观察状态 | 用磁体吸引 | 取样,闻气味 |
A . A
B . B
C . C
D . D
为测定某铁粉样品(含少量木炭粉)中铁的含量,往盛有一定量稀盐酸的烧杯中不断加入铁粉样品,测得生成氢气质量与所加铁粉样品质量的关系如图所示。

-
(1) 稀盐酸恰好完全反应时,生成氢气的质量为g。
-
(2) 求该铁粉样品中铁的质量分数(写出计算过程,结果保留1位小数)
A~E是初中化学常见的物质,其中A和B是黑色固体、且A是单质,D和E是组成元素相同的气态氧化物,它们之间的转化关系如图所示。请回答下列问题:

-
(1) A的化学式为。
-
(2) E的一种用途是。
-
(3) 反应③属于基本反应类型。
-
(4) 反应①的化学方程式为。
等质量、等浓度的稀硫酸分别与足量的镁、锌两种金属反应,下列图像能正确表示产生氢气质量与反应时间之间关系的是( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
下列关于化肥和农药的说法正确的是( )
A . 农药施用后,会通过农作物、农产品等发生转移
B . 农药本身有毒,应该禁止施用农药
C . 当农作物易倒伏、易被病虫侵害时,可施用 CO(NH2)2
D . 硝酸铵(NH4 NO3)能与碱性物质混合施用
化学就在我们身边。下列说法正确的是( )
A . 霉变的大米、花生经蒸煮后可继续食用
B . pH小于5.6的降雨称为酸雨
C . 硝酸钾、草木灰(主要成分为碳酸钾)都是复合肥
D . 炒菜时油锅起火可放入菜叶灭火,原理是降低了油的着火点
钢铁是应用最普遍的金属材料,也是最容易发生锈蚀的金属材料之一、人类为金属的锈蚀付出了巨大的代价,所以金属的防腐和废旧金属的回收有着十分重要的意义。
-
(1) 工业上用赤铁矿(主要成分Fe2O3)炼铁的原理:(用化学方程式表示)。
-
(2) 钢铁生锈是铁与空气中发生化学反应的结果。
-
(3) 处理某废旧金属后的溶液中含有Cu(NO3)2和AgNO3两种溶质,为回收其中的金属,向该溶液中加入一定量的铁粉,充分反应后过滤,再向滤渣中加入稀盐酸,无气泡产生。则滤液中一定含有的金属离子是;滤渣中可能含有。
明代宋应星所著的《天工开物》中有煅烧炉甘石(ZnCO3)和煤炭(C)炼锌的记载,其化学反应原理为: 。某化学兴趣小组在实验室用ZnCO3和C模拟古法炼锌。实验结束后,同学们设计实验对2.0g粗锌产品中含有的杂质进行探究并测定粗锌中单质锌的含量。实验装置设计如下(忽略其它因素对结果的影响):
。某化学兴趣小组在实验室用ZnCO3和C模拟古法炼锌。实验结束后,同学们设计实验对2.0g粗锌产品中含有的杂质进行探究并测定粗锌中单质锌的含量。实验装置设计如下(忽略其它因素对结果的影响):
 。某化学兴趣小组在实验室用ZnCO3和C模拟古法炼锌。实验结束后,同学们设计实验对2.0g粗锌产品中含有的杂质进行探究并测定粗锌中单质锌的含量。实验装置设计如下(忽略其它因素对结果的影响):
。某化学兴趣小组在实验室用ZnCO3和C模拟古法炼锌。实验结束后,同学们设计实验对2.0g粗锌产品中含有的杂质进行探究并测定粗锌中单质锌的含量。实验装置设计如下(忽略其它因素对结果的影响):

回答下列问题:
-
(1) 如图连接好装置后,装入药品前,首先应进行的操作是。
-
(2) A装置试管中加入足量稀硫酸充分反应后,仍有少量黑色固体剩余,说明粗锌中一定含有。
-
(3) B装置中澄清石灰水变浑浊,此时B装置中发生反应的化学方程式为,B装置的作用是。
-
(4) 综合以上实验现象可知,粗锌含有的杂质有。
-
(5) C装置收集的气体为;实验结束后,若D处一共收集到200.0mL液体,则2.0g粗锌中含有单质锌的质量为g。(已知此温度下C装置收集的气体的密度ρ≈0.1g/L)
鉴别、除杂是重要的实验技能。下列实验设计能达到实验目的的是( )
选项 | 实验目的 | 实验设计 |
A | 去除铁粉中的碳粉 | 在足量的氧气中灼烧 |
B | 比较铜和银的金属活动性强弱 | 分别向盛有铜和银的试管中加入稀盐酸 |
C | 鉴别硫酸铵和硫酸钾固体 | 分别与少量熟石灰混合后,研磨,闻气味 |
D | 检验久置的NaOH是否变质 | 取样,滴加酚酞溶液 |
A . A
B . B
C . C
D . D
最近更新







