第三节 水分子的变化 知识点题库
流程一:从只含有CuSO4的废液中回收金属铜,并得到工业原料硫酸亚铁,生产流程如图2所示: 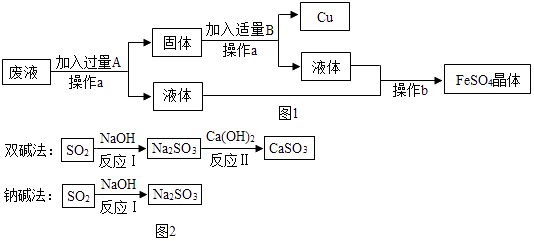
-
(1) 加入过量的A物质,该A物质为.操作a的名称是,操作a所用到的玻璃仪器有烧杯、玻璃棒,操作a中玻璃棒的作用是.
-
(2) 写出流程图中的固体成分的化学式,B的溶液中溶质的化学式
-
(3) 流程二:如图2是两种常用脱硫工艺中含硫物质的转化路径(部分产物已略),请回答下列问题:
①CaSO3中Ca、S、O元素的质量比是.
②已知原料NaOH的价格为2.9元/kg.而Ca(OH)2的价格为0.36元/kg.两种工艺中,处理相同质量的SO2 , 双碱法所需的原料成本更低,其原因是.
-
(1) 甲同学将固体氢氧化钠放入装有稀盐酸的试管中并振荡,试管壁发烫,于是他得出酸碱中和反应是放热反应的结论.乙同学认为甲同学推理不合理,理由是.
-
(2) 乙同学为了验证甲同学的结论,将实验加以改进:将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出氢氧化钠溶液温度随加入稀盐酸质量的变化如下图:

①由图知,稀盐酸与氢氧化钠溶液发生的反应是(填“放热”或“吸热”)反应.
②逐渐滴加稀盐酸的过程中,烧杯中溶液pH逐渐.
③稀盐酸加过量时,溶液中的溶质有.
-
(3) 丙同学将稀盐酸滴入氢氧化钠溶液中,有气泡产生,他认为氢氧化钠溶液已变质.请你分析变质的原因(用化学方程式表示).
已知:A中发生的反应为:H2SO4(浓)+Na2SO3═Na2SO4+SO2↑+H2O
B中发生的反应为:Na2SO3+SO2═Na2S2O5

-
(1) 图中盛放浓硫酸的仪器名称是;
-
(2) 写出C中发生反应的化学方程式;
-
(3) 在实验过程中,滴加浓硫酸不宜过快,理由是.
-
(4) 该实验开始滴加浓硫酸时,应先除尽装置内的空气,若忘记这一操作,新制取的Na2S2O5产品中会混有Na2SO4杂质,这与O2的有关(填化学性质)

-
(1) 下列措施符合我国“世界环境日”主题的是 . (填字母)A . 限制发展高耗能的产业 B . 推广使用“乙醇汽油”,减少有害气体排放 C . 为了减少废气对本地区空气的污染,化工厂加高烟囱 D . 将污染严重的工厂迁到农村去
-
(2) 天然气的主要成分是(填名称),其完全燃烧的化学方程式为.
-
(3) 图中的信息告诫人类:二氧化碳等气体过多的排放,使加剧,导致全球变暖.为减少二氧化碳过多的排放对环境的影响,你能做的一件事;科学家采取“组分转化”技术,将二氧化碳和氢气以一定比例混和,在一定条件下反应,生成一种重要的化工原料乙烯(C2H4)和水.该反应的化学方程式为.
-
(4) 为解决能源短缺和环境污染的问题,目前有待开发、利用的新能源有.(写一种)
-
(5) “绿箱子环保计划﹣﹣废弃手机及配件回收联合行动”已在全国许多重点城市中相继开展,废弃手机中的金属材料回收利用的意义,你认为有(举出一个方面)
①NaOH+NH4NO3 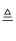 NaNO3+NH3↑+H2O
NaNO3+NH3↑+H2O
②Ca(OH)2+2NH4Cl 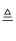 CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O
③2KOH+(NH4)2SO4 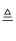 K2SO4+2NH3↑+2H2O
K2SO4+2NH3↑+2H2O
-
(1) 碱与铵盐反应的规律是都生成盐、水和;由此可知铵态氮肥使用时的一点注意事项是.
-
(2) 选用一种溶液分别加入到K2CO3、(NH4)2SO4、NH4Cl三种物质的溶液样品中并微热,就可以将它们鉴别开,所选溶液中溶质的化学式为.

请回答:
-
(1) 若A在常温下为固体,则反应①的化学方程式为,下图所示的仪器中,可用作该反应发生装置的是(填字母);若A 在常温下为液体,则A的化学式为,反应①的基本反应类型是。

-
(2) 在金属活动性顺序中,B位于铁的(填“前面”或“后面”)。若要证明,所需试剂有:B的单质、铁的单质和(只填一种)。
-
(3) G的化学式为,它不具有的性质有(填字母)。
A.酸性 B.还原性 C.毒性 D. 助燃性
-
(4) 反应②的化学方程式为。
-
(1) 工业常用氯化镁溶液与烧碱溶液制取Mg(OH)2 , 化学方程式是。
-
(2) 某同学用氨水在实验室模拟制取Mg(OH)2的过程:一定温度下,往含一定量氯化镁的溶液中加入适量氨水(氨水易挥发),再经过滤、洗涤得到Mg(OH)2晶体。为探究获得较高Mg(OH)2晶体转化率条件,该同学进行如下对比实验,数据如下:
实验编号
氯化镁溶液溶质质量分数
反应温度/℃
Mg(OH)2转化率/%
a
10%
30
27.06
b
15%
30
56.77
c
15%
40
69.64
d
15%
60
54.30
e
20%
60
50.60
①实验b和c的目的是。
②由实验可知,能够得到最多Mg(OH)2的条件是溶质质量分数和温度℃。
③在氯化镁溶液溶质质量分数都是40%的情况下,60℃时Mg(OH)2的转化率比40℃时低的原因是。
-
(3) 根据燃烧的条件可知,Mg(OH)2能做阻燃剂的原因是 (填编号)。
①清除可燃物 ②使温度降低到着火点以下 ③隔绝空气
-
(1) 写出一个生成白色沉淀的化学方程式 ;
-
(2) 取废液少许,测得其pH为12.则废液显性;
-
(3) 废液中除一定含有OHˉ外,有三种离子在任何条件下都会存在,它们是;
-
(4) 另取废液少量于试管中,加入Na2CO3溶液,看到有白色沉淀生成,则废液中一定没有离子。
![]()
-
(1) 实验室常用①②③三个原理制取氧气,需要加热条件的是(填序号,后同),反应中用到催化剂的是。
-
(2) 写出反应①③的文字表达式:
①:
③。
-
(3) 上述三个反应都属于反应(填基本反应类型)。

-
(1) 左图中海水属于(填“纯净物”或“混合物”),海水含有大量氯化钠,氯化钠溶液俗称食盐水,食盐水中的阳离子是(填离子符号);
-
(2) 右图试管B中气体的化学式为,试管A所对应的电源是 (填“正”或“负”)极;
-
(3) 在水蒸发的过程中,下列说法正确的是 (填字母序号,下同):A . 水分子不断运动 B . 水分子之间间隔不变 C . 水分子大小不发生变化 D . 水分子可以保持水的物理性质
-
(4) 在电解水的过程中,下列说法正确的是( ) 。A . 水分子本身发生了改变 B . 氢原子和氧原子数目没有发生变化 C . 氢原子和氧原子种类发生了改变 D . 氢原子和氧原子质量发生了变化
-
(1) 请选择下列合适物质的序号填入空格内:
A 氮气 B 氧气 C 稀有气体 D 二氧化碳
①能使带火星的木条复燃的气体是;
②可导致温室效应的气体是;
③可制作多种电光源的气体是;
④可制氮肥的气体是。
-
(2) 在 ①红磷 ②二氧化硫 ③高锰酸钾 ④食盐水 ⑤ 液氮 ⑥ 过氧化氢溶液 ⑦银白色的细铁丝;这些物质中属于混合物的是;属于纯净物的是。(填序号)
-
(3) 观察、比较与归纳是学习化学的重要方法。对于以下三个反应的表达式:
①氢气+氧气
 水 ②镁+氧气
水 ②镁+氧气  氧化镁 ③木炭+氧气
氧化镁 ③木炭+氧气  二氧化碳
二氧化碳①通过比较,发现它们有许多共同点,请你写出其中两点:
A.;
B.。
-
(1) 天然水中含有许多杂质,实验室常用过滤方法除去水中不溶性杂质,过滤需要用到的仪器有带铁圈的铁架台、烧杯、玻璃棒和(填仪器名称),得到的滤液是物(填“纯净”或“混合”)。
-
(2) 可用于区别硬水和软水的是,实验室用的蒸馏水是净化程度较高的水,可以通过自来水制取。不论是自来水还是纯净水,保持水化学性质的最小粒子是。
-
(3) 下列是两个关于水的实验。
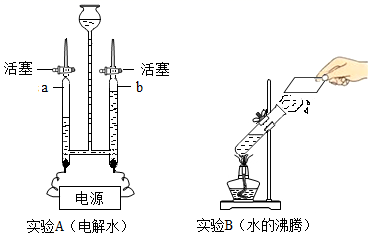
①实验A,两电极相连的玻璃管上方产生的气体a是(填名称),反应的化学方程式为。
②能确定水是由氢元素和氧元素组成的实验是(填序号)。

A.实验过程中,

-
(1) 根据图中电解水装置回答:试管a中产生的气体是气,a与b中气体的体积比为。
-
(2) 电解水的文字表达式:,它属于反应 。
 氧化铜+二氧化碳+水
B . 镁+氧气
氧化铜+二氧化碳+水
B . 镁+氧气  氧化镁
C . 石蜡+氧气
氧化镁
C . 石蜡+氧气  二氧化碳+水
D . 铁+氧气
二氧化碳+水
D . 铁+氧气  四氧化三铁
四氧化三铁

-
(1) 电解水时,负极上产生的气体a是。
-
(2) 电解水反应的文字表达式(或符号表达式)。
-
(3) 该实验说明水是由组成的。
A.铁丝在氧气中燃烧
B.测定空气中氧气含量
C.探究燃烧的条件
D.探究二氧化碳的性质
-
(1) 实验A中反应现象为,水的作用是。
-
(2) 实验B中量筒中水的作用是,实验中若装置未冷却就打开止水夹对测定结果的影响是(选填“偏大”、“偏小”、“无影响”)。
-
(3) 实验C中热水的作用是提供热量和。
-
(4) 实验D中水的作用是和。



