课题3 制取氧气 知识点题库
现有实验室制取气体的部分装置,请结合所学化学知识,回答有关问题。

-
(1) 写出图中②标示的仪器名称.
-
(2) 若用A装置制取氧气,写出A中发生反应的化学方程式,通过排水量测定所收集到的氧气体积,则可用装置选用A. F. G,且各装置的管口连接顺序是:a−b−c−d,则F装置图内导管b和c的长短情况是 (填“b长c短”或“c长b短”)如实验过程发现F瓶中的水变红了,则在A装置组装时出现的错误是.
-
(3) 若选用A.E装置制取氧气,主要操作步骤有①加入药品②加热③检验装置的气密性 ④收集气体⑤停止加热⑥将导管移出水面,正确的顺序是 (写序号).
-
(4) 用收集到的氧气做细铁丝燃烧的实验时,发现瓶底炸裂,发生失误的操作原因可能是.
-
(5) 实验室需少量甲烷气体,可用加热无水醋酸钠与碱石灰的固体混合物制得。制甲烷气体的发生装置应选用 (填字母)装置;收集甲烧气可选用D或E装置,由此推断甲烷气具有的物理性质是.
根据下图装置回答实验室制取氧气及氧气性质的相关问题。

-
(1) 用高锰酸钾制氧气,反应的化学方程式为。
-
(2) 用向上排空气法收集氧气,验满的操作是。
-
(3) B中观察到木炭剧烈燃烧,发出白光,说明氧气具有的性质是。
如图所示装置,结合所学化学知识回答下列问题:
学习材料:氨气(NH3)是一种具有刺激性气味的无色气体,密度比空气小,极易溶于水。氨气能使湿润的红色石蕊试纸变蓝色。实验室可用加热氯化铵和熟石灰两种固体的方法制取氨气[2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O]。
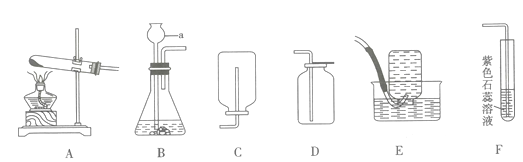
-
(1) 写出仪器a的名称:。
-
(2) 实验室用高锰酸钾制取氧气时,选择的发生装置是(填字母序号,下同),收集装置是。
-
(3) 实验室制备二氧化碳可选用的发生装置是,发生反应的化学方程式为。
-
(4) 将二氧化碳通人F装置会观察到的实验现象是。
-
(5) 检验氨气是否收集满的方法是。
请从A或B两题中任选一个作答,若两题均作答,按A计分。

A | B |
实验室用高锰酸钾制取氧气的化学方程式是。 用装置A、E制取氧气应该等到时再收集。 | ⑴实验室制取二氧化碳的化学方程式是。 ⑵通常用装置C收集二氧化碳的理由是 。 |
请根据下列装置,回答问题:

-
(1) 写出标号①②的仪器名称:①,②。
-
(2) 实验室用过氧化氢制取氧气,可选用装置(填写装置序号)能收集到较纯净的氧气,实验结束后回收二氧化锰的正确操作顺序是填写选项序号)
a.烘干
b.溶解
c.过滤
d.洗涤
-
(3) 检验收集的气体是氧气的方法。
-
(4) 用高锰酸钾制取O2 , 装置A还需做的一点改动是。
-
(5) 用装置F制取气体,在反应过程中,用弹簧夹夹住导气管上的橡皮管,过一会儿反应就会停止。其原因是。
实验室中用如图装置制取氧气。

-
(1) 高锰酸钾分解的化学方程式为。
-
(2) 用排水法收集氧气的原因。
实验室现有石灰石、高锰酸钾、稀盐酸、二氧化锰、火柴、棉花、升降台及下列仪器,请回答下列问题:

-
(1) 经过思考,张南同学认为利用上述仪器及药品可以制取的气体是①,若要选择仪器X来检验该气体,需要补充的一种药品是②,气体应从③(填字母)端通入仪器X。实验中会观察到液面下的导管口有气泡冒出,这是因为发生装置内物质反应时气体④,压强⑤,大于外界压强,在压强差的作用下,气体从导管口冒出。
-
(2) 若补充① (填仪器名称),再利用上述仪器及药品还可以制取另一种气体,请写出制取该气体的化学方程式②。
请根据下列各图中提供的信息回答问题。

-
(1) 写出仪器a的名称:。
-
(2) 请写出用装置B制取二氧化碳的化学方程式:,证明二氧化碳收集满的方法是。
-
(3) 比较用过氧化氢溶液和用氯酸钾固体制取O2的方法,两者的共同点是( )A . 发生装置相同 B . 都可用MnO2做催化剂 C . 完全反应后剩余的固体成分相同
-
(4) 装置B,C都可用来制取二氧化碳,装置C相对于装置B在操作方面的优势是。
-
(5) 用大理石和稀盐酸制取一瓶二氧化碳气体,将这瓶气体按G所示慢做倒入烧杯中,观察到,说明二氧化碳具有的性质是。
-
(6) 实验室用装置A制取氧气的化学方程式为:;若用D装置收集氧气,实验操作中当等到再收集。
依据下列实验装置图,回答问题:
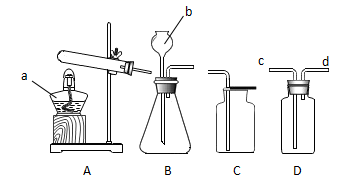
-
(1) 上述装置中,仪器a的名称是,仪器b的名称是。
-
(2) 在实验室用装置A制取O2 , 试管口放一小团棉花的作用是,该反应的化学方程式。若用装置D收集O2,则气体从端通入(填“c”或“d”)。
-
(3) 实验室制取CO2时发生反应的化学方程式为。若用装置C收集CO2。检验CO2是否收集满的操作是,若在装置D中盛有足量澄清石灰水。再通入CO2,能观察到的实验现象是。
氧气的化学性质比较活泼,能支持燃烧.
①如何验证一瓶无色气体是氧气?
②可燃物燃烧的剧烈程度与氧气浓度或接触面积等因素有关,任举一例加以说明.
实验室开放日,某化学兴趣小组的同学在老师的指导下,设计了如下实验装置进行气体制取和性质的探究,请回答有关问题:
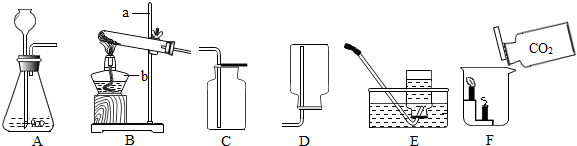
-
(1) 实验室用氯酸钾和二氧化锰混合制取氧气时,应选用的发生装置是(填写装置的字母代号,下同),请写出该反应的化学方程式:,其中二氧化锰起作用。
-
(2) 实验室制取二氧化碳气体时,应选择的发生装置是,验证收集的二氧化碳已满的方法是。
-
(3) 如图F所示,向烧杯中倾倒二氧化碳,下层蜡烛先熄灭,上层蜡烛后熄灭,说明二氧化碳具有的化学性质是。
如图是实验室制取气体的常用装置。

-
(1) 写出标号①仪器的名称:。
-
(2) 实验室制氧气可以选择装置C,发生反应的化学方程式是,试管口需放一团棉花,作用是。若用F装置收集氧气,氧气应从(选填“a”、“b”)导管通入。
-
(3) 实验室可以利用块状大理石(有效成分碳酸钙CaCO3)和一种叫稀盐酸(有效成分HCl)的溶液来制取二氧化碳,发生装置可选用A或B。原因是,二者反应后生成氯化钙(CaCl2)、水和二氧化碳,则发生反应的化学方程式是,与装置A相比,装置B的优点是。二氧化碳的密度大于空气且能溶于水,收集二氧化碳可选用的装置是(填字母)。
-
(4) 同学们学习氧气后发现,许多物质在氧气中能剧烈燃烧,如:蜡烛在氧气中燃烧且有明亮的火焰;铁丝也能在氧气中燃烧,但是没有火焰。针对这些问题同学们进行实验请你参与他们的实验探究。
(a)写出实验室用过氧化氢溶液和二氧化锰制取氧气的化学方程式。同学们对铁丝在氧气中燃烧的实验进行了改进,用适量10%的过氧化氢溶液和二氧化锰代替原实验集气瓶中的水(如图1所示),其优点是实验简便且保证安全,还有;实验观察到的现象是铁丝剧烈燃烧、火星四射、,反应的化学方程式为。
(b)点燃蜡烛,用坩埚钳夹持一根尖嘴玻璃管,将其末端插入燃着的蜡烛烛心附近,一段时间后用火柴在玻璃管尖嘴处点燃,有火焰产生(如图2所示)由此可知,蜡烛燃烧产生的火焰是由(选填“固态”或者“气态”)石蜡燃烧形成的。要使该实验成功,同学们认为尖嘴玻璃管不宜过长,原因是。

空气是一种宝贵的自然资源。下列有关空气的说法错误的是( )
A . 氮气的化学性质不活泼,可用于食品的防腐
B . 工业上利用空气来获取氧气
C . 空气的成分按质量计算,氧气大约占 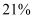 D . 禁止燃放烟花爆竹,可以减少空气污染
D . 禁止燃放烟花爆竹,可以减少空气污染
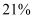 D . 禁止燃放烟花爆竹,可以减少空气污染
D . 禁止燃放烟花爆竹,可以减少空气污染
实验室常用过氧化氢溶液与二氧化锰制氧气,请回答下列问题:
-
(1) 反应的化学方程式为。
-
(2) 下列仪器中A的名称是,实验中,为了得到平稳的气流,最适合的装置组合是(填字母)。

-
(3) 若用排水集气法收集一瓶体积分数约为80%的氧气,预先应向容积为360 mL的集气瓶中加水,水的体积约为mL(氧气约占空气总体积的
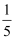 )。
)。
如图是实验室制取气体的常见装置。请回答下列问题:


-
(1) 仪器②的名称是。
-
(2) 用A和F装置制取氧气,反应的化学方程式是。
-
(3) 制取二氧化碳的发生装置可选用B或C,与B相比,C装置的优点是。
-
(4) 若用G装置收集二氧化碳,应将二氧化碳从(填“a”或“b”)通入,检验二氧化碳是否收集满的方法是。
探究“化学实验”奥秘,如图是实验室制取气体的发生装置和气体收集装置。请你回答下列问题:

-
(1) 仪器a的名称是,仪器b的名称是。
-
(2) 实验室用过氧化氢溶液制取氧气,其反应的符号表达式是,若从控制反应速率和节约药品的角度考虑,应选择的发生装置是(填字母编号)。
-
(3) D、E、F、G都是实验室中气体的收集装置,其中不能用来收集氧气的是(填字母编号)。若用G装置收集一瓶O2 , 则应该进出,验满的方法是。
-
(4) 用收集的氧气完成铁丝燃烧的实验,集气瓶中预先放少量水的原因是;铁丝燃烧的符号表达式为。
-
(5) 如图是硫在氧气和空气中燃烧的实验,下列说法错误的是。

A 氧气含量越多硫燃烧越剧烈
B 硫在氧气中燃烧发出蓝紫色火焰
C 瓶底的水可以吸收生成的有害气体
D 硫在空气和氧气中燃烧的生成物不同
现有A、B、C、D、E、F、G、H、I九种初中化学常见的物质,常温下,A、B都无色液体且组成元素相同,C、D为气体单质,E为黑色固体,F、I是常见的无色气体且具有相同组成元素,G为大理石的主要成分,H是一种不稳定的酸,它们之间转化关系如图所示.回答下列问题:

-
(1) 写出化学式:A,F,
-
(2) 写出化学方程式:反应①,反应⑥.
-
(3) 反应⑤在工业上有何用途?.
化学兴趣小组同学完成了以下两个实验。请回答:


-
(1) Ⅰ、实验一
写出仪器名称:a,b;
-
(2) 实验室用氯酸钾和二氧化锰混合加热制取氧气,该反应的文字表达式为; 发生和收集装置可选用(填序号);若收集到的氧气不纯净,可能原因是。
-
(3) 查阅资料得知,相同条件下,氨气(NH3)的密度比空气小,且易溶于水,其水溶液称为氨水。则收集氨气应选择的装置是(填序号)。
-
(4) Ⅲ、实验二
比较步骤②与步骤③观察到的现象,说明燃烧剧烈程度与有关。
-
(5) 步骤④的实验目的是,观察到的现象为。
下列说法正确的是( )
A . 水中溶有较多的氯化钙时,加入肥皂水后,产生的泡沫较少
B . 只要化学反应前后质量和化学性质不变,那么该物质就是催化剂
C . 一种化合物中同种元素的化合价一定相等
D . 所有原子的原子核一定是由质子和中子构成
下列关于催化剂的说法正确的是( )
A . 可以增加生成物的质量
B . 能改变化学反应速率
C . 在化学反应后其质量增加
D . 二氧化锰可以作任何反应的催化剂
最近更新



