第四章 保护生存环境 知识点题库
-
(1) 铜与浓硝酸反应生成NO2的化学反应方程式是
-
(2) NO2可用水吸收,该反应的化学反应方程式是
-
(3) 工业上可将SO2通入浓的Fe2(SO4)3溶液中来治理污染得副产物绿矾和硫酸,写出该反应的离子方程式
-
(4)
利用反应6NO2+8NH3
 7N2+12H2O也可处理NO2 . 当反应转移0.6mol电子时,则消耗的NH3在标准状况下的体积是
7N2+12H2O也可处理NO2 . 当反应转移0.6mol电子时,则消耗的NH3在标准状况下的体积是 -
(5) 已知:2SO2(g)+O2(g)⇌2SO3(g)△H1=﹣196.6kJ•mol﹣1
2NO(g)+O2(g)⇌2NO2(g)△H2=﹣113.0kJ•mol﹣1
则反应NO2(g)+SO2(g)⇌SO3(g)+NO(g)的△H= kJ•mol﹣1 .
一定条件下,将NO2与SO2以物质的量之比1:2置于恒容密闭容器中发生上述反应.
①下列能说明反应达到平衡状态的是 .
A.体系压强保持不变
B.SO3和NO的体积比保持不变
C.混合气体颜色保持不变
D.每消耗1mol SO3的同时消耗1mol NO2
②测得上述反应平衡时NO2与SO2物质的量之比为1:11,该反应的平衡常数
K= (保留1位小数).
(1)家庭装修所用的复合板材中常会放出对人体有严重危害的物质,这种有害物质只要是指 (填名称).
(2)天然水中含有的细小悬浮颗粒可以用明矾做进行净化处理,明矾水解得到的 可以吸附细小悬浮颗粒.
(3)为了改善空气质量,必须控制大气中二氧化硫、氮氧化物、烟尘等污染物的排放量.为控制大气中二氧化硫的排放,常采取的措施是在煤炭中加入石灰石粉末对化石燃料进行脱硫处理,其原理用方程式可表示为
选项 | 叙述Ⅰ | 叙述Ⅱ |
A | 纯碱是强碱弱酸盐 | 用纯碱溶液可清洗油污 |
B | 不锈钢是合金 | 不锈钢在潮湿环境中容易被腐蚀 |
C | Fe2O3是碱性氧化物 | Fe2O3可用作红色油漆和涂料 |
D | NO2是红棕色气体 | 常温下可用铜与浓硝酸制取NO2 |
-
(1) 甲组采用如下装置脱硫(部分装置略)。

① CaO脱硫后的产物是。
② b中品红很快褪色,说明脱硫效果不好。下列措施能提高脱硫效果的是。
ⅰ. 加快SO2气体流速
ⅱ. 将堆集在一起的CaO平铺在整个玻璃管
ⅲ. 加热a,脱硫效果可能会更好
③ 小组拟通过CaO的增重评价其脱硫能力。需要测量的数据是。
-
(2) 乙组选用AgNO3溶液脱除SO2 。

现象:通入SO2 , 立即生成大量白色沉淀A。
对白色沉淀A的成分进行探究,提出假设:
假设1:发生了氧化还原反应,依据是AgNO3溶液中含有O2、
 等具有氧化性的粒子,沉淀A主要是Ag2SO4(微溶)。
等具有氧化性的粒子,沉淀A主要是Ag2SO4(微溶)。假设2:发生了复分解反应,依据是SO2与水生成酸,能与AgNO3溶液发生复分解反应。
实验探究:
① 取沉淀A,加入蒸馏水,静置。取上层清液滴加Ba(NO3)2溶液,无明显变化。
② 取,加入蒸馏水,静置。取上层清液滴加Ba(NO3)2溶液,产生沉淀。
实验证明“假设1”不成立。
③ 为进一步确认“假设2”,向A中加入浓HNO3 , 立即产生红棕色气体。加入浓硝酸的目的是;经确认,反应后混合液存在SO
 。
。 实验证明“假设2”成立。
④ 产生沉淀A的化学方程式是。AgNO3溶液具有良好的脱硫能力,但因其价格高,未能大规模使用。
-
(3) 丙组用NaClO脱除SO2 , 用1 L 0.1 mol/L 的NaClO溶液最多可以吸收标准状况下的SO2L。
该法的工艺流程为: 
其中第①步存在平衡2CrO42−(黄色)+2H+⇌Cr2O32−(橙色)+H2O
-
(1) 若平衡体系的pH=2,该溶液显色.
-
(2) 能说明第①步反应达平衡状态的是_____(填序号)A . Cr2O72−和CrO42−的浓度相同 B . 2v(Cr2O72−)=v(CrO42−) C . 溶液的颜色不变
-
(3) 第②步中,还原1molCr2O72−离子,需要mol的FeSO4•7H2O.
-
(4) 第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)⇌Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)•c3(OH-)=10-32 , 要使c(Cr3+)降至10-5mol/L,溶液的pH应调至.
-
(5) 方法2:电解法.
该法用Fe做电极电解含Cr2O72−的酸性废水,随着电解的进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀.
用Fe做电极的原因为(用电极反应式解释).
-
(6) 在阴极附近溶液pH升高,溶液中同时生成的沉淀还有.
![]()
![]()
![]()
![]()
![]()
![]()
![]()
-
(1) 若A常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
①D的化学式是;
②在工业生产中B气体的大量排放被雨水吸收后形成而污染了环境。
-
(2) 若A在常温下为气体,C是红棕色的气体.
①A、C的化学式分别是:A;C。
② C→D反应的化学方程式 ;该反应(填“属于”或“不属于”)氧化还原反应。
-
(1) 工业上用氢气和氮气直接合成氨,写出反应的化学方程式。氨气极易溶于水,水溶液显 性,能使酚酞溶液变色,使湿润的红色石蕊试纸变色。
-
(2) 氮的氧化物有多种,一氧化氮和二氧化氮都是大气污染物。氨气在催化剂作用下可被氧化生成一氧化氮,一氧化氮气体与空气变色,原因是(用化学方程式表示);二氧化氮易溶于水并与水反应,此反应的氧化剂是,还原剂是,氧化剂和还原剂的质量之比为
| 选项 | 用途 | 解释 |
| A | Na可用于与TiCl4反应得Ti粉 | Na具有强还原性 |
| B | 明矾可用于净水 | 明矾能杀菌消毒 |
| C | Na2O2可用于潜水艇制O2 | Na2O2具有强氧化性 |
| D | MgO、Al2O3可用于制作耐高温坩埚 | MgO、Al2O3在高温下化学性质稳定 |
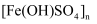 能用作净水剂(絮凝剂),可由绿矾(
能用作净水剂(絮凝剂),可由绿矾(  )与
)与 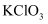 在水溶液中反应得到:
在水溶液中反应得到: 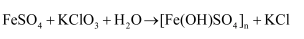 (未配平)下列说法正确的是( )
(未配平)下列说法正确的是( )
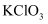 作氧化剂,每消耗
作氧化剂,每消耗 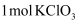 可生成
可生成 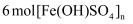 B . 生成聚合硫酸铁后,水溶液的
B . 生成聚合硫酸铁后,水溶液的  变小
C . 聚合硫酸铁可在水中形成氢氧化铁胶体而净水
D . 在相同条件下,
变小
C . 聚合硫酸铁可在水中形成氢氧化铁胶体而净水
D . 在相同条件下, 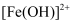 比
比  的水解能力更强
的水解能力更强




