第一节 改善大气质量 知识点题库
-
(1)
冶炼废水中砷元素主要以亚砷酸(H3AsO3)形式存在,可用化学沉降法处理酸性高浓度含砷废水,其工艺流程如下:
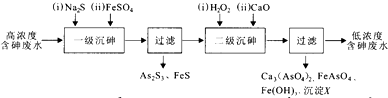
已知:I.As2 S3与过量的S2一存在以下反应:As2S3+3S2﹣⇌2AsS
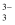
II.亚砷酸盐的溶解性大于相应砷酸盐
①亚砷酸中砷元素的化合价为.
②砷酸的电离方程式为.
③“一级沉砷”中FeSO4的作用是.
④“二级沉砷”中H2 O2与含砷物质反应的化学方程式为.
⑤沉淀X为(填化学式).
-
(2) 冶炼废渣中的砷元素主要以As203的形式存在,可用古氏试砷法半定量检测(As的最低检出限为3.0x 10 ﹣6g).
步骤1:取10g废渣样品,粉碎后与锌粉混合,加人H2 SO4共热,生成AsH3气体.
步骤2:将AsH3气体通入AgNO3溶液中,生成银镜和As2 O3 .
步骤3:取1g废渣样品,重复上述实验,未见银镜生成.
①AsH3的电子式为.
②步骤2的离子方程式为.
③固体废弃物的排放标准中,砷元素不得高于4.0×10一5g•kg一1 , 请通过计算说明该废渣是否符合排放标准.
Ⅰ某校研究性学习小组设计如图流程以回收铜和硫酸亚铁.请回答:

-
(1) 反应①的离子方程式为.
-
(2) 操作①中用到的玻璃仪器是(填序号).
a.烧杯 b.漏斗 c.玻璃棒 d.酒精灯
-
(3) 固体成分是(填名称).
-
(4) 原料②的名称为.
-
(5) Ⅱ回收的铜可用于制备胆矾(CuSO4•5H2O).,可将铜和一定浓度稀硫酸混合后并在加热的情况下通入氧气,发生如下反应:2Cu+2H2SO4+O2
 2CuSO4+2H2O.制得硫酸铜溶液后经过蒸发、浓缩,冷却结晶,过滤可得胆矾.
2CuSO4+2H2O.制得硫酸铜溶液后经过蒸发、浓缩,冷却结晶,过滤可得胆矾.①请分析2Cu+2H2SO4+O2
 2CuSO4+2H2O反应中,氧化剂是,还原剂是(填化学式).
2CuSO4+2H2O反应中,氧化剂是,还原剂是(填化学式).②用双线桥标出上述反应的电子得失.

-
(1) 通常状况下,NO2的颜色是;
-
(2) 反应①的化学方程式是;
-
(3) NO2易溶于水,并和水发生化学反应。该反应中,氧化剂是;
-
(4) 化合物A的化学式是;
-
(5) 治理汽车尾气的一种方法是用催化剂使NO与CO发生反应:
2NO + 2CO = 2CO2 + N2。当生成2mol N2时,被还原的NO为mol。
-
(1) 酸雨是指pH的雨水。
-
(2) NOx主要来源于汽车尾气。硝酸型酸雨的形成过程中涉及的化学方程式有:①
 ;②
;② 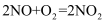 ;③。
;③。
-
(3) SO2主要是煤、石油等燃烧产生,为减少SO2的排放,可采取下列有效措施:
①在含硫煤中加入生石灰可以起到固硫的作用,燃烧过程中,硫元素转化成其最高价态的化合物,该化合物的化学式是。
②在一定条件下用CO还原SO2得到单质硫的方法来除去SO2 , 该反应的化学方程式为。
③用氨水将SO2转化为NH4HSO3 , 再氧化成
 来脱除烟气中的SO2 , 原理是、(用离子方程式表示)。
来脱除烟气中的SO2 , 原理是、(用离子方程式表示)。
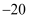 ”飞机上大量使用的碳纤维是一种新型有机高分子材料
D . 工业用乙烯直接氧化法制环氧乙烷体现了“绿色化学”和“原子经济”
”飞机上大量使用的碳纤维是一种新型有机高分子材料
D . 工业用乙烯直接氧化法制环氧乙烷体现了“绿色化学”和“原子经济”
-
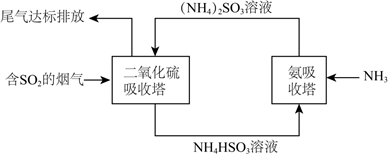
(1) I.某企业利用下列流程综合处理工厂排放的含有
 的烟气,以减少其对环境造成的污染。试回答下列问题:
的烟气,以减少其对环境造成的污染。试回答下列问题: 二氧化硫吸收塔中发生反应的化学方程式为。
-
(2) 氨吸收塔中发生反应的离子方程式为。
-
(3) 一定条件下,通过下列反应可实现燃煤烟气中硫的回收:
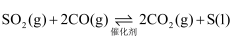 ,该反应的能量变化如图所示。
,该反应的能量变化如图所示。 
①该反应为(填“放热”或“吸热”)反应。
②如果要提高该反应的反应速率,可以采取的措施是(选填编号)
A.减压 B.增加
 的浓度 C.升温 D.及时移出产物
的浓度 C.升温 D.及时移出产物 -
(4) II.用活性炭还原法处理氮氧化物。有关反应为:
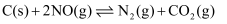 某研究小组向一个容器容积为3L且容积不变的密闭真空容器(固体试样体积忽略不计)中加入
某研究小组向一个容器容积为3L且容积不变的密闭真空容器(固体试样体积忽略不计)中加入 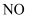 和足量的活性炭,在恒温(T1℃)条件下反应,测得不同时间(t)时各物质的物质的量(n)如表:
和足量的活性炭,在恒温(T1℃)条件下反应,测得不同时间(t)时各物质的物质的量(n)如表: 时间/min
NO物质的量(mol)
 物质的量(mol)
物质的量(mol) 物质的量(mol)
物质的量(mol)0
2.00
0
0
10
1.16
a
a
20
b
0.60
0.60
30
b
0.60
0.60
①表中b=,计算T1℃时
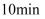 内,用
内,用  浓度增加来表示该反应的平均速率。
浓度增加来表示该反应的平均速率。②下列各项能判断该反应达到平衡状态的是(填序号字母)。
A.
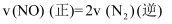 B.容器内
B.容器内  和
和  的体积比为
的体积比为 
C.混合气体的平均相对分子质量保持不变 D.容器内压强保持不变



