第二节 爱护水资源 知识点题库
下列物质误食后不会引起中毒的是 ( )
A . 味精
B . NaNO2
C . CH3OH
D . 白磷
为探究物质的燃烧条件,某同学进行了如图所示的实验,下列有关说法正确的是( )
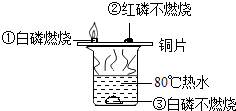
A . 现象①③说明物质燃烧需要达到一定的温度
B . 现象②③说明物质燃烧需要氧气
C . 现象①②说明白磷的着火点比红磷的着火点低
D . 现象②说明红磷不是可燃物
2014年3月9日凌晨,一辆拖挂车装载150桶约30吨白磷驶往山东,在雅西高速西昌收费站附近发生侧翻,车上白磷泄漏燃烧,大量白色烟雾飘进西昌城区.
-
(1) 工业上用磷酸钙,木炭和二氧化硅混合高温制取白磷,并生成常见气体和硅酸盐.其化学方程式为:;
-
(2) 已知白磷(P4)为正四面体分子,其燃烧产物分子结构相当于P4分子中每最近两个磷原子之间镶入一个氧原子,且每个磷原子另与一个氧原子成键,则该燃烧产物分子式为,消防队员喷水将其吸收,所得产物中所含化学键类型为;
-
(3) 磷元素的简单氢化物分子空间构型为,它可以在在空气中燃烧,但燃烧后残余少量P2H4分子,该分子电子式为.
-
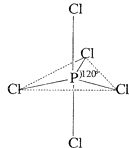
(4) 白磷(P4)易被卤素单质氧化成卤化磷,卤化磷通常有三卤化磷或五卤化磷.PCl5分子结构如图所示,它与水反应的化学方程式为:;
-
(5) 白磷和氯、溴反应,生成混合卤化磷PCl5﹣xBrx(1≤x≤4,且x为整数).若某混合卤化磷共有3种不同结构,该混合卤化磷的分子式为.
PH3 是一种无色剧毒气体.下列判断错误的是( )
A . PH3 分子是非极性分子
B . PH3分子中有一对电子孤对
C . PH3 分子VSEPR模型的名称是四面体
D . PH3 分子稳定性低于 NH3 分子
下列说法中正确的是( )
A . 生石灰可用作食品抗氧化剂
B . 焰色反应是物质燃烧时火焰呈现的颜色变化,属于化学变化
C . “海水淡化”可以解决“淡水供应危机”,但加入明矾不能使海水淡化
D . 分散系中分散质粒子的大小:Fe(OH)3悬浊液<Fe(OH)3 胶体<FeCl3溶液
下列说法错误的是( )
A . FeSO4常用于制取净水剂,原因是溶于水时形成具有净水作用的氢氧化亚铁胶体
B . 纳米铁粉和FeS都可以去除水体中的Cu2+、Hg2+等离子,其原理不相同
C . SO2具有还原性,可用KMnO4溶液测定食品中SO2残留量
D . 利用碳酸钠溶液可消除燃煤烟气中的SO2
2020年4月20日,习.平总书记来到秦岭,关注山清水秀。下列做法正确的是( )
A . 集中深埋废旧电池
B . 远海排放工业污水
C . 减少冶炼含硫矿物
D . 推广使用一次性木筷
半导体生产中常需要使用掺杂剂,以保证控制电阻率,三氯化磷(PCl3)是一种重要的掺杂剂。实验室要用黄磷(即白磷)与干燥的Cl2模拟工业生产制取PCl3,装置如图所示:(部分夹持装置略去)
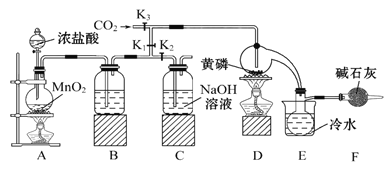
已知:①黄磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5;②PCl3遇水会强烈水解生成H3PO3和HCl;③PCl3遇O2会生成POCl3,POCl3溶于PCl3;④PCl3、POCl3的熔沸点见下表:
| 物质 | 熔点/℃ | 沸点/℃ |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
请回答下列问题:
-
(1) B中所装的试剂是,F中碱石灰的作用是。
-
(2) 实验时,检査装置气密性后,先打开K3、关闭K1 , 通入干燥的CO2,再迅速加入黄磷。通干燥CO2的作用是,通过控制K1、K2能除去A、B装置中的空气,具体的操作是。
-
(3) 粗产品中常含有POCl3、PCl5等。加入黄磷加热除去PCl5后,通过(填实验操作名称),即可得到较纯净的PCl3。
-
(4) 通过下面方法可测定产品中PCl3的质量分数:
①迅速称取1.00 g产品,加水反应后配成250 mL溶液;
②取以上溶液25.00 mL,向其中加入淀粉作为指示剂
③向其中加入 0.1000 mol·L-1碘水,充分反应,当达到终点时消耗碘水溶液6.9mL。已知:H3PO3+H2O+I2===H3PO4+2HI,假设测定过程中没有其他反应。
滴定时,滴定终点的现象是,配制0.1000 mol·L-1的碘水溶液的过程中,下列操作会使所得溶液浓度偏大的是
A烧杯中溶液转移至容量瓶中时,未洗涤烧杯
B定容时俯视刻度线
C定容时仰视刻度线
D容量瓶未干燥
E移液时有少量液体溅出
F溶解碘时放热,未冷却至室温就转移至容量瓶并定容
根据上述数据,该产品中PCl3的质量分数为。
化学知识在生产和生活中有着重要的应用。下列说法中正确的是( )
①钠的还原性很强,可以用来冶炼金属钛、钽、铌、锆等
②K、Na合金可作原子反应堆的导热剂
③发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔
④Na2O2既可作呼吸面具中O2的来源,又可漂白织物、麦杆、羽毛等
⑤碳酸钠在医疗上是治疗胃酸过多的一种药剂
⑥明矾常作为消毒剂
A . ①②③④
B . ①②③④⑤
C . ①②③④⑥
D . ①②③④⑤⑥
下列“化学与生活”的说法错误的是( )
A . 硫酸钡可用钡餐透视
B . 盐卤可用于制豆腐
C . 明矾可用于水的消毒、杀菌
D . 醋可用于除去暖水瓶中的水垢
下列说法错误的是( )
A . 二氧化硫可用于漂白纸浆
B . 热的纯碱溶液可以去除厨房里的油污
C . 目前用于饮用水净化的含铝净水剂正逐步被含铁净水剂所取代
D . 钢铁因含杂质而容易生锈,所以合金一定不耐腐蚀
聚合硫酸铁 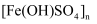 能用作净水剂(絮凝剂),可由绿矾(
能用作净水剂(絮凝剂),可由绿矾(  )与
)与 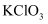 在水溶液中反应得到:
在水溶液中反应得到: 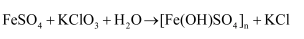 (未配平)下列说法正确的是( )
(未配平)下列说法正确的是( )
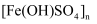 能用作净水剂(絮凝剂),可由绿矾(
能用作净水剂(絮凝剂),可由绿矾(  )与
)与 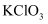 在水溶液中反应得到:
在水溶液中反应得到: 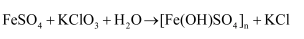 (未配平)下列说法正确的是( )
(未配平)下列说法正确的是( )
A . 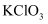 作氧化剂,每消耗
作氧化剂,每消耗 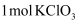 可生成
可生成 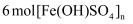 B . 生成聚合硫酸铁后,水溶液的
B . 生成聚合硫酸铁后,水溶液的  变小
C . 聚合硫酸铁可在水中形成氢氧化铁胶体而净水
D . 在相同条件下,
变小
C . 聚合硫酸铁可在水中形成氢氧化铁胶体而净水
D . 在相同条件下, 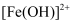 比
比  的水解能力更强
的水解能力更强
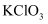 作氧化剂,每消耗
作氧化剂,每消耗 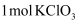 可生成
可生成 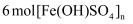 B . 生成聚合硫酸铁后,水溶液的
B . 生成聚合硫酸铁后,水溶液的  变小
C . 聚合硫酸铁可在水中形成氢氧化铁胶体而净水
D . 在相同条件下,
变小
C . 聚合硫酸铁可在水中形成氢氧化铁胶体而净水
D . 在相同条件下, 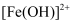 比
比  的水解能力更强
的水解能力更强
下列说法错误的是( )
A . 金属铝密度小、硬度大,可用于制造飞机等部件
B . 硫酸钡难溶于水,医疗上可用作检查肠胃的内服药剂
C . 工业上可采用高温冶炼黄铜矿的方法获得粗铜
D . 氯化铁、硫酸铁可用做净水剂
回答下列问题:
-
(1) 漂白粉是一种常用消毒剂,其中的有效成分是 (写出化学式)。
-
(2) 高铁酸钠(Na2FeO4)可以用作自来水处理剂,高铁酸钠处理过程中有氢氧化铁胶体生成,则高铁酸钠作自来水处理剂的优点是。
-
(3) 铁是应用最广泛的金属,铁有卤化物、氧化物以及高价铁的含氧酸盐等。电子工业常用 30%的 FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。请写出 FeCl3 溶液与铜反应的离子方程式 ;如何检验 FeCl3 腐蚀铜后的溶液是否含 Fe3+ 。
-
(4) 在用二氧化氯进行水处理时,ClO2 除了杀菌消毒外,还能除去水中的 Fe2+和 Mn2+。用 ClO2氧化除去 Mn2+生成
 和 MnO2的离子方程式为 。
和 MnO2的离子方程式为 。
下列说法错误的是( )
A . 可用电渗析法进行海水淡化
B . 煤的干馏是指煤在空气中加强热使其分解的过程
C . 大量排放含磷污水会导致水质恶化
D . 硫氧化物和 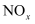 是形成酸雨的主要物质
是形成酸雨的主要物质
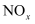 是形成酸雨的主要物质
是形成酸雨的主要物质
下列说法正确的是( )
A . 光化学烟雾、臭氧层空洞、温室效应的形成都与氮的氧化物有关
B . 中国“神州十三”号载人飞船上用的钛合金比纯钛具有更优良的性能
C . 牙膏中添加氟化物可用于预防龋齿,原因是氟化物具有氧化性
D . 自来水厂常用明矾、O3、ClO2等作水处理剂,其作用都是杀菌消毒
从科技前沿到日常生活,化学无处不在。下列说法不正确的是( )
A . 我国首次在实验室实现了二氧化碳到淀粉的合成,生物酶催化剂的使用改变了反应历程
B . 神州十三号顺利升空时,火箭尾部喷射的气体呈红棕色是因为部分助燃剂 转化为
转化为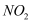 C . 水是21世纪最宝贵的资源之一,明矾与高铁酸钾均可作水处理剂,两者处理水的原理相同
D . 2022年北京冬奥会将采用石墨烯材料制造户外保暖穿戴设备,石墨烯中碳原子为
C . 水是21世纪最宝贵的资源之一,明矾与高铁酸钾均可作水处理剂,两者处理水的原理相同
D . 2022年北京冬奥会将采用石墨烯材料制造户外保暖穿戴设备,石墨烯中碳原子为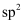 杂化
杂化
 转化为
转化为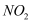 C . 水是21世纪最宝贵的资源之一,明矾与高铁酸钾均可作水处理剂,两者处理水的原理相同
D . 2022年北京冬奥会将采用石墨烯材料制造户外保暖穿戴设备,石墨烯中碳原子为
C . 水是21世纪最宝贵的资源之一,明矾与高铁酸钾均可作水处理剂,两者处理水的原理相同
D . 2022年北京冬奥会将采用石墨烯材料制造户外保暖穿戴设备,石墨烯中碳原子为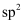 杂化
杂化
化学与生活息息相关。下列说法不正确的是( )
A . 84消毒液和洁厕灵不能混合使用,因为会产生有毒的氯气
B . 明矾净水是因为明矾可以对自来水进行消毒杀菌
C . 硫氧化物的超量排放是造成酸雨的原因之一
D . 汽车尾气中含有氮氧化物和碳氧化物,因此应提倡绿色出行
化学与生产、生活、环境密切相关。下列说法正确的是( )
A . 荧光材料BGO的主要成分锗酸铋(Bi2Ge2O7)属于无机非金属材料
B . 活性炭具有还原性,可用于除去水体中Pb2+等重金属离子
C . 棉、丝、羽毛及塑料完全燃烧都只生成CO2和H2O
D . “燃煤脱硫”有利于实现“碳达峰、碳中和
化学与人体健康及环境保护息息相关。下列叙述错误的是( )
A . 酸雨是指pH小于5.6的酸性降水
B . 非处方药的包装上印有“OTC”标识
C . 过量使用氮肥不会造成水体污染
D . 水果罐头中添加维生素C起抗氧化作用
最近更新



